【答案】
分析:(1)铜与浓硫酸反应加热条件下生成硫酸铜、二氧化硫、水,依据氧化还原反应写出化学方程式;
(2)二氧化硫是酸性氧化物溶于水生成亚硫酸显酸性,二氧化硫的漂白性具有选择性;
(3)二氧化硫的漂白作用不稳定,加热恢复原来的颜色;
(4)浓硫酸溶液中水是水合分子形式,开始反应生成水少,与铜反应开始生成的硫酸铜沉淀;
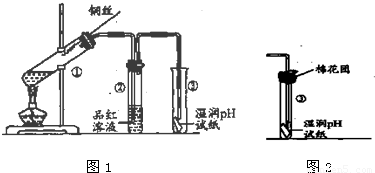
(5)铜丝离开浓硫酸或停止加热终止反应;
(6)二氧化硫污染空气,棉花应是吸收二氧化硫的溶液,可以是碱溶液,或氧化剂.
解答:解:(1)铜与浓硫酸反应加热条件下生成硫酸铜、二氧化硫、水,依据氧化还原反应写出化学方程式;Cu+2H
2SO
4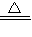
CuSO
4+SO
2↑+2H
2O,
故答案为:Cu+2H
2SO
4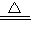
CuSO
4+SO
2↑+2H
2O;
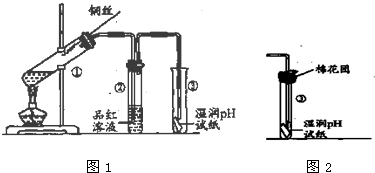
(2)二氧化硫是酸性氧化物溶于水生成亚硫酸显酸性,装置3湿润的PH试纸变红色,证明二氧化硫溶液显酸性;同时证明二氧化硫的漂白性具有选择性,不能漂白变色的pH试纸,
故答案为:酸;不能;
(3)试管2二氧化硫通入后品红变无色,加热恢复原来的颜色红色,说明二氧化硫的漂白性不稳定,二氧化硫和水生成的亚硫酸和有色物质结合成不稳定的无色物质,加热恢复原来的颜色,
故答案为:溶液由无色恢复为红色;说明二氧化硫与有色物质生成的无色物质不稳定;
(4),浓硫酸溶液中水是水合分子形式,开始反应生成水少,与铜反应开始生成的硫酸铜不能溶解;实验初期发现大试管内有白色沉淀生成,
故答案为:CuSO
4 ;
(5)终止试管①中反应的方法是,停止加热或把铜丝抽离浓硫酸溶液,故答案为:停止加热或把铜丝抽离浓硫酸溶液;
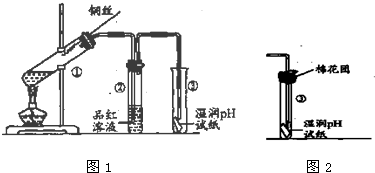
(6)装置中 生成的二氧化硫气体是污染性气体,不能排放到空气中,改进装置中的棉花是吸收二氧化硫的作用,可以用氢氧化钠溶液或高锰酸钾溶液等,
故答案为:NaOH溶液或高锰酸钾溶液;
点评:本题考查了浓硫酸性质的应用,产物性质的分析实验验证方法,反应现象分析,熟练掌握二氧化硫的性质是解题关键,题目难度中等.

 CuSO4+SO2↑+2H2O,
CuSO4+SO2↑+2H2O, CuSO4+SO2↑+2H2O;
CuSO4+SO2↑+2H2O;

 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案