
| A.溶液①中,c(CH3COO-)=c(H+) |
| B.溶液①、②等体积混合,混合液中c(CH3COO-)等于溶液③中的c(CH3COO-) |
| C.溶液①、②等体积混合,混合液中c(CH3COO-)+c(CH3COOH)=c(Na+) |
| D.溶液①、③等体积混合,混合液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
| A.大于 | B.等于 | C.小于 | D.无法确定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| c(H+) |
| c(OH-) |
| A.该溶液中氢离子的浓度:c(H+)=1×10-11mol/L |
| B.0.1mol/L氨水溶液与0.1mol/LHCl溶液等体积混合后所得溶液中:c(NH+4)+c(H+)=c(Cl-)+c(OH+) |
| C.0.1mol/L的氨水溶液与0.05mol/LH2SO4溶液等体积混合后所得溶液中:c(NH+4)+c(NH3)+c(NH3?H2O)=2c(SO2-4) |
| D.浓度均为0.1mol/L的NH3?H2O和NH4Cl溶液等体积混合后,若溶液呈碱性,则c(NH4+)>c(NH3?H2O)>c(Cl-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加NaOH | B.通入H2S气体 |
| C.降温 | D.加入Na2S晶体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.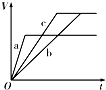 | B. | C. | D. |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③④⑤ | B.②③④⑤⑥ | C.②③⑤⑥⑦ | D.①②⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.强电解质溶液一定比弱电解质溶液的导电性强 |
| B.强电解质的水溶液中不存在电解质分子 |
| C.强电解质都是离子化合物,弱电解质都是共价化合物 |
| D.不同的弱电解质只要物质的量浓度相同,电离程度也就相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Cl2、SO2、NH3的水溶液都能够导电,因此都属于电解质 |
| B.任何一个氧化还原反应都可以设计为电池,输出电能 |
| C.任何可逆反应,其平衡常数越大,反应速率、反应物的转化率就越大 |
| D.电解饱和食盐水的过程中,水的电离平衡正向移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金属单质都能导电,非金属单质都不能导电 |
| B.离子化合物一定不含有共价键 |
| C.只含有共价键的物质一定是非电解质 |
| D.CaCl2在熔融状态下可导电,它是强电解质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com