
【题目】已知常温下氨气能与 CaCl2 固体结合生成 CaCl2·8NH3。下列说法不正确的是
A.CaCl2·6NH3(s)+ 2NH3(g) ![]() CaCl2·8NH3(s) ΔH < 0
CaCl2·8NH3(s) ΔH < 0
B.实验室可用氯化铵固体和熟石灰共热来制备氨气,说明相对高温不利于 CaCl2 与氨气的化合
C.常温下,在密闭容器中缩体加压能增加体系中活化分子百分数,有利于氨气的吸收
D.CaCl2·6NH3(s) CaCl2·c4NH3(s)+ 2NH3(g),He 气流可促进反应进行
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】纯净干燥的氯气与熔融金属锡反应可制备SnCl4,某化学小组的同学设计了如下实验装置进行制备。
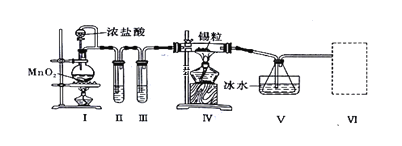
已知:①金属锡熔点为231℃,化学活泼性与铁相似;②SnCl4的沸点为114℃;③SnCl4易与水反应。
请根据上图装置回答:
(1)装置I中反应的离子方程式是________________________________________
(2)试管II中的试剂是________,试管III中的试剂是____________。
(3)装置V的作用是____________。
(4)裝置Ⅵ 最好选用下列装置中的________(填标号)。
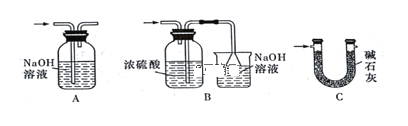
(5)实验结束后,欲回收利用装置Ⅰ中未反应完的MnO2,需要的玻璃仪器有_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用光能分解水的装置如图,在直流电场作用下,双极性膜将水解离为H+和OH,并实现其定向通过。下列说法错误的是( )
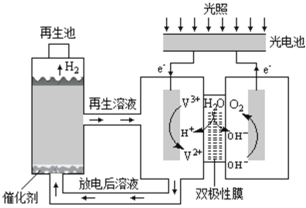
A.光电池能将光能转化为电能
B.阳极区发生的电极反应为:2H2O4e=4H++O2↑
C.双极性膜能控制两侧溶液的酸碱性不同
D.再生池中发生的反应为:2V2++2H+=2V3++H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿比朵尔是一种抗病毒药物,其分子结构如图,关于阿比朵尔说法不正确的是
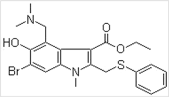
A.阿比朵尔分子式为 C22H24BrN2O3S
B.阿比朵尔能与碱或酸溶液反应生成盐
C.阿比朵尔一定条件下能发生取代、加成、氧化、还原反应
D.一定条件下,1 mol 阿比朵尔与足量 NaOH 溶液反应,最多可消耗 4 mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取软锰矿石(主要成分为![]() )
)![]() 跟足量浓盐酸发生如下反应(杂质不参与反应)
跟足量浓盐酸发生如下反应(杂质不参与反应)![]() ,制得
,制得![]() (标准状况)。下列有关说法中不正确的是( )
(标准状况)。下列有关说法中不正确的是( )
A. 这种软锰矿石中![]() 的质量分数为
的质量分数为![]()
B. 被氧化的![]() 的物质的量为
的物质的量为![]()
C. 参加反应的![]() 的质量为
的质量为![]()
D. 被还原的![]() 的物质的量为
的物质的量为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设[aX+bY]为 a 个 X 微粒和 b 个 Y 微粒组成的一个微粒集合体,N(z)为微粒 z 的数量,NA 为阿伏加德罗常数的值。下列说法一定不正确的是
A.C(石墨)+O2(g) = CO2(g) ΔH=-390 kJ·mol1,则每 1 mol [![]() C(石墨)+
C(石墨)+![]() O2(g)]完全燃烧放热 130 kJ
O2(g)]完全燃烧放热 130 kJ
B.Cu 与 1mol/L 的硝酸溶液充分反应,若生成 22.4 L 气体,则转移电子数为 3NA
C.标准状况下 1.6g 氧气含分子数为 0.05NA,且平均每个 O2 分子的体积约为 ![]() L
L
D.1 mol Cl2 与稀 NaOH 溶液完全反应,则反应后的溶液中 N(ClO)+N(HClO)=1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生为探究钠与二氧化碳的反应,利用如图装置进行实验。
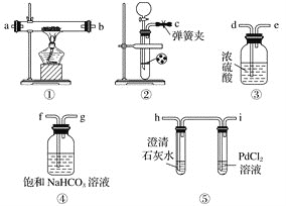
已知PdCl2能被一氧化碳还原得到黑色的Pd。请回答下列问题:
(1)请将上图各装置连接完整:c接f,______接______,______接______,______接______。
(2)若用稀盐酸与碳酸钙反应制备二氧化碳,在加稀盐酸时,发现碳酸钙与稀盐酸不能接触,而稀盐酸又不够了,为使反应能顺利进行,可向长颈漏斗中加入的试剂是______(填字母)。
A.硝酸钠溶液 B.四氯化碳 C.苯 D.稀硝酸
(3)检查装置气密性并装好药品后,点燃酒精灯之前应进行的操作是打开弹簧夹,让二氧化碳充满整个装置,当观察到________________时,再点燃酒精灯。此步操作的目的是________________________________。
(4)反应过程中二氧化碳足量,假如反应过程中有下列两种情况,分别写出两种情况下钠与二氧化碳反应的化学方程式。
Ⅰ.装置⑤PdCl2溶液中观察到有黑色沉淀,装置①中固体成分只有一种,且向固体中加入稀盐酸产生能使澄清石灰水变浑浊的气体: ___________________________。
Ⅱ.装置①中钠的质量为0.46 g,充分反应后,将装置①中的固体加入到足量稀盐酸中产生224 mL(标准状况)二氧化碳气体,且溶液中还有固体残留:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硫酸法钛白粉生产中排放的含锰废水(主要金属离子为Mn2+、Fe2+、Al3+,还含有少量Ca2+、Mg2+、Cu2+和Ni2+等离子)为原料,生产MnCO3的工艺流程如下:
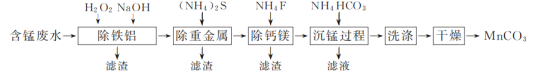
已知:25 ℃时,Ksp(CaF2)=1.5×10-10、Ksp(MgF2)=7.5×10-11。
(1)流程中含锰废水经过前三步预处理,得到主要含有Mn2+的母液。
①除铁铝时,在搅拌条件下先加入H2O2溶液,再加入NaOH溶液调节pH。加入H2O2溶液时发生反应的离子方程式为__________________________________________。
②除钙镁步骤中,当Ca2+、Mg2+沉淀完全时,溶液中![]() =________。
=________。
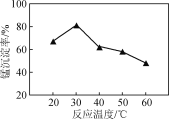
(2) 沉锰过程在pH为7.0条件下充分进行,反应温度对锰沉淀率的影响关系如图所示。
①沉锰过程发生反应的离子方程式为____________。该过程中加入适当过量的NH4HCO3的原因是________。
②当温度超过30 ℃,沉锰反应的锰沉淀率随温度升高而下降的原因是______________________________。
(3) 沉锰后过滤得到MnCO3粗产品,依次用去离子水和无水乙醇各洗涤2~3次,再低温干燥,得到纯净的MnCO3。用无水乙醇洗涤的目的是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无论以何种比例混合的10mL混和气,在50mL的氧气中燃烧生成CO2和液态的H2O,燃烧后所得气体的体积为35mL,则该混合物可能为
A. C3H6 C4H6 B. C2H6 C3H6
C. C2H4 C3H8 D. C2H2 C2H6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com