
 PCl3(g)+Cl2(g) ��H��0 K��1 ��
PCl3(g)+Cl2(g) ��H��0 K��1 �� COCl2(g) ��H ��0 K��5��104 ��
COCl2(g) ��H ��0 K��5��104 �� CO(g)+ Cl2(g) ��H��0 ��
CO(g)+ Cl2(g) ��H��0 �� ��ĩ�����ϵ�д�
��ĩ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 3C( g) ��H����a kJ/mol��a��0�����ﵽƽ��ʱ�ų�������Ϊ bkJ��B���������Ϊ��1�����Իش�
3C( g) ��H����a kJ/mol��a��0�����ﵽƽ��ʱ�ų�������Ϊ bkJ��B���������Ϊ��1�����Իش�| A���¶Ⱥ����һ��ʱ��������ѹǿ���ٱ仯 |
| B���¶Ⱥ����һ��ʱ��ijһ����Ũ�Ȳ��ٱ仯 |
| C������һ������������ƽ����Է����������ٱ仯 |
| D���¶Ⱥ�ѹǿһ��ʱ�����������ܶȲ��ٱ仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����FeCl3��Һ���ɺ��ܵõ�FeCl3���� |
B�����淴Ӧ2SO2+O2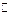 2SO3�У���SO2��O2��SO3�������ʵ���֮��Ϊ2��1��2ʱ��ʾ�Ѵ�ƽ��״̬�ı�־ 2SO3�У���SO2��O2��SO3�������ʵ���֮��Ϊ2��1��2ʱ��ʾ�Ѵ�ƽ��״̬�ı�־ |
| C����������þ�ۼӵ�NH4Cl��Һ����̬����ֻ��H2 |
| D��������ۻ�ʱ���ܵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
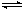 2SO3;��H��-92.6 kJ��mol-1������Ӧ�ﵽƽ��ʱ�����д�ʩ���ٽ����¶ȣ��ڼ�Сѹǿ������V2O5��������������O2��Ũ�ȣ�������SO2��Ũ�ȣ���ѹͨ��He���������SO2ת���ʵ���
2SO3;��H��-92.6 kJ��mol-1������Ӧ�ﵽƽ��ʱ�����д�ʩ���ٽ����¶ȣ��ڼ�Сѹǿ������V2O5��������������O2��Ũ�ȣ�������SO2��Ũ�ȣ���ѹͨ��He���������SO2ת���ʵ���| A���٢ڢ� | B���٢ܢ� | C���ܢݢ� | D���٢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������������ɫ���ƽ����Է����������� | B��ƽ�ⲻ�ƶ�����������ܶ����� |
| C��H2ת��������HIƽ��Ũ�ȱ�С | D��t0ʱ�ı����������ѹ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 CO2��g������2��g�����ﵽƽ��ʱ���n��H2��Ϊ0.5mol������˵������ȷ���� �� ��
CO2��g������2��g�����ﵽƽ��ʱ���n��H2��Ϊ0.5mol������˵������ȷ���� �� ��| A���ڸ��¶���ƽ�ⳣ��K="1" | B��ƽ�ⳣ���뷴Ӧ�¶��� |
| C��CO��ת����Ϊ50% | D��������������ʱ���ı�ѹǿƽ�ⲻ�ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 cC(g)+dD(g)���ﵽ
cC(g)+dD(g)���ﵽ| A��a+b�� c+d | B��ƽ�������ƶ� |
| C�����´�ƽ��ʱ��A����ת�������� | D�����´�ƽ��ʱ��D�����������С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
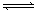 xC��g�����ﵽƽ���C���������Ϊm%����ά�������ݻ����¶Ȳ��䣬��0.6molA��0.3molB��1.4molCΪ��ʼ���ʵ������ﵽƽ���C�����������Ϊm%����x��ֵ����Ϊ
xC��g�����ﵽƽ���C���������Ϊm%����ά�������ݻ����¶Ȳ��䣬��0.6molA��0.3molB��1.4molCΪ��ʼ���ʵ������ﵽƽ���C�����������Ϊm%����x��ֵ����Ϊ�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
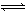 2NO2ƽ������¶Ȳ��䣬��ͨ������N2O4���壬����Ӧ�ﵽ�µ�ƽ��ʱ������ƽ�����ƽ����ȣ���
2NO2ƽ������¶Ȳ��䣬��ͨ������N2O4���壬����Ӧ�ﵽ�µ�ƽ��ʱ������ƽ�����ƽ����ȣ���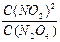 ��ֵ
��ֵ| A����� | B������ | C����С | D����ȷ�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com