
【题目】下列各组物质在一定条件下反应,可以制得较纯净的 1,2-二氯乙烷的是( )
A.乙烷与氯气在光照条件下反应B.乙烯与氯化氢气体混合
C.乙烯与氯气混合D.乙烯通入浓盐酸
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】青蒿素是治疗疟疾的有效药物。用水提取青蒿索需采用较高温度,产品药效较差,改用低温、乙醚冷浸,药效显著提高。若把青蒿素制成双氢青蒿素,其治疗疟疾的效果比青蒿素更好。下列叙述中正确的是
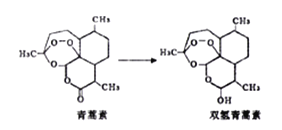
A. 青蒿素的分子式为C15H21O5 B. 双氢青蒿素的水溶性小于青蒿素
C. 青蒿素生成双氢青蒿素属于氧化反应 D. 低温可以减少药物提取过程中过氧键的断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷(As)是第四周期第ⅤA族元素,可以形成As2S3、As2O5、H3AsO3、H3AsO4等化合物,有着广泛的用途。回答下列问题:
(1)工业上用砷废渣制H3AsO4的反应为:2As2S3+5O2+6H2O=4H3AsO4+6S,通常将含砷废渣(主要成分为As2S3)制成浆状,加压通O2氧化。分别分析“制成浆状”、“ 加压通O2”对该反应的影响___________________。
(2)已知:As(s)+ ![]() H2(g)+2O2(g)=H3AsO4(s) △H1
H2(g)+2O2(g)=H3AsO4(s) △H1
2As(s)+O2(g)=As2O5(s) △H2
H2(g)+ ![]() O2(g)=H2O(l) △H3
O2(g)=H2O(l) △H3
则反应As2O5(s)+3H2O(l)=2H3AsO4(s) 的△H=______________。
(3)H3AsO3 和H3AsO4水溶液中含砷的各物种的分布分数(平衡时某物种的依度占各物种浓度之和的分数)与pH的关系分别如图1和图2所示。

①以酚酞为指示剂(变色范围pH:8.0~10.0),将NaOH溶液逐滴加入到H3AsO3溶液中,当溶液由无色变为红色时停止滴加。该过程中主要反应的离子方程式为_______________。
②已知H3AsO4的各级电离常数为Ka1、Ka2、Ka3,则Ka2=_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂排出的铬渣含有SiO2、A12O3、Fe2O3、Na2Cr2O7(易溶于水,是强氧化剂)等,处理建议是将+6价铬转化为低毒性的+3价铬后制备K2Cr2O7。实验室模拟处理铬渣的工艺流程如下(部分操作和条件略):

(1)已知过滤1后的滤液中存在如下平衡:Cr2O72-(橙色)+H2O![]() 2CrO42-(黄色)+2H+,则滤液应呈现的颜色是_________
2CrO42-(黄色)+2H+,则滤液应呈现的颜色是_________
(2)滤渣1的成分为______ 滤渣2中所含的金属元素为___________
(3)根据表中生成成氧化物沉淀的pH数据判断,流程中a的范围为__________。
物质 | Fe(OH)3 | Al(OH)3 | Cr(OH)3 | Fe(OH)2 |
开始沉淀 | 1.5 | 3.4 | 4.9 | 6.3 |
完全沉淀 | 2.8 | 4.7 | 5.5 | 8.3 |
(4)过滤3所得滤液又回流到过滤1所得滤液中,其目的是__________
(5)由Cr(OH)3得到黄色溶液过程中发生的反应的离子方程式是_________
(6)向橙色的K2Cr2O7溶液中,滴加Ba(NO3)2溶液,产生黄色沉淀,溶液pH减小。试推测黄色沉淀是_________,用平衡移动的原理解释溶液pH变小的原因是________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中Q单质可制成半导体材料.下列判断正确的是( )
A.W形成的离子半径大于T形成的离子半径
B.W的单质在过量氧气中燃烧生成WO3
C.最高价氧化物的水化物的酸性:R<Q
D.T是地壳中含量最多的金属元素,其单质的化学性质较活泼
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于自然界中氮循环(如图)的说法正确的是
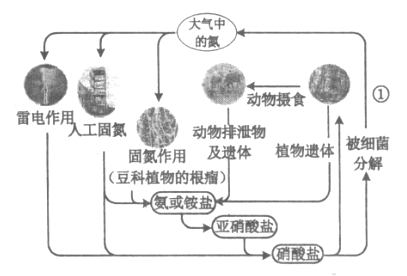
A. “雷电作用”中发生的反应是:![]()
B. 工业合成氨属于人工固氮
C. 氮元素均被还原
D. 过程①必须有O2参与
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,由相同种类元素组成的是 ( )
A.胆固醇、脂肪酸、脂肪酶 B.淀粉、半乳糖、糖原
C.氨基酸、核苷酸、麦芽糖 D.性激素、脱氧核糖、胰岛素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com