

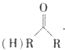
 $\stackrel{HCN}{→}$
$\stackrel{HCN}{→}$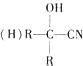 $→_{H+}^{H_{2}O}$
$→_{H+}^{H_{2}O}$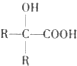
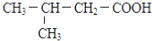 B.
B.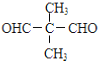 C.
C.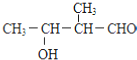 D.
D.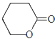
 .
. )可以生物降解,实现在自然界中的循环,是理想的绿色高分 子材料.请以乙醛为有机原料,设计聚乳酸的合成路线.(无机试剂任选,合成路线参照“已 知”中的书写形式)
)可以生物降解,实现在自然界中的循环,是理想的绿色高分 子材料.请以乙醛为有机原料,设计聚乳酸的合成路线.(无机试剂任选,合成路线参照“已 知”中的书写形式) .
. 分析 结合A的分子式可知丙烯与水发生加成反应生成A,A发生催化氧化生成B,B分子中只有一种化学环境的氢原子,则B为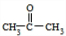 ,A为
,A为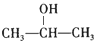 .由题目信息可知,丙酮与HCN发生加成反应,然后酸性条件下反应生成C为
.由题目信息可知,丙酮与HCN发生加成反应,然后酸性条件下反应生成C为 ,C发生消去反应生成D为
,C发生消去反应生成D为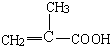 ,D与甲醇发生酯化反应生成E为
,D与甲醇发生酯化反应生成E为 ,
, 发生加聚反应得到PMMA为
发生加聚反应得到PMMA为 .
.
解答 解:结合A的分子式可知丙烯与水发生加成反应生成A,A发生催化氧化生成B,B分子中只有一种化学环境的氢原子,则B为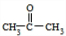 ,A为
,A为 .由题目信息可知,丙酮与HCN发生加成反应,然后酸性条件下反应生成C为
.由题目信息可知,丙酮与HCN发生加成反应,然后酸性条件下反应生成C为 ,C发生消去反应生成D为
,C发生消去反应生成D为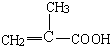 ,D与甲醇发生酯化反应生成E为
,D与甲醇发生酯化反应生成E为 ,
, 发生加聚反应得到PMMA为
发生加聚反应得到PMMA为 .
.
(1)从丙烯→A的反应类型为加成反应,化合物A为 ,含有的官能团为羟基,
,含有的官能团为羟基,
故答案为:加成反应;羟基;
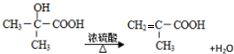
(2)化合物 C→D反应的化学方程式: ,
,
故答案为: ;
;
(3)E为 ,
,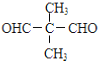 、
、 与 E的分子式相同,结构不同,互为同分异构体,
与 E的分子式相同,结构不同,互为同分异构体,
故答案为:BD;
(4)PMMA的结构简式: ,
,
故答案为: ;
;
(5)从“乙醛(CH3CHO)→聚乳酸(  )”的合成路线流程图为:
)”的合成路线流程图为: ,
,
故答案为: .
.
点评 本题考查有机物推断与合成,注意根据反应条件及给予的信息进行推断,熟练掌握官能团的性质与转化,较较好地考查学生自学能力、知识迁移运用能力,难度中等.


 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 在混合液中加入氢氧化钠溶液,充分振荡后分液 | |
| B. | 在混合液中加人一定量的浓硫酸和乙醇,加热,将乙酸转化为乙酸乙酯 | |
| C. | 在混合液中加人足量的水.充分振荡后分液 | |
| D. | 在混合液中加入适量的饱和碳酸钠溶液,充分振荡后分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 分子式 | C4H10O | C3H8 | C7H16 | C8H10 |
| 限定条件 | 能与钠反应 | 二氯代物 | 分子中含有3个甲基 | 芳香烃,能得到3中硝化产物 |
| 同分异构体数目 | 4 | 3 | 2 | 3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑤ | B. | ①③⑤⑦ | C. | ①③④⑤ | D. | ①②③⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
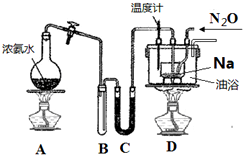 叠氮化钠 (NaN3) 常作为汽车安全气囊的药剂,其固体易溶于水,微溶于乙醇,不溶于乙醚.
叠氮化钠 (NaN3) 常作为汽车安全气囊的药剂,其固体易溶于水,微溶于乙醇,不溶于乙醚.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18O2-结构示意图: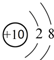 | |
| B. | 硝基苯的结构简式: | |
| C. | NaHSO4熔融时电离方程式:NaHSO4═Na++HSO4- | |
| D. | 模型 可表示甲烷分子或四氯化碳分子 可表示甲烷分子或四氯化碳分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
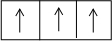 :下列对这种元素的分析中正确的( )
:下列对这种元素的分析中正确的( )| A. | 最外层电子数为3 | |
| B. | 最高价氧化物对应水化物的分子式可能是H3RO4 | |
| C. | 最高价为+3价 | |
| D. | 此元素可能是24号元素铬(Cr)或25号元素锰(Mn) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com