
【题目】有下述有机反应类型①消去反应,②水解反应,③加聚反应,④加成反应,⑤还原反应,⑥氧化反应,以丙醛为原料制取 1,2-丙二醇,所需进行的反应类型依次是( )
A. ⑥④②①B. ⑤②④①C. ①③②⑤D. ⑤①④②
科目:高中化学 来源: 题型:
【题目】目前市场上有一种专门为婴幼儿设计的电解质饮料,适合在婴幼儿感冒、发烧时快速补充体内流失的电解质成分。下列物质可用作该饮料中的电解质的是
A.Fe B.葡萄糖 C.MgSO4 D.CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在氮族、氧族、卤素中NH3、H2O、HF出现沸点反常现象是由于( )
A. 分子间的结合力减小了
B. 键的极性很弱
C. 分子间产生了一种氢键的相互作用
D. 共用电子对强烈地偏向H原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图烧瓶内充满氯气,底部有层细沙(不参与反应),b处塞有小块钠。从a口用细铁丝把钠送下去,再从a口滴下一滴水,恰好滴在钠块上,立即剧烈反应,烧瓶内产生大量白色烟雾。不正确的说法是

A. 水可能参与二个氧化还原反应
B. Cl2可能参与四个氧化还原反应
C. 氧元素参与的反应一定是氧化还原反应
D. 氢元素参与的反应包含被氧化与被还原过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组在实验室中模拟上述过程。其设计的模拟装置如下:

根据要求填空:
(1)B装置有三种功能:①均匀混合气体;② ;③ 。
(2)设V(Cl2)/V(CH4)=x,若理论上欲获得最多的氯化氢,则x值应 。
(3)D装置的石棉中均匀混有KI粉末,其作用是 。
(4)E装置的作用是 (填编号)。
A.收集气体 B.吸收氯气
C.防止倒吸 D.吸收氯化氢
(5)E装置除生成盐酸外,还含有有机物,从E中分离出盐酸的最佳方法为 (填分离方法名称)。
(6)该装置还有缺陷,原因是没有进行尾气处理,其尾气主要成分为 (填编号)。
A.CH4B.CH3C1 C.CH2C12D.CHCl3E.CCl4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A. 钠和冷水反应Na+2H2O=Na++2OH-+H2↑
B. 金属铝溶于氢氧化钠溶液Al+2OH-=AlO2-+H2↑
C. 金属铝溶于盐酸中2Al+6H+=2Al3++3H2↑
D. 铁跟稀硫酸反应2Fe+6H+=2Fe3++3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列数据:
物质 | 熔点(℃) | 沸点(℃) | 密度(g·cm-3) |
乙醇 | -117.0 | 78.0 | 0.79 |
乙酸 | 16.6 | 117.9 | 1.05 |
乙酸乙酯 | -83.6 | 77.5 | 0.90 |
某学生在实验室制取乙酸乙酯的主要步骤如下:

①配制2 mL浓硫酸、3 mL乙醇(含18O)和2 mL乙酸的混合溶液。
②按上图连接好装置(装置气密性良好)并加入混合液,用小火均匀加热3 min~5 min。
③待试管乙收集到一定量产物后停止加热,撤出试管乙并用力振荡,然后静置待分层。
④分离出乙酸乙酯,洗涤、干燥。
(1)反应中浓硫酸的作用是______________________________________;
写出制取乙酸乙酯的化学方程式:_____________________________。
(2)上述实验中饱和碳酸钠溶液的作用是________(填字母)。
A.中和乙酸和乙醇 B.中和乙酸并吸收乙醇
C.减少乙酸乙酯的溶解 D.加速酯的生成,提高其产率
(3)步骤②中需要小火均匀加热,其主要理由是___________________;
步骤③所观察到的现象是_____________________________________;
欲将乙试管中的物质分离以得到乙酸乙酯,必须使用的仪器有________;分离时,乙酸乙酯应从仪器________(填“下口放”或“上口倒”)出。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含苯酚的工业废水的处理流程如图所示。

(1)①流程图设备Ⅰ中进行的是________操作(填写操作名称)。实验室里这一步操作可以用________(填仪器名称)进行。
②在设备Ⅲ中发生反应的化学方程式为________________________。
(2)为了防止水源污染,用简单而又现象明显的方法检验某工厂排放的污水中有无苯酚,此方法是_______________________________________。
(3)为测定废水中苯酚的含量,取此废水100 mL,向其中加入浓溴水至不再产生沉淀为止,得到沉淀0.331 g,此废水中苯酚的含量为______mg·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、下表是元素周期表的一部分,请回答有关问题:
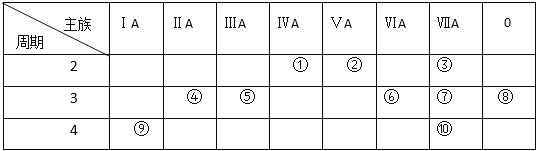
(1)表中能形成两性氢氧化物的元素是 _________ (用元素符号表示),写出该元素的单质与⑨最高价氧化物的水化物反应的化学方程式_____________________________。
(2)④元素与⑦元素形成的化合物的电子式 _____________________________。
(3)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是 ______。(填化学式)
Ⅱ、A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B同周期,C、D同主族,A的原子结构示意图为: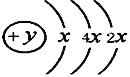 ,B、C可形成离子化合物B3C2,据此填空:
,B、C可形成离子化合物B3C2,据此填空:
(1)A元素在周期表中的位置_____________________________。
(2)A、B、C、D四种元素的原子,半径由小到大的顺序为_______________。
(3)B和C的最高价氧化物对应的水化物反应的离子方程式为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com