
 已知某种气态矿物燃料含有碳和氢两种元素.为了测定这种燃料中碳和氢两种元素的质量比,可将气态燃料放入足量的氧气中燃烧,并使产生的气体全部通入图所示的装置(气体流向如图),得到如下表所列的实验结果(假设产生的气体完全被吸收).
已知某种气态矿物燃料含有碳和氢两种元素.为了测定这种燃料中碳和氢两种元素的质量比,可将气态燃料放入足量的氧气中燃烧,并使产生的气体全部通入图所示的装置(气体流向如图),得到如下表所列的实验结果(假设产生的气体完全被吸收).| 装置的质量 | 实验前 | 实验后 |
| (固体+U形管A) | 101.1g | 102.9g |
| (固体+U形管B) | 312.0g | 314.2g |
| m |
| M |
| 2 |
| 18 |
| 12 |
| 44 |
| 3 |
| 12 |
| 1 |
| 1 |


科目:高中化学 来源: 题型:
 阿司匹林是常见的解热镇痛药,结构简式如图所示,有关阿司匹林的说法正确的是( )
阿司匹林是常见的解热镇痛药,结构简式如图所示,有关阿司匹林的说法正确的是( )| A、能发生取代、酯化反应,但不能发生氧化、还原反应 |
| B、阿司匹林分子中最多可以有13个原子在同一平面上 |
| C、1mol该物质完全氧化最多可消耗10mol氧气 |
| D、1mol该物质最多可与3mol NaOH发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
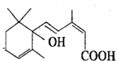 北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开.S-诱抗素的分子结构如图,回答:
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开.S-诱抗素的分子结构如图,回答:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:D>C>B>A |
| B、C与B只能形成一种化合物 |
| C、A、D、E的最高价氧化物对应水化物的酸性逐渐增强 |
| D、C和E的单质可通过电解饱和的CE水溶液获得 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲基橙呈黄色的溶液中:I-、Cl-、NO3-、Na+ |
| B、滴加无色酚酞后仍为无色的溶液:Na+、CO32-、K+、ClO-、SO42- |
| C、由水电离的c(OH-)=10-14mol?L-1 的溶液:NO3-、SO42-、Na+、K+ |
| D、含大量Al3+的溶液中:K+、HS-、NO3-、ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、饱和溶液一定是浓溶液 |
| B、冷却热饱和溶液一定有晶体析出 |
| C、溶液一定是均一、稳定的混合物 |
| D、同种溶质的饱和溶液一定比不饱和溶液浓度大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com