
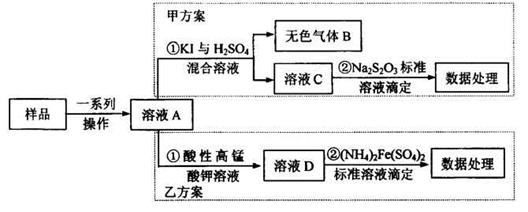
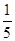 ×0.0010×0.01=2×10-6mol,乙方案中消耗的高锰酸钾为0.012L×0.0005mol/L-2×10-6mol=4×10-6mol;n(NaNO2)=
×0.0010×0.01=2×10-6mol,乙方案中消耗的高锰酸钾为0.012L×0.0005mol/L-2×10-6mol=4×10-6mol;n(NaNO2)=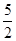 ×4×10-6mol=10-5mol,故每kg中含有690/amg。
×4×10-6mol=10-5mol,故每kg中含有690/amg。

 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源:不详 题型:单选题
| A.不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 |
| B.不慎将浓碱溶液沾到皮肤上,要立即用大量的水冲洗,然后涂上硼酸溶液 |
| C.金属钠着火,应立即用沙子灭火 |
| D.配制浓硫酸时,可先在量筒中加一定体积的水,再在搅拌下慢慢加入浓硫酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
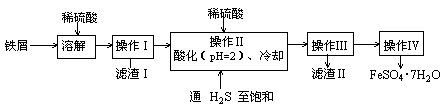
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
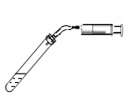 | 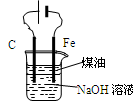 | 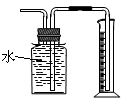 | 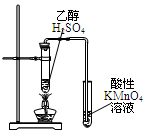 |
| A.测定生成CO2的化学反应速率 | B.制得Fe(OH)2并能保存较长时间不变质 | C.测量Cu与浓硝酸反应产生气体的体积 | D.证明CH3CH2OH发生消去反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.存放新制氯水时,使用带玻璃塞的棕色玻璃瓶 |
| B.配制一定物质的量浓度的溶液时,若开始容量瓶中有少量蒸馏水,对浓度无影响 |
| C.酸碱中和滴定实验中用到的玻璃仪器仅有酸式滴定管、碱式滴定管和烧杯 |
| D.进行蒸发操作时,不能使混合物中的水分完全蒸干 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.利用图①装置做喷泉实验 |
| B.利用图②装置吸收尾气SO2 |
| C.利用图③装置进行胶体电泳实验可以说明Fe(OH)3胶体带正电荷 |
| D.利用图④装置用MnO2和浓盐酸制备并收集Cl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com