
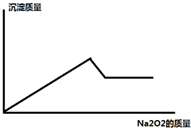
 ij��Һ�У����ܺ���Al3+��Fe3+��K+��Mg2+��Fe2+��Cu2+�е�һ�ֻ��֣��ּ����������ֻ������ɫ��ζ������ ��ͬʱ������ɫ����������������Ƶ����������������֮��Ĺ�ϵ��ͼ
ij��Һ�У����ܺ���Al3+��Fe3+��K+��Mg2+��Fe2+��Cu2+�е�һ�ֻ��֣��ּ����������ֻ������ɫ��ζ������ ��ͬʱ������ɫ����������������Ƶ����������������֮��Ĺ�ϵ��ͼ���� ����Na2O2��ĩ������������ˮ��Ӧ��2Na2O2+2H2O=4NaOH+O2������ͬʱ������ɫ�������ʿ��ƶϲ�����Fe3+��Fe2+��Cu2+��
����������Ĺ�������ʱ�������ɰ�ɫ����������������ܽ⣬�ƶ�һ����Mg2+��Al3+�����ܺ���K+�����������ӣ�������ɫ��Ӧ���Դ˽����⣮
K+�ļ��飺�ýྻ�IJ�˿պȡ����Һ���ھƾ��������գ�����ɫ�ܲ����۲�������ɫ���������ɫ��˵������K+��
��� �⣺����Na2O2��ĩ������������ˮ��Ӧ��2Na2O2+2H2O=4NaOH+O2������ͬʱ������ɫ�������ʿ��ƶϲ�����Fe3+��Fe2+��Cu2+��
����������Ĺ�������ʱ�������ɰ�ɫ����������������ܽ⣬�ƶ�һ����Mg2+��Al3+�����ܺ���K+�����������ӣ�������ɫ��Ӧ����
��1��ԭ��Һ��һ������Mg2+��Al3+���ʴ�Ϊ��Mg2+��Al3+��
��2�������Ϸ�����֪���ܺ���K+���ʴ�Ϊ��K+��
��3����õ���ɫ��������һ��û��Fe3+��Fe2+��Cu2+���ʴ�Ϊ��Fe3+��Fe2+��Cu2+��
��4����Ҫ��������ӣ�������ɫ��Ӧ���𣬲�������Ϊ�ྻ�IJ�˿պȡ����Һ���ھƾ��������գ�����ɫ�ܲ����۲�������ɫ���������ɫ��˵������K+��
�ʴ�Ϊ���ýྻ�IJ�˿պȡ����Һ���ھƾ��������գ�����ɫ�ܲ����۲�������ɫ���������ɫ��˵������K+��
���� ���⿼���˳������ӵļ��鷽������Ŀ�Ѷ��еȣ���ȷ�������ӵ�����Ϊ���ؼ���ע���������ճ������ӵļ��鷽���������ֿ�����ѧ���ķ������������Ӧ��������


 ��������ϵ�д�
��������ϵ�д� ����˼ά����ѵ����ʱ��ѧ��ϵ�д�
����˼ά����ѵ����ʱ��ѧ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
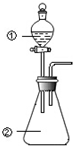 ��ͼ��ʾװ�ý�������ʵ�飺��������Һ������У�Ԥ���������ʵ��������� ��������
��ͼ��ʾװ�ý�������ʵ�飺��������Һ������У�Ԥ���������ʵ��������� ��������| ѡ�� | �������� | �������� | Ԥ����е����� |
| A | ϡ���� | ����������Һ | ���������� |
| B | Ũ���� | ��ɰֽ��ĥ�������� | ��������ɫ���� |
| C | �Ȼ�����Һ | Ũ����������Һ | ��������������ɫ���� |
| D | ������Һ | �������������Һ | ��Һ����ɫ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������������������������κ��ᷴӦ | |
| B�� | ��ΪCO2ͨ��ˮ�����п��Ƶù��ᣬ˵��̼������Աȹ�������ǿ | |
| C�� | SiO2��������ά�IJ��ϣ�SiO2�����У�ÿ����ԭ����������ԭ������ | |
| D�� | ��ҵ���Ʋ�������Ҫԭ���У������ʯ��ʯ��ʯӢ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
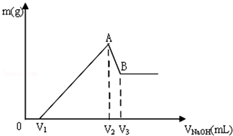 ��Mg��Al��ɵĻ���ﹲ0.1mol����100mL 3mol/LHCl��Һ�У��ٵμ�1mol/LNaOH ��Һ���ڵμ�NaOH��Һ�Ĺ����У�����������m��NaOH��Һ���V�ı仯��ͼ��ʾ��
��Mg��Al��ɵĻ���ﹲ0.1mol����100mL 3mol/LHCl��Һ�У��ٵμ�1mol/LNaOH ��Һ���ڵμ�NaOH��Һ�Ĺ����У�����������m��NaOH��Һ���V�ı仯��ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2S?2H++S2- | B�� | NaHCO3�TNa++H++CO32- | ||
| C�� | NaCl�TNa++Cl- | D�� | CH3COOH�TCH3COO-+H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ڢ� | C�� | �ڢ� | D�� | �ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���� | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pHֵ | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
| A�� | CO2+H2O+NaClO�TNaHCO3+HClO | B�� | CO2+H2O+2NaClO�TNa2CO3+2HClO | ||
| C�� | CH3COOH+NaCN�TCH3COONa+HCN | D�� | CH3COOH+NaClO�TCH3COONa+HClO |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com