
【题目】下列化学方程式或离子方程式正确的是( )
A.苯酚钠溶液中通入少量CO2:2C6H5O﹣+CO2+H2O→2C6H5OH+CO32﹣
B.甲醛溶液中加入足量的银氨溶液并加热:HCHO+2[Ag(NH3)2]++2OH﹣ ![]() HCOO﹣+NH4++2Ag↓+3NH3+H2O
HCOO﹣+NH4++2Ag↓+3NH3+H2O
C.1一氯丙烷中加入氢氧化钠溶液并加热:CH3CH2CH2Cl+NaOH ![]() CH3CH=CH2↑+NaCl+H2O
CH3CH=CH2↑+NaCl+H2O
D.向小苏打溶液中加入醋酸:HCO3﹣+CH3COOH═CO2↑+H2O+CH3COO﹣
【答案】D
【解析】解:A.苯酚钠溶液中通入少量CO2,二者反应生成苯酚和碳酸氢钠,正确的离子方程式为:C6H5O﹣+CO2+H2O→C6H5OH+HCO3﹣,故A错误;
B.甲醛溶液中加入足量的银氨溶液并加热的离子反应为HCHO+4[Ag(NH3)2]++4OH﹣ ![]() CO32﹣+2NH4++4Ag↓+6NH3+2H2O,故B错误;
CO32﹣+2NH4++4Ag↓+6NH3+2H2O,故B错误;
C.1一氯丙烷中加入氢氧化钠溶液并加热,二者发生水解反应,正确的离子方程式为:CH3CH2CH2Cl+NaOH ![]() CH3CH2CH2OH+NaCl,故C错误;
CH3CH2CH2OH+NaCl,故C错误;
D.向小苏打溶液中加入醋酸,反应的离子反应为:HCO3﹣+CH3COOH═CO2↑+H2O+CH3COO﹣,故D正确;
故选D.


科目:高中化学 来源: 题型:
【题目】A、B、C三种常见物质中均含有同一种元素,它们之间有如图所示的转化关系(部分反应物质已略去)。下列说法不正确的是

A. 若A是一种两性氧化物,则B的水溶液可呈酸性,C的水溶液可呈碱性
B. 若A为一种金属单质时,则反应①、②、③均可为化合反应,反应④可为置换反应
C. 若A、B、C是三种不同类别的固态物质,则B可以是工业上制取A、C的原料
D. 若A、B均是可燃性物质,完全燃烧都生成气体C,常温下A溶液pH<7,则将C通入A溶液中,pH值先减小后增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.2,2﹣二甲基﹣1﹣丁醇与2﹣甲基﹣2﹣丁醇互为同分异构体
B.![]() 的核磁共振氢谱有5个峰
的核磁共振氢谱有5个峰
C.根据核磁共振氢谱能鉴别1﹣溴丙烷和2﹣溴丙烷
D.用KMnO4酸性溶液能鉴别CH3CH═CHCH2OH和CH3CH2CH2CHO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、D、E、F、G是原子序数依次增大的六种短周期元素。A和B能形成B2A和B2A2两种化合物,B、D、G的最高价氧化物对应水化物两两之间都能反应,D、F、G原子最外层电子数之和等于15。回答下列问题:
(1)E元素在元素周期表中的位置是___________;A离子的结构示意图为____________。
(2)D的单质与B的最高价氧化物对应水化物的溶液反应,其离子方程式为________。
(3)①B2A2中含有___________键和___________键。
②该物质与水反应的化学反应方程式为___________________。
(4)下列说法正确的是____________(填字母序号)。
①B、D、E原子半径依次减小
②六种元素的最高正化合价均等于其原子的最外层电子数
③D的最高价氧化物对应水化物可以溶于氨水
④元素气态氢化物的稳定性:F>A>G
(5)在E、F、G的最高价氧化物对应水化物中,酸性最强的为__________(填化学式),用原子结构解释原因:同周期元素电子层数相同,从左至右,__________,得电子能力逐渐增强,元素非金属性逐渐增强。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在2L恒容密闭容器中,发生反应2NO(g)+O2(g)2NO2(g).
①某温度时,按物质的量比2:1充入NO和O2开始反应,n(NO)随时间变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.007 | 0.006 | 0.006 | 0.006 |
0~4s内以O2浓度变化表示的反应速率为________.
②能说明该反应已达到平衡状态的是________.
A.气体颜色保持不变 B.气体平均相对分子质量保持不变
C.υ正(NO)=2υ正(O2) D.气体压强保持不变
③已知:K300℃>K400℃.下列措施能使该反应的反应速率增大且平衡向正反应方向移动的是_______.
A、升高温度 B、充入Ar使压强增大
C、选择高效催化剂 D、充入NO使压强增大
(2)甲烷燃料电池可以提升能量利用率.如图是利用甲烷燃料电池电解100ml 1mol/L食盐水,电解一段时间后,收集到标准状况下的氢气2.24L(设电解后溶液体积不变).
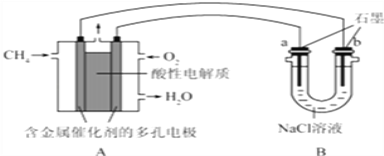
①甲烷燃料电池的负极反应式:____________________________________________.
②电解后溶液的pH=________(忽略氯气与氢氧化钠溶液反应).
(3)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示.请认真观察如图,然后回答问题:

①下列3个反应中符合示意图描述的反应的是 ___________(填代号).
A、铝粉与Fe2O3反应 B、用水稀释浓硫酸溶液 C、灼热的碳与CO2反应
②以甲烷为原料制取氢气是工业上常用的制氢方法.已知:
CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+306kJ/mol
CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=+240kJ/mol
CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为_______________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有着“植物大熊猫”和世界上最长寿树种美称、在地球上已有250万年历史的红豆杉,入选2010年世博会中国馆珍稀植物展出品种。其体内含量最多的化学元素和最基本的化学元素分别是( )
A. C和O B. C和H C. O和C D. H和O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表列出了 a~m 13种元素在周期表(已省略了过渡元素)中的位置:
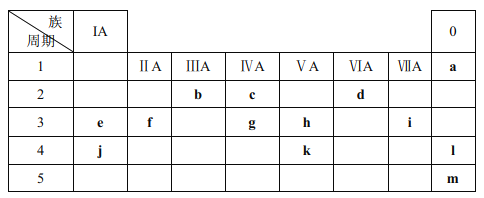
(1)元素 b为______(填名称);画出 g 的原子结构示意图______。
(2)元素 f、i、j 的原子半径从大到小的顺序是______ (用元素符号表示);这三种原子分别形成简单离子后,离子半径从大到小的顺序是______ (用离子符号表示)。
(3) h 和 k 的原子序数相差______ (填数字)。
(4)元素d和e形成的一种化合物为淡黄色固体,该化合物的电子式为_____________,该化合物中化学键有______,该化合物与c的最高价氧化物反应的化学方程式为________________________ 。
(5)人们曾认为, a、l、m 的单质不发生化学反应, 曾把它们叫做“惰性气体”。 但后来发现这族气体有的可参加化学反应,a、l、m中最有可能首先被发现可以形成化合物的元素是__________(写元素符号)。
(6)用高能射线照射含有 10 电子的 d 元素氢化物分子时,一个分子能释放出一个电子,同时产生一种具有较强氧化性的阳离子,试写出该阳离子的电子式:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:1,3﹣丁二烯的一类二烯烃能发生与具有双键的化合物进行1,4﹣加成反应,生成环状化合物,这类反应称为双烯合成,例如:
在下列横线上写出适当的反应物或生成物的结构简式,完成下列反应的化学方程式:
(1)![]() →
→
(2)+→ ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素是构成我们生活的世界中一切物质的“原材料”。
(1)自18世纪以来,科学家们不断探索元素之谜。通过从局部到系统的研究过程,逐渐发现了元素之间的内在联系。下面列出了几位杰出科学家的研究工作。
序号 | ① | ② | ③ | ④ |
科学 | 纽兰兹 | 道尔顿 | 德贝莱纳 | 尚古尔多 |
工作 | 发现“八音律”,指出从某一指定的元素起,第八个元素是第一个元素的某种重复 | 创立近代原子论,率先开始相对原子质量的测定工作 | 发现了5组性质相似的“三元素组”,中间元素的相对原子质量为前后两种元素相对原子质量的算术平均值 | 认为各元素组之间并非毫不相关,可以用相对原子质量把它们按从小到大的顺序串联 |
上述科学家的研究按照时间先后排序合理的是_________(填数字序号)。
(2)1869年,门捷列夫在前人研究的基础上制出了第一张元素周期表,如图所示。
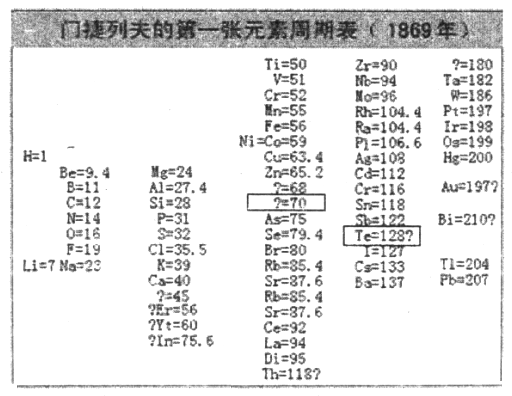
①门捷列夫将已有元素按照相对原子质量排序,同一___________(填“横行”或“纵列”)元素性质相似。结合表中信息,猜想第4列方框中“?=70”的问号表达的含义是_______________,第5列方框中“Te=128?”的问号表达的含义是_______________。
②到20世纪初,门捷列夫周期表中为未知元素留下的空位逐渐被填满。而且,随着原子结构的逐渐揭秘,科学家们发现了元素性质不是随着相对原子质量递增呈现周期性变化,而是随着原子序数(核电荷数)递增呈现周期性变化。其本质原因是_______________(填字母序号)。
A. 随着核电荷数递增,原子核外电子排布呈现周期性变化
B. 随着核电荷数递增,原子半径呈现周期性变化
C. 随着核电荷数递增,元素主要化合价呈现周期性变化
(3)短周期元素A、B、D、E、G、J在周期表中的位置如下:
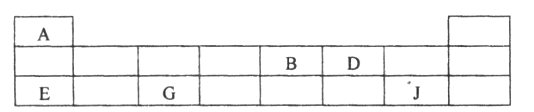
根据上表回答问题:
①D在周期表中的位置是_______________。
②A、B、E、G的原子半径由大到小的顺序是_______________(填元素符号)。
③B、D的气态氢化物的稳定性大小关系为_______________(填化学式)。
④E、G、J的最高价氧化物对应水化物两两之间反应的离子方程式分别为i. H++OH-=H2O、ii. _______________、iii_______________。
⑤用电子式表示E的最高价氧化物的形成过程_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com