
��ҵ���Ʊ�H2��һ����Ҫ�����ǣ�
CO(g) + H2O(g)  CO2 (g) + H2(g) ��H��Q kJ/mol
CO2 (g) + H2(g) ��H��Q kJ/mol
��֪
�÷�Ӧ��ƽ�ⳣ��K���¶�T�Ĺ�ϵ����ͼ��ʾ������һ�̶����ܱ������У�
850�� ʱ����������Ӧ����������ڸ����ʵ�Ũ�� (mol/L)��ʱ��ı仯
��ϵ���±���

��֪��850�� ʱ�÷�Ӧ�Ļ�ѧƽ�ⳣ��K = 1.0 ����ش��������⣺
(1) Q 0��� �� ������ �� ������ ����
(2)����850��ʱ��Ӧ�����г���H2O(g),K ֵ (������С�����䣩
(3)�ϱ��� c2Ϊ mol/L , CO(g)��ת����Ϊ (������λ��Ч����)
 ���Ͱ�ͨ��ĩ���ϵ�д�
���Ͱ�ͨ��ĩ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ᡢ�Ҵ���Ũ���������У�����H218O����һ��ʱ���18O�����ڣ� ��
A��ֻ��������������� B����������������������з�����
C��ֻ�������Ҵ������� D��������ˮ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ʹ1mol��ϩ�����������ӳɷ�Ӧ��Ȼ��ʹ�üӳɷ�Ӧ�IJ����������ڹ��յ�����
�½���ȡ���������������ȫ��Ӧ�������������������ĵ������������ʵ����ǣ� ��
A��6mol B��5mol C��4mol D��3mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ʵ�顱���м��ס����㡢��Լ����ɫ���ŵ㣬�۲������ĸ�
�����ʵ�顱���г�װ��δ���������ж�����˵����ȷ���ǣ�����
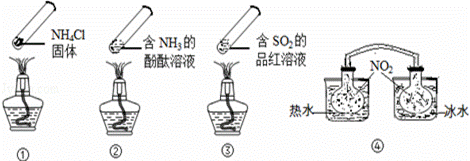
A.����ʱ�����ϲ��㼯�˹���NH4Cl��˵��NH4Cl�����ȶ��ԱȽϺ�
B.����ʱ���ڡ�����Һ����죬��ȴ���ֶ���Ϊ��ɫ
C.����,��������ˮ�е�������������ɫ����,�����ڱ�ˮ�е�������
������ɫ��dz
D.�ĸ������ʵ�顱���������Ļ�ѧ��Ӧ���ǿ��淴Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ж�ʵ���������������������
A����FeCl3��KSCN�����Һ�м�������KCl���壬��ҺѪ��ɫ��dz
B.��5mL0.1mol/LK2Cr2O7��Һ�м�������NaOH����,��Һ�ɳ�ɫ��Ϊ��ɫ
C.�������Ũ��Na2S2O3��H2SO4���,�¶����߳��ֻ��Ǻ����������ٶȼӿ�
D������KMnO4��Һ�еμ�H2C2O4��H2C2O4Ũ��Խ����ɫ�����������ٶ�Խ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵���У���ȷ���ǣ��� ��
A��1 Lˮ���ܽ���40 g NaOH��������ҺŨ��Ϊ1 mol/L
B����1 L 2 mol/L��NaCl��Һ��ȡ��0.5 L������Һ��Ũ��Ϊ1 mol/L
C������״���µ�HCl����2.24 Lͨ��ˮ���Ƴ�100 mL��Һ��������Һ�����ʵ���Ũ��Ϊ1 mol/L
D������1 L 0.2 mol/L��CuSO4��Һ������25 g����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij500mL��Һ�к�0.1 mol Fe2+��0.2molFe3+������0.2mol���ۣ���Fe3+ ��ȫ��ԭ����Һ��Fe2+�����ʵ���Ũ��Ϊ(���跴Ӧǰ���������) ���� ��
����ʾ��2 Fe3+ + Fe ��3 Fe2+ ��
A��0.4 mol/L B��0.6 mol/L C��0.8 mol/L D�� l.0 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
300 mLijŨ�ȵ�NaOH��Һ�к���60 g���ʡ���������1 mol��L�D1��NaOH��Һ��Ӧȡԭ��Һ������ˮ�������ԼΪ���� ��
����A��1��4������ B��1��5������ C��2��1������ D��2��3����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����й�Ħ��������������Ӧ���У�����ȷ����
A��1 mol NH ������Ϊ18 g B��SO2��Ħ������Ϊ64 g��mol��1
������Ϊ18 g B��SO2��Ħ������Ϊ64 g��mol��1
C����ԭ�ӵ�Ħ�����������������ԭ������ D��һ��ˮ���ӵ�����Լ����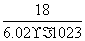 g
g
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com