
碳酸钠(Na2CO3)俗称纯碱,是一种重要的基础化工原料,广泛应用于玻璃、造纸等工业。下列与碳酸钠有关的说法正确的是:
| A.Na2CO3的稳定性介于Na2CO3·10H2O和NaHCO3之间 |
| B.“侯氏制碱法”制得的碱是指NaHCO3 |
| C.可用盐酸鉴别Na2CO3和NaHCO3固体 |
| D.纯碱有时可代替烧碱使用,比如溶解石英、促进乙酸乙酯的水解等 |
C
解析试题分析:A Na2CO3·10H2O加热失去结晶水。NaHCO3之受热分解:2NaHCO3=Na2CO3+CO2↑+H2O。所以Na2CO3的稳定性最强。错误。B“侯氏制碱法”制得的碱是指Na2CO3,错误。C盐酸和Na2CO3 . 首先反应产生NaHCO3和氯化钠,然后是第一步产生的NaHCO3和盐酸继续反应产生氯化钠、二氧化碳、水。而NaHCO3和盐酸直接反应放出二氧化碳气体。二者现象不同,故可用盐酸鉴别Na2CO3和NaHCO3固体。正确。D.在常温下纯碱与石英不反应,而氢氧化钠与石英能发生反应,故常温下不能用来溶解石英;乙酸乙酯在碳酸钠溶液的的溶解度很小,不能促进其水解等。故这时不能用纯碱有时可代替烧碱使用。错误。
考点:考查侯氏制碱法及Na2CO3和NaHCO3的性质、用途等的知识。


科目:高中化学 来源: 题型:单选题
120 mL含有0.20 mol碳酸钠溶液和200 mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是
| A.2.0mol/L | B.1.5 mol/L | C.0.18 mol/L | D.0.24mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述正确的是
| A.将FeCl3溶液加热蒸干得到FeCl3固体 |
| B.向Fe(NO3)2溶液中加少量盐酸,无明显现象 |
| C.向氢氧化镁悬浊液中滴加FeCl3溶液,无明显现象 |
| D.向FeSO4溶液中滴加NaOH溶液,先出现白色沉淀,最终沉淀转化成红褐色 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
一些不法商人在面粉生产中添加过氧化钙(CaO2)等添加剂对食品进行增白。下列关于过氧化钙(CaO2)的叙述正确的是
| A.CaO2中阴、阳离子的个数比为1:1 |
| B.CaO2对面粉增白原理与SO2漂白原理相似 |
| C.CaO2和水反应时,每产生1 molO2转移电子4 mol |
| D.CaO2放入NaHCO3溶液中,会放出二氧化碳,并产生白色浑浊 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
4.6g钠投入100g水中,下列叙述错误的是
| A.钠浮在水面,熔化成银色光亮的小球 | B.钠贮存在煤油中 |
| C.所得溶液的质量分数为4.4﹪ | D.该反应中转移0.2mole- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列实验方案中,不能测定Na2CO3和NaHCO3,混合物中Na2CO3质量分数的是
| A.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克 |
| B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体 |
| C.取a克混合物充分加热,得b克固体 |
| D.取a克混合物与足量Ca(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
Al、Cu都是重要的金属元素。下列说法正确的是
| A.两者对应的氧化物均为碱性氧化物 |
| B.两者的单质都能与稀硫酸反应产生氢气 |
| C.常温条件下,两种金属都能溶解于浓硝酸中 |
| D.用惰性电极电解AlCl3、CuCl2的水溶液均可得到氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
工业上用含有铝、铁、铜的废弃合金为主要原料制取硫酸铝溶液、硝酸铜晶体和无水氯化铁,其生产流程如下图所示。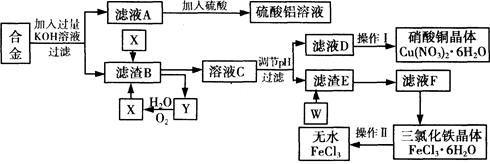
已知:调节适当PH范围可使Fe3+沉淀完全而Cu2+不会沉淀。
请回答下列问题:
(1)写出向合金中加入KOH溶液后所发生反应的离子方程式: 。
(2)在滤液A中直接加入硫酸后所得到的硫酸铝溶液中除含少量硫酸外,还一定含有的杂质是
(填化学式)。
请设计一个更合理的实验方案由滤液A制备纯净的硫酸铝溶液,仿照上图形式画出制备流程图(提示:在箭头上下方标出所用试剂和实验操作) 。
(3) 写出试剂X的名称 。
(4) 实验操作I的顺序依次为 (选填序号)。
| A.蒸馏 | B.蒸发浓缩 | C.过滤 | D.冷却结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(14分)下列框图中的字母分别代表一种常见的物质或其溶液,相互之间的转化关系如下图所示(部分产物及反应条件已略去)。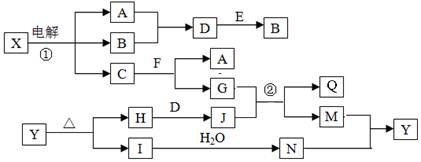
已知A、B为气态单质,F是地壳中含量最多的金属元素的单质:E、H、I为氧化物,E为黑色固体,H为红棕色粉末,I为红棕色气体;M为红褐色沉淀,Q为白色胶状物质。
请回答下列问题:
(1)组成单质F的元素在周期表中的位置是______;C中存在的化学键类型为____;E的化学式是___。
(2)A在B中燃烧的现象是_______ 。
(3) D+E→B的反应中,被氧化与被还原的物质的物质的量之比是_______。
(4)反应①的化学方程式为___________________________________ 。
(5)反应②的离子方程式为___________________________________。
(6)Y受热分解可生成H、I和氧气,.写出该反应的化学方程式:______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com