
ЁОЬтФПЁПЛ№ЗЈСЖЙЏЪЧдкВЛЬЋИпЕФЮТЖШЯТЃЈ450ЁЋ800ЁцЃЉЃЌНЋЙЏПѓЪЏЛђОЋПѓНјааБКЩеЃЌжБНгНЋЙЏЛЙдГЪЦјЬЌЗжРыГіРДЃЌЖјКѓРфФ§ГЩвКЬЌЙЏЃЎФПЧАЙЄвЕЩЯжЦДжЙЏЕФСїГЬШчЭМЃК

ЯТСагаЙиЫЕЗЈе§ШЗЕФЪЧЃЈ ЃЉ
A. СїГЬжаМгШыбѕЛЏИЦЕФФПЕФЪЧМѕЩйSO2ЕФХХЗХ
B. ЁАГНЩАЁБМгШШЪБЗЂЩњЗДгІЃКHgS+O2 ![]() Hg+SO2ЃЌИУЗНЗЈЪєгкШШЗжНтЗЈ
Hg+SO2ЃЌИУЗНЗЈЪєгкШШЗжНтЗЈ
C. ЯДЕгДжЙЏЪБПЩгУ5%ЕФбЮЫсДњЬц5%ЕФЯѕЫс
D. КЌЙЏбЬЦјжаЙЏЕФКЌСПКмЕЭЃЌПЩвджБНгХХЗХ
ЁОД№АИЁПA
ЁОНтЮіЁПЪдЬтЗжЮіЃКAЃЎЁАГНЩАЁБМгШШЪБЗЂЩњЗДгІЃКHgS+O2![]() Hg+SO2ЃЌгаЮлШОЦјЬхSO2ВњЩњЃЌвђДЫМгШыбѕЛЏИЦПЩМѕЩйSO2ЕФХХЗХЃЌЙЪAе§ШЗЃЛBЃЎИУЗДгІВЛЪєгкЗжНтЗДгІЃЌЙЪBДэЮѓЃЛCЃЎДжЙЏжаЕФЭЧІдгжЪВЛШмгкЯЁбЮЫсЃЌдђВЛФмгУ5%ЕФбЮЫсДњЬц5%ЕФЯѕЫсЃЌЙЪCДэЮѓЃЛDЃЎЙЏеєЦћгаЖОЃЌБиаыНјааДІРэВХФмХХЗХЃЌЙЪDДэЮѓЁЃЙЪбЁAЁЃ
Hg+SO2ЃЌгаЮлШОЦјЬхSO2ВњЩњЃЌвђДЫМгШыбѕЛЏИЦПЩМѕЩйSO2ЕФХХЗХЃЌЙЪAе§ШЗЃЛBЃЎИУЗДгІВЛЪєгкЗжНтЗДгІЃЌЙЪBДэЮѓЃЛCЃЎДжЙЏжаЕФЭЧІдгжЪВЛШмгкЯЁбЮЫсЃЌдђВЛФмгУ5%ЕФбЮЫсДњЬц5%ЕФЯѕЫсЃЌЙЪCДэЮѓЃЛDЃЎЙЏеєЦћгаЖОЃЌБиаыНјааДІРэВХФмХХЗХЃЌЙЪDДэЮѓЁЃЙЪбЁAЁЃ


 ХргХШ§КУЩњЯЕСаД№АИ
ХргХШ§КУЩњЯЕСаД№АИ гХЛЏзївЕЩЯКЃПЦММЮФЯзГіАцЩчЯЕСаД№АИ
гХЛЏзївЕЩЯКЃПЦММЮФЯзГіАцЩчЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгУКЌгаAl2O3ЁЂSiO2КЭЩйСПFeOЁЄxFe2O3ЕФТСЛвжЦБИAl2ЃЈSO4ЃЉ3ЁЄ18H2OЃЌЙЄвеСїГЬШчЯТЃЈВПЗжВйзїКЭЬѕМўТдЃЉЃК
Ђё. ЯђТСЛвжаМгШыЙ§СПЯЁH2SO4ЃЌЙ§ТЫЃЛ
Ђђ. ЯђТЫвКжаМгШыЙ§СПKMnO4ШмвКЃЌЕїНкШмвКЕФpHдМЮЊ3ЃЛ
Ђѓ. МгШШЃЌВњЩњДѓСПзиЩЋГСЕэЃЌОВжУЃЌЩЯВуШмвКГЪзЯКьЩЋЃЛ
Ђє. МгШыMnSO4жСзЯКьЩЋЯћЪЇЃЌЙ§ТЫЃЛ
Ђѕ. МгШШХЈЫѕЁЂРфШДНсОЇЁЂЙ§ТЫЁЂЯДЕгЁЂИЩдяЃЌЕУЕНВњЦЗЁЃ
ЃЈ1ЃЉH2SO4ШмНтAl2O3ЕФРызгЗНГЬЪНЪЧ__________________ЁЃ
ЃЈ2ЃЉKMnO4бѕЛЏFe2ЃЋЕФРызгЗНГЬЪНВЙГфЭъећЃК_________________

ЃЈ3ЃЉвбжЊЃКЩњГЩЧтбѕЛЏЮяГСЕэЕФpH
AlЃЈOHЃЉ3 | FeЃЈOHЃЉ2 | FeЃЈOHЃЉ3 | |
ПЊЪМГСЕэЪБ | 3.4 | 6.3 | 1.5 |
ЭъШЋГСЕэЪБ | 4.7 | 8.3 | 2.8 |
зЂЃКН№ЪєРызгЕФЦ№ЪМХЈЖШЮЊ0.1molЁЄLЃ1
ИљОнБэжаЪ§ОнНтЪЭВНжшЂђЕФФПЕФ_______________ЃЛ
ЃЈ4ЃЉвбжЊЃКвЛЖЈЬѕМўЯТЃЌMnO4ЃПЩгыMn2ЃЋЗДгІЩњГЩMnO2ЃЌ
ЂйЯђЂѓЕФГСЕэжаМгШыХЈHClВЂМгШШЃЌФмЫЕУїГСЕэжаДцдкMnO2ЕФЯжЯѓЪЧ____________ЁЃ
ЂкЂєжаМгШыMnSO4ЕФФПЕФЪЧ_____________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЩњЮяЬхЩњУќЛюЖЏЕФжївЊГаЕЃепЁЂвХДЋаХЯЂЕФаЏДјепЁЂНсЙЙКЭЙІФмЕФЛљБОЕЅЮЛЁЂЩњУќЛюЖЏЕФжївЊФмдДЮяжЪвРДЮЪЧ ЃЈ ЃЉ
AЃЎКЫЫсЁЂЕААзжЪЁЂЯИАћЁЂЬЧРр BЃЎЕААзжЪЁЂКЫЫсЁЂЯИАћЁЂжЌЗО
CЃЎЕААзжЪЁЂКЫЫсЁЂЯИАћЁЂЬЧРр DЃЎКЫЫсЁЂЕААзжЪЁЂЬЧРрЁЂЯИАћ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈЁЁЁЁЃЉ
A.![]() ЕФвЛфхДњЮяКЭ
ЕФвЛфхДњЮяКЭ ![]() ЕФвЛфхДњЮяЖМга4жжЃЈВЛПМТЧСЂЬхвьЙЙЃЉ
ЕФвЛфхДњЮяЖМга4жжЃЈВЛПМТЧСЂЬхвьЙЙЃЉ
B.C5H11Clга3жжЭЌЗжвьЙЙЬх
C.АДЯЕЭГУќУћЗЈЃЌЛЏКЯЮя  ЕФУћГЦЪЧ2ЃЌ3ЃЌ4ЉШ§МзЛљЉ2ЉввЛљЮьЭщ
ЕФУћГЦЪЧ2ЃЌ3ЃЌ4ЉШ§МзЛљЉ2ЉввЛљЮьЭщ
D.CH3CHЈTCHCH3ЗжзгжаЕФЫФИіЬМдзгдкЭЌвЛжБЯпЩЯ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЫФбѕЛЏШ§ЧІЃЈPb3O4ЃЌвВПЩаДзї2PbOЁЄPbO2ЃЉЫзУћЁАЧІЕЄЁБЛђЁАКьЕЄЁБЃЌПЩгУзїЗРатМСЁЃЙЄвЕЩЯвдЗЯОЩЧІЫсЕчГиЕФЧІИрЃЈжївЊГЩЗжЪЧPbSO4КЭPbO2ЃЉЮЊдСЯжЦБИPb3O4ЕФСїГЬШчЯТЃК
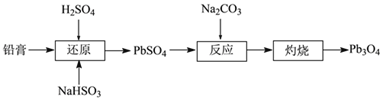
ЃЈ1ЃЉЁАЛЙдЁБЪБЕФЛЏбЇЗНГЬЪНЮЊ________ЁЃ
ЃЈ2ЃЉвбжЊЃКKsp[PbCO3]=1.5ЁС10Ѓ13ЁЃШєЪЙШмвКжаPb2+ЕФХЈЖШаЁгк1ЁС10Ѓ5 molL-1ЃЌДЫЪБШмвКжаЕФc(CO32Ѓ) > ________molL-1ЁЃ
ЃЈ3ЃЉЮЊВтЖЈФГбљЦЗЫФбѕЛЏШ§ЧІКЌСПЃЌГЦШЁбљЦЗ0.1200gЃЌМгШызуСПЕФ6 molLЃ1HNO3ГфЗжШмНтЃЌЙ§ТЫЃЌЕУЕНКЌPb2+ЕФТЫвККЭPbO2ЙЬЬхЁЃНЋЙЬЬхPbO2СЌЭЌТЫжНвЛВЂжУгкСэвЛжЛзЖаЮЦПжаЃЌМгШызуСПЕФДзЫсКЭДзЫсФЦЛьКЯШмвКЃЌдйМгШыЙ§СПKIЃЌЪЙPbO2ГфЗжбѕЛЏIЃЃЌвдЕэЗлШмвКзїжИЪОМСЃЌгУ0.01000molLЃ1 Na2S2O3ШмвКЕЮЖЈЃЌжеЕуЪБгУШЅ30.00 mLЁЃвбжЊЃКI2 + 2Na2S2O3 ЃН Na2S4O6 + 2NaIЁЃ
ЂйЫљМгKIБиаыЙ§СПЃЌдвђЪЧ________ЁЃ
ЂкМЦЫуЪдбљжаPb3O4ЕФжЪСПЗжЪ§_____ЁЃЃЈаДГіМЦЫуЙ§ГЬЃЉ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЮвЙњЛЏбЇМвНќФъРДКЯГЩЕФОлввШВбмЩњЮяЗжзгMЕФНсЙЙЪНМАMдкЯЁСђЫсзїгУЯТЕФЫЎНтЙ§ГЬШчЭМЃКЯТСагаЙиЫЕЗЈжаВЛе§ШЗЕФЪЧЃЈЁЁЁЁЃЉ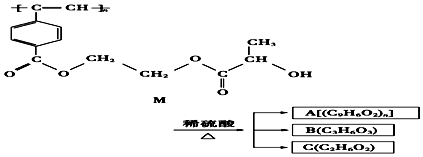
A.MгыAОљФмЪЙЫсадИпУЬЫсМиШмвККЭфхЫЎЭЪЩЋ
B.BжаКЌгаєШЛљКЭєЧЛљСНжжЙйФмЭХЃЌBФмЗЂЩњЯћШЅЗДгІКЭѕЅЛЏЗДгІ
C.1molMгыШШЕФЩеМюШмвКЗДгІЃЌПЩЯћКФ2nmolЕФNaOH
D.AЃЌBЃЌCИї1molЗжБ№гыН№ЪєФЦЗДгІЃЌЗХГіЦјЬхЕФЮяжЪЕФСПжЎБШЮЊ1ЃК2ЃК2
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЭМЪОгыЖдгІЕФа№ЪіЯрЗћЕФЪЧ
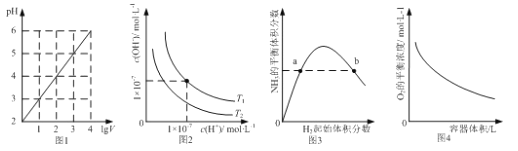
A. ЭМ1БэЪО1LpH=2ЕФCH3COOHШмвКМгЫЎЯЁЪЭжСVLЃЌpHЫц1gVЕФБфЛЏ
B. ЭМ2БэЪОВЛЭЌЮТЖШЯТЫЎШмвКжаH+КЭOH-ХЈЖШЕФБфЛЏЕФЧњЯпЃЌЭМжаЮТЖШT1 ЃМT2
C. ЭМ3БэЪОвЛЖЈЬѕМўЯТЕФКЯГЩАБЗДгІжаЃЌNH3ЕФЦНКтЬхЛ§ЗжЪ§ЫцH2Ц№ЪМЬхЛ§ЗжЪ§ЃЈN2ЕФЦ№ЪМСПКуЖЈЃЉЕФБфЛЏЃЌЭМжаaЕуN2ЕФзЊЛЏТЪаЁгкbЕу
D. ЭМ4БэЪОЭЌвЛЮТЖШЯТЃЌдкВЛЭЌШнЛ§ЕФШнЦїжаНјааЗДгІ2BaO2ЃЈsЃЉ2BaOЃЈsЃЉ+O2ЃЈgЃЉЃЌO2ЕФЦНКтХЈЖШгыШнЦїШнЛ§ЕФЙиЯЕ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаБфЛЏЪєгкЮќШШЗДгІЕФЪЧЃЈЁЁЁЁЃЉ
ЂйвКЬЌЫЎЦћЛЏ
ЂкНЋЕЈЗЏМгШШБфЮЊАзЩЋЗлФЉ
ЂлХЈСђЫсЯЁЪЭ
ЂмТШЫсМиЗжНтжЦбѕЦј
ЂнЩњЪЏЛвИњЫЎЗДгІЩњГЩЪьЪЏЛвЃЎ
A.ЂйЂмЂн
B.ЂйЂкЂм
C.ЂкЂл
D.ЂкЂм
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПМзДМЪЧвЛжжПЩдйЩњФмдДЃЌОпгаЙуЗКЕФПЊЗЂКЭгІгУЧАОАЃЎЙЄвЕЩЯвЛАуВЩгУЯТСаСНжжЗДгІКЯГЩМзДМЃЎ
ЗДгІЂёЃКCOЃЈgЃЉ+2H2ЃЈgЃЉCH3OHЃЈgЃЉЁїH1
ЗДгІЂђЃКCO2ЃЈgЃЉ+3H2ЃЈgЃЉCH3OHЃЈgЃЉ+H2OЃЈgЃЉЁїH2
ЯТБэЫљСаЪ§ОнЪЧЗДгІЂёдкВЛЭЌЮТЖШЯТЕФЛЏбЇЦНКтГЃЪ§ЃЈKЃЉЃК
ЮТЖШ | 250Ёц | 300Ёц | 350Ёц |
K | 2.0 | 0.27 | 0.012 |
ЃЈ1ЃЉдквЛЖЈЬѕМўЯТНЋ2mol COКЭ6mol H2ГфШы2LЕФУмБеШнЦїжаЗЂЩњЗДгІЂёЃЌ5minКѓВтЕУcЃЈCOЃЉ=0.4mol/LЃЌМЦЫуПЩЕУДЫЖЮЪБМфЕФЗДгІЫйТЪЃЈгУH2БэЪОЃЉЮЊmol/ЃЈLminЃЉЃЎ
ЃЈ2ЃЉгЩБэжаЪ§ОнХаЖЯЁїH10 ЃЈЬюЁАЃОЁБЁЂЁАЃМЁБЛђЁА=ЁБЃЉЃЛ
ЗДгІCO2ЃЈgЃЉ+H2ЃЈgЃЉCOЃЈgЃЉ+H2OЃЈgЃЉЁїH3= ЃЈгУЁїH1КЭЁїH2БэЪОЃЉЃЎ
ЃЈ3ЃЉШєШнЦїШнЛ§ВЛБфЃЌдђЯТСаДыЪЉПЩЬсИпЗДгІЂёжаCOзЊЛЏТЪЕФЪЧ ЃЈЬюзжФИађКХЃЉЃЎ
aЃЎГфШыCOЃЌЪЙЬхЯЕзмбЙЧПдіДѓ bЃЎНЋCH3OHЃЈgЃЉДгЬхЯЕжаЗжРы
cЃЎГфШыHeЃЌЪЙЬхЯЕзмбЙЧПдіДѓ dЃЎЪЙгУИпаЇДпЛЏМС
ЃЈ4ЃЉаДГіЗДгІЂђЕФЛЏбЇЦНКтГЃЪ§БэДяЪНЃКKЂђ=ЃЛБЃГжКуЮТКуШнЃЌНЋЗДгІЂђЕФЦНКтЬхЯЕжаИїЮяжЪХЈЖШОљдіДѓЮЊдРДЕФ2БЖЃЌдђЛЏбЇЦНКтвЦЖЏЃЈЬюЁАе§ЯђЁБЁЂЁАФцЯђЁБЛђЁАВЛЁБЃЉЃЌЦНКтГЃЪ§KЂђЃЈЬюЁАБфДѓЁБЁЂЁАБфаЁЁБЛђЁАВЛБфЁБЃЉЃЎ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com