
����Ŀ������һ�ֹ��ɽ���Ԫ�أ�ͨ�������Ͻ���ֵ����Ӽ�������Ԫ�ؿ���ǿ �Ͻ��ǿ�ȡ�Ӳ�ȡ��ɺ��Լ����ԣ�������ǿ�����¼���ʴ���ܡ���ͼ�ǻ��������� �Ʊ����������Ҫ����ͼ��
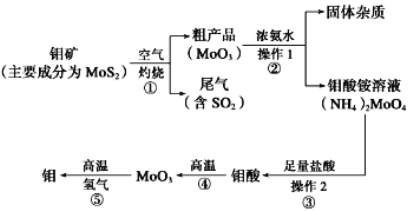
(1)д���ڸ����·�����Ӧ�ٵĻ�ѧ����_________________________________________
(2)��������������Ũ��ˮ���շ�Ӧ�ٵ�β���ϳɷ��ϣ�д���÷�Ӧ�����ӷ���ʽ��______________________________
(3)�����ʵ����ģ����� 1 �Ͳ��� 2������Ҫʹ�õ���Ҫ����������______________________________
(4)ijͬѧ������ͼ��ʾװ�����Ʊ�����������������ԭ�������⣬����Ҫ��ش����⣺
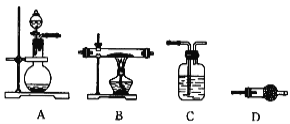
�� �����һ��ʵ�鷽����֤H2�Ļ�ԭ�Բ����������������װ������˳����______________________________
�� ����ƿ A �м�����������ͭ��Ŀ����_____
�� ����ʹ�� D װ�ã�������ʢ��ҩƷ������_____��_____
���𰸡�2MoS2 + 7O2![]() 2MoO3 + 4SO2 SO2 + 2NH3��H2O�� 2NH4+ + SO32��+ H2O �ձ���©���������� ACBDD ���γ�ԭ��أ��ӿ��������������� ��ˮ����ͭ ��ʯ��
2MoO3 + 4SO2 SO2 + 2NH3��H2O�� 2NH4+ + SO32��+ H2O �ձ���©���������� ACBDD ���γ�ԭ��أ��ӿ��������������� ��ˮ����ͭ ��ʯ��
��������
��������ͼ������Ҫ��Ӧ����Ҫ��������ɻ�ѧ����ʽ��ѡ����������������ʵ��Ŀ�ģ�������ʵ�飬����ֹ������Ӱ�졣
��1��������ͼ�ҳ���Ӧ�ٵķ�Ӧ���������û��ϼ���������ƽ����2MoS2 + 7O2![]() 2MoO3 + 4SO2��
2MoO3 + 4SO2��
��2��������Ũ��ˮ����SO2�������Σ����ӷ���ʽΪSO2 + 2NH3��H2O�� 2NH4+ + SO32��+ H2O��
��3������ڵù������Һ������1Ϊ���ˡ�����۸��ֽⷴӦ�ܽ��У�������������ˮ������2Ϊ���ˡ���Ҫʹ�õ���Ҫ�����������ձ���©������������
��4�����Ʊ�H2����ԭMoO3��֤���仹ԭ�ԣ�����ˮ����ͭ������������ˮ������������������ֹ������ˮ�����š���װ������˳����ACBDD��
������ƿA�м�����������ͭ��п�û���ͭ���Ӷ��γ�ԭ��أ��ӿ��������������ʣ�
�۵�һ��ʹ��Dװ�ã���ʢҩƷΪ��ˮ����ͭ�����ڼ�����������ˮ���ڶ���ʹ��Dװ�ã���ʢҩƷΪ��ʯ�ҵȣ���ֹ�����е�ˮ��ʹ��ˮ����ͭ������


 ��ѧʵ����ϵ�д�
��ѧʵ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������Է�������Ϊ86����������к���3����CH3��2����CH2����1��![]() ����ýṹ������һ��ȡ����(�����������칹)�� (���� )
����ýṹ������һ��ȡ����(�����������칹)�� (���� )
A. 9��B. 6��C. 5��D. 4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����꣬��ѧ���о����Ҵ����ϳ������������·�����2C2H5OH(g) ![]() CH3COOC2H5(g)+2H2(g)���ڳ�ѹ�·�Ӧ�������ռ�����ó�����Һ���ռ�������Ҫ���������������ͼ��ʾ�����ڸ÷����������Ʋⲻ��������
CH3COOC2H5(g)+2H2(g)���ڳ�ѹ�·�Ӧ�������ռ�����ó�����Һ���ռ�������Ҫ���������������ͼ��ʾ�����ڸ÷����������Ʋⲻ��������
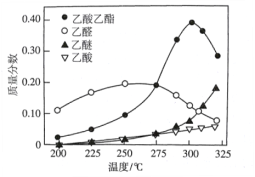
A. ��Ӧ�¶Ȳ��˳���300��
B. �÷�Ӧ������ȥ��Ӧ
C. �ڴ��������£���ȩ�Ƿ�Ӧ�����е��м����
D. ��ߴ����Ļ��Ժ�ѡ���ԣ��������ѡ���ϩ�ȸ������ǹ��յĹؼ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A����B2����C����D2��4�����Ӿ�����ͬ�ĵ��Ӳ�ṹ��������������˳��
��B2����A����C����D2����C����D2����A����B2����B2����A����D2����C����D2����C����A����B2��4�����ӵİ뾶�ɴ�С�Լ�4��Ԫ��ԭ�������ɴ�С��˳��ֱ���( )
A.�٢�B.�ܢ�C.�ڢ�D.�ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ũ�Ⱦ�Ϊ3mol��L-1������������100mL���ֱ�����������Fe�ۣ���Ӧ��Ϻ��������������֮��Ϊ3��4������������е����۵�����Ϊ
A. 5.6g B. 8.4g C. 11.2g D. 16.8g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Li4Ti5O12��LiFePO4��������ӵ�صĵ缫���ϣ���������������Ҫ�ɷ�ΪFeTiO3������������MgO��SiO2�����ʣ����Ʊ��������������£�

�ش��������⣺
��1���������ʵ���У����Ľ����ʽ������ͼ��ʾ����ͼ��֪�������Ľ�����Ϊ70%ʱ�������õ�ʵ������Ϊ_____________��
��2���������������Ҫ��![]() ��ʽ���ڣ�д����Ӧ��Ӧ�����ӷ���ʽ________��
��ʽ���ڣ�д����Ӧ��Ӧ�����ӷ���ʽ________��
��3��TiO2��xH2O������˫��ˮ����ˮ��Ӧ40 min����ʵ�������±���ʾ��

����40 ��ʱTiO2��xH2Oת������ߵ�ԭ��________��
��4��Li2Ti5O15��Ti�Ļ��ϼ�Ϊ+4�����й���������ĿΪ_______��
��5��������Һ�ڡ���![]() ������˫��ˮ�����ᣨ����Һ�������1������ʹ
������˫��ˮ�����ᣨ����Һ�������1������ʹ![]() ǡ�ó�����ȫ����Һ��
ǡ�ó�����ȫ����Һ��![]() ����ʱ�Ƿ���
����ʱ�Ƿ���![]() �������ɣ� ________����ʽ���㣩��
�������ɣ� ________����ʽ���㣩��![]() ��Ksp�ֱ�Ϊ
��Ksp�ֱ�Ϊ![]()
��6��д�����������բڡ�����![]() �Ʊ�
�Ʊ�![]() �Ļ�ѧ����ʽ___________��
�Ļ�ѧ����ʽ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ��������������ԭ�����͵��ǣ� ��
A. FeCl3+3KSCN![]() Fe(SCN)3+3KClƽ����ϵ�м�������KSCN���壬��Һ��ɫ����
Fe(SCN)3+3KClƽ����ϵ�м�������KSCN���壬��Һ��ɫ����
B. ��ҵ�ϳɰ��У�������Һ������
C. A��B��֧�Թ��зֱ��������5%��H2O2��Һ����B�Թ��м���2��3��FeCl3��Һ��B���Թ��в������ݿ�
D. ���ڷ�Ӧ2NO2(g)![]() N2O4(g) ��H<0�������¶ȿ�ʹ��ϵ��ɫ����
N2O4(g) ��H<0�������¶ȿ�ʹ��ϵ��ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij��HA�ĵ��볣��Ka=2.0��10-8����2mol/LNaOH��Һ�ζ�100ml2mol/LHA��Һ����Һ��pH�����NaOH��Һ������仯������ͼ![]() ����˵����ȷ����
����˵����ȷ����

A. a����Һ��pH=4
B. b����Һ�д��ڣ�c��A-��>c��Na+��>c��H+��=c��OH-��
C. b��c��HA��/c��A-��=5
D. c��c��A-��+c��H+��=c��Na+��+c��OH-��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���в���ȷ����
A. K2FeO4�ɴ���Cl2��������ˮ����ɱ����������
B. CaO2���ڼ��������Ҳ�������ӻ�������������Ӹ�����Ϊ1:2
C. ���ݹ����������Һ�Ĺ������������ʵ�ˮ��������Ϊ�˱���ˮ��
D. �����¿��ý����ƻ�ԭ���Ȼ�������ȡ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com