
| A. | 若能与金属钠和碳酸氢钠反应,则其结构中同时含有-OH和-COOH | |
| B. | 若该物质中含有两个-CH3,则它可以是碳酸酯 | |
| C. | 若该物质中结构中不能只含有C-O键和C-H键 | |
| D. | 若1mol C3H6O3与足量钠反应只产生1mol氢气,说明一分子C3H6O3中含有2个-OH和一个-CHO |
分析 该物质不饱和度=$\frac{3×2+2-6}{2}$=1,说明含有一个不饱和键,可能含有一个-COOH和一个-OH,可能含有一个-COO-和一个-OH、可能含有一个-CHO和两个-OH,可能含有-COOH和-O-等,据此分析解答.
解答 解:该物质不饱和度=$\frac{3×2+2-6}{2}$=1,说明含有一个不饱和键,可能含有一个-COOH和一个-OH,可能含有一个-COO-和一个-OH、可能含有一个-CHO和两个-OH,可能含有-COOH和-O-,
A.若能与金属钠和碳酸氢钠反应,-COOH和Na、碳酸氢钠都反应,该分子中可能不含-OH,含有-O-,故A错误;
B.若该物质中含有两个-CH3,则它可以是碳酸酯,为碳酸甲酯,故B正确;
C.若该物质中结构中能只含有C-O键和C-H键,为环状的醚,故C错误;
D.若1mol C3H6O3与足量钠反应只产生1mol氢气,一分子C3H6O3中可能含有2个-OH和一个-CHO或1个-COOH、一个-OH,故D错误;
故选B.
点评 本题考查有机物结构和性质,为高频考点,侧重考查学生分析判断能力,正确判断可能的结构是解本题关键,注意同分异构体种类判断方法,题目难度中等.


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ①②④⑤ | C. | ②⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物.
第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 侯德榜--创立了联合制碱法 | |
| B. | 凯库勒--首次提出了“有机化学”概念 | |
| C. | C维勒--首次用无机物合成了有机物 | |
| D. | 门捷列夫--创设了元素周期表 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.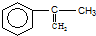 出发来合成A,其合成路线如下:
出发来合成A,其合成路线如下: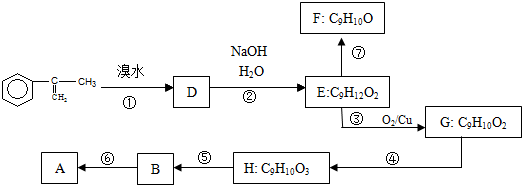
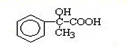
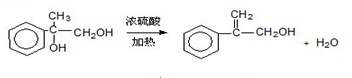 .两分子H之间发生反应生成六元环酯化学方程式是:2
.两分子H之间发生反应生成六元环酯化学方程式是:2 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$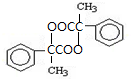 +2H2O.
+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验 | 编号 | 实验温度/℃ | 药品 | |
| Ⅰ | ① | 25 | 铝条 | 盐酸5ml3mol•L-1 |
| ② | 25 | 铝条(规格同上) | 盐酸5ml0.5mol•L-1 | |
| Ⅱ | ① | 25 | 碳酸钙粉末 | 盐酸5ml3mol•L-1 |
| ② | 25 | 块状碳酸钙 | 盐酸5ml3mol•L-1 | |
| Ⅲ | ① | 5 | 二氧化氮与四氧化二氮的混合气体 | |
| ② | 35 | 二氧化氮与四氧化二氮的混合气体 | ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com