
【题目】(1)锌电池有望代替铅蓄电池,它的构成材料是锌、空气某种电解质溶液,发生的总反应式是:2Zn+O2=2ZnO。则该电池的负极材料是(写名称)____________;当导线中有1mol电子通过时,理论上消耗的O2在标准状况下的体积是__________。
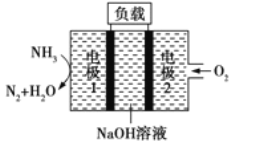
(2)瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池示意图如下所示,该燃料电池工作时,外电路中电子的流动方向是从电极________到电极________(填“1”或“2”),电池的总反应为________。
【答案】 锌 5.6L 1 2 4NH3+3O2=2N2+6H2O
【解析】(1)Zn失去电子,发生氧化反应,作原电池负极,O2得到电子发生还原反应,作原电池正极;每消耗1molO2转移4mole-,当导线中通过1mole-时,消耗0.25molO2;
②燃料电池工作时,还原性气体NH3在电极1失电子,发生氧化反应,所以电极1为负极,O2在电极2得电子,发生还原反应,所以电极2为正极,电池总反应为:4NH3+3O2=2N2+6H2O。以此解答。
(1)Zn失去电子,发生氧化反应,作原电池负极,O2得到电子发生还原反应,作原电池正极;每消耗1molO2转移4mole-,当导线中通过1mole-时,消耗0.25molO2,在标准状况下的体积为:0.25mol×22.4L/mol=5.6L。
因此,本题答案为:锌 ;5.6L;
②燃料电池工作时,还原性气体NH3在电极1失电子,发生氧化反应,所以电极1为负极,电极反应式为:2NH3+6OH—6e-=N2+6H2O;电子从电极1经外电路到电极2,O2在电极2得电子,发生还原反应,所以电极2为正极,电极反应式为:O2+4e-+2H2O=4OH-,电池总反应为:4NH3+3O2=2N2+6H2O。
因此,本题答案为:1 ,2;; 4NH3+3O2=2N2+6H2O。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
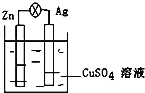
【题目】在银锌原电池中,以硫酸铜为电解质溶液,锌为_____极,电极上发生的是_____反应(“氧化”或“还原”).电极反应式为_____,锌片上观察到的现象为_____银为_____极,电极上发生的是_____反应(“氧化”或“还原”),电极反应式是_____,银片上观察到的现象是_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A,B两种液态有机物均由碳、氢、氧三种元素组成。A能溶于水,它的相对分子质量是60,分子中有8个原子,其中氧原子数与碳原子数相等,且A与碳酸钠溶液混合时冒气泡。B分子中有9个原子,分子内所有原子的核电荷数之和为26,且B只能跟钠反应放出氢气,不能与碳酸钠溶液反应。
(1)A的结构简式为 __________________ ,B的结构简式为 ________________。
(2)写出A与碳酸钠溶液反应的化学方程式________________________________。
(3)写出B与钠反应的化学方程式_____________________________。
(4)写出A与B反应的化学方程式_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示,其中A为地壳中含量最高的金属元素。
B | C | D | ||
A | E |
请用化学用语回答下列问题:
(1)A、D、E元素简单离子半径由大到小的顺序为 > > (填粒子符号)_____
(2)F与D同主族且相邻二者气态氢化物稳定性的大小关系为 > (填粒子符号)_________
(3)用高能射线照射含有10电子的D元素氢化物分子时,一个分子能释放出一个电子,同时产生一种
具有较强氧化性的阳离子,试写出该阳离子的电子式:______________。该阳离子中存在的化学键有_________。
(4)由C、E两种元素组成的化合物甲,常温下为易挥发的淡黄色液体,甲分子构型为三角锥形,且分子中C、E两种原子最外层均达到8个电子的稳定结构。甲遇水蒸气可形成一种常见的漂白性物质。写出甲遇水蒸气的化学方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H是一种香料,可用下图的设计方案合成。
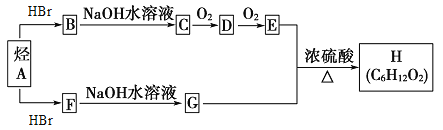
已知:
①R-CH2X![]() R-CH2OH(X代表卤素原子)。
R-CH2OH(X代表卤素原子)。
②在一定条件下,有机物有下列转化关系:
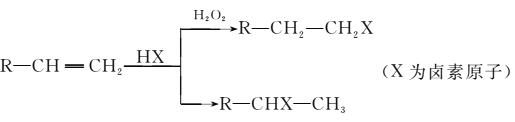
③烃A和等物质的量HBr在不同的条件下发生加成反应,既可以生成只含有一个甲基的B,也可以生成含有两个甲基的F。
(1)D的结构简式为_____________。
(2)烃A→B的化学反应方程式为:_____________。
(3)F→G的反应类型:_______________。
(4)E+G→H的化学反应方程式:________________。
(5)H有多种同分异构体,其中能与NaHCO3溶液反应产生气体,且其烃基上的一氯代物有两种的是(用结构简式表示):____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的盐酸跟过量的锌粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的 ①NaOH溶液 ②H2O ③CH3COONa固体 ④NaNO3溶液⑤稀硫酸
A.②③ B.②④ C.②③④ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅及其化合物有着优异的性能和广泛的应用。工业上利用铅浮渣(主要成分是PbO、Pb,还含有少量的Ag、CaO)制备硫酸铅。制备流程图如下
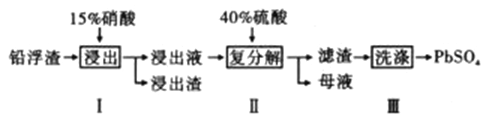
已知:Ksp(PbSO4)=1.6×10-8 Ksp(CaSO4)=4.9×10-5
(1)步骤I有NO产生浸出液中含量最多的金属阳离子为Pb2+,写出Pb参加反应的化学方程式___________________________,为防止Ag被溶解进入溶液,步骤I操作时应注意_______________________。
(2)粗PbSO4产品含有的杂质是____________;要得到纯净的PbSO4,需要用试剂进行多次洗涤,再用蒸馏水洗涤。最好选用的试剂是_________________。
A.稀硫酸 B.稀盐酸 C.硝酸铅溶液 D.酒精
(3)母液可循环利用的物质是HNO3,若母液中残留的SO42-过多,循环利用时可能出现的问题是______________________________。
(4)若将步骤Ⅱ中的Pb2+完全沉淀,则溶液中的c(SO42-)至少为___________mol/L。
(5)(CH3COO)2Pb是皮毛行业可溶于水的染色助剂,可用PbSO4与CH3 COONH4反应制备,写出该反应的离子方程式_______________________。
(6)铅蓄电池是电压稳定、使用方便的二次电池。PbSO4在其中扮演了重要角色,写出铅蓄电池充电时阳极的电极反应_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在生物实验中,可以根据与某些化学试剂所产生的颜色反应,检测生物组织中的有关有机化合物的存在。在下列实验列表中,正确的是( )
选项 | 待检测的物质 | 使用试剂 | 呈现颜色 |
A | 苹果中的还原糖 | 斐林试剂 | 橘黄色 |
B | 马铃薯中的淀粉 | 双缩脲试剂 | 蓝色 |
C | 花生的脂肪 | 苏丹Ⅲ染液 | 橘黄色 |
D | 大豆中的蛋白质 | 斐林试剂 | 紫色 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com