
【题目】下列事实不能用勒夏特列原理(平衡移动原理)解释的是
①溴水中存在化学平衡:Br2+H2O ![]() HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
②铁在潮湿的空气中易生锈
③二氧化氮与四氧化二氮的平衡体系,增大压强后颜色加深
④合成氨反应,为提高氨的产率,理论上应采取降低温度的措施
⑤钠与氯化钾共融制备钾:Na(l)+KCl(l) ![]() K(g)+NaCl(l)
K(g)+NaCl(l)
A.①④B.③④C.②⑤D.②③
【答案】D
【解析】
根据题中勒夏特列原理可知,本题考查改变影响平衡的条件,运用如果改变影响平衡的条件之一,平衡将向着能够减弱这种改变的方向移动和使用勒夏特列原理时,该反应必须是可逆反应分析。
①加入AgNO3溶液后,AgNO3和HBr反应导致平衡正向移动,则溶液颜色变浅,能用平衡移动原理解释,故①不选;
②铁在潮湿的空气中易生锈是电化学腐蚀,不是可逆反应,故②选;
③增大压强,平衡正向移动,气体颜色变浅,但颜色加深是体积缩小,二氧化氮浓度变大,不能用平衡移动原理解释,故③选;
④合成氨反应是放热反应,降低温度平衡正向移动,提高氨的产率,故④不选;
⑤K为气体,减小生成物的浓度可使平衡正向移动,能用勒夏特列原理解释,故⑤不选;
答案选D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:
【题目】硒可防止人体因氧化而引起的衰老、组织硬化。回答下列问题:
(1)写出基态硒(Se)原子的价电子排布式____________;其中未成对电子数为_________;
(2)砷(As)和硒(Se)的第一电离能较大的是__________________;
(3)SeF2的立体构型为______________,Se原子的杂化方式为____________________;
(4)H2Se和H2O的熔沸点较高的是_________,原因是___________________________;
![]()
(5)Se和Zn组成的某种晶胞如图所示,则该晶体的化学式为________________,若已知该晶胞的密度为ρg/cm3,则该晶胞的棱长a=_______cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电离平衡常数是衡量弱电解质电离程度的物理量。已知:
化学式 | 电离常数(25 ℃) |
HCN | K=4.9×10-10 |
CH3COOH | K=1.8×10-5 |
H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
(1)25 ℃时,有等浓度的NaCN溶液、Na2CO3溶液和CH3COONa溶液,三溶液的pH由大到小的顺序为________(用化学式表示)。
(2)向NaCN溶液中通入少量的CO2,发生反应的化学方程式为_____________。
(3)25 ℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=________ mol·L-1(填精确值),c(CH3COO-)/c(CH3COOH)=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在A、B两个恒容密闭容器中发生反应:2NO22NO +O2反应过程中NO2的物质的量随时间变化的状况如图所示:
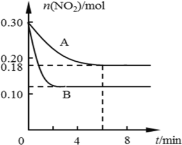
(1)若A容器的体积为5 L,反应经6 min达到平衡状态,则0~6 min内以O2浓度变化表示的反应速率为___________。
(2)该反应化学平衡常数K=__________(写出表达式)。
(3)说明该反应已达到平衡状态的是_______。
A.v正(NO2)=v逆(NO)B.c(NO2)=c(NO)
C.气体的平均摩尔质量不变 D.气体的密度保持不变
(4)若A、B两容器中只是温度不同,则TA____TB (填“>”或“<”),请写出一条能提高二氧化氮转化率的措施_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值.下列叙述错误的是
A.7.8gNa2O2与过量水反应转移电子数为0.1NA
B.1 mol OD-离子含有的质子、中子数均为9NA
C.46g NO2和N2O4混合气体中含有原子总数为3NA
D.已知N2(g)+3H2(g)![]() 2NH3(g)△H=﹣92.4kJ·mol﹣1,当有3NA个电子转移时,△H变为﹣46.2kJ·mol﹣1
2NH3(g)△H=﹣92.4kJ·mol﹣1,当有3NA个电子转移时,△H变为﹣46.2kJ·mol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,改变反应物中n(SO2)对反应2SO2(g)+O2(g)2SO3(g) △H<0的影响如图所示,下列说法正确的是
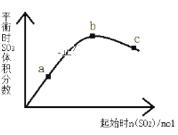
A.a、b、c三点中,平衡时的速率大小关系:v(b)>v(c)>v(a)
B.a、b、c三点中,a点时SO2的转化率最高
C.上述图象可以得出SO2的含量越高得到的混合气体中SO3的体积分数越高
D.a、b、c三点的平衡常数Kb>Kc>Ka
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】查尔酮类化合物![]() (
(![]() )的一种合成路线如下:
)的一种合成路线如下:

已知:![]()
回答下列问题:
(1)![]() 的名称为_______,
的名称为_______,![]() 的官能团名称为_____________。
的官能团名称为_____________。
(2)![]() 的分子式为_____________________。
的分子式为_____________________。
(3)![]() 的反应类型为____________________。
的反应类型为____________________。
(4)![]() 的反应方程式为_________________。
的反应方程式为_________________。
(5)M是E的同分异构体,满足下列条件,其中核磁共振氢谱有4组吸收峰,峰面积之比为![]() 的结构为__________________。
的结构为__________________。
①能发生水解反应 ②遇![]() 显色
显色
(6)参照上述合成路线,写出用苯乙烯与苯甲醛为原料制备查尔酮(![]() )的合成路线(其他试剂任选)。________________
)的合成路线(其他试剂任选)。________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】骨胶黏剂是一种极具应用前景的医用高分子材料。某骨胶黏剂的制备原料为聚酯三元醇,其合成原理如下:
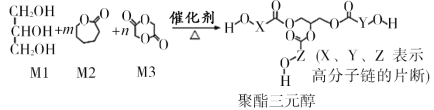
已知:R1COOR2+R318OH![]() R1CO18OR3+R2OH
R1CO18OR3+R2OH
下列说法正确的是
A.单体Ml可用于配制化妆品,且分子中含有3个手性碳原子
B.改变Ml在三种单体中的比例,可调控聚酯三元醇的相对分子质量
C.该合成反应为缩聚反应
D.X、Y、Z中包含的结构片段可能有![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组以Mg(NO3)2为研究对象,拟通过实验初步探究硝酸盐热分解的规律.
(提出猜想)小组提出如下4种猜想:
甲:Mg(NO3)2、NO2、O2 乙:MgO、NO2、O2
丙:Mg3N2、O2 丁:MgO、NO2、N2
(1)查阅资料得知,NO2可被NaOH溶液吸收,反应的化学方程式为:____________.
(2)实验前,小组成员经讨论认定猜想丁不成立,理由是____________.
(实验操作)
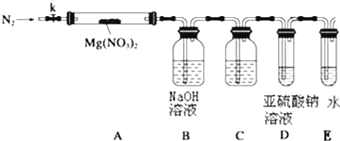
(3)设计如图装置,用氮气排尽装置中空气,其目的是___________;加热Mg(NO3)2固体,AB装置实验现象是:____________,说明有Mg(NO3)2固体分解了,有NO2生成.
(4)有同学提出可用亚硫酸钠溶液检验是否有氧气产生,但通入之前,还需在BD装置间增加滴有酚酞的氢氧化钠溶液,其作用是:____________
(5)小组讨论后认为即便通过C后有氧气,仅仅用亚硫酸钠溶液仍然难以检验,因为:____________,改进的措施是可在亚硫酸钠溶液中加入____________.
(6)上述系列改进后,如果分解产物中有O2存在,排除装置与操作的原因,未检测到的原因是____________.(用化学方程式表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com