
【题目】反应aA(g)+bB(g)![]() cC(g) (ΔH<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示:
cC(g) (ΔH<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示:
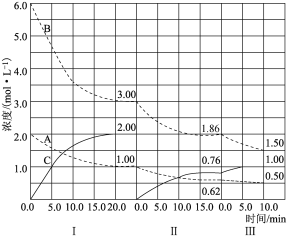
(1)第Ⅰ阶段达平衡时的平衡常数K=___。
(2)A的平均反应速率vⅠ(A)、vⅡ(A)、vⅢ(A)从小到大排列次序为___;
(3)B的平衡转化率αⅠ(B)、αⅡ(B)、αⅢ(B)中最大的是___;
(4)由第Ⅰ阶段平衡到第Ⅱ阶段平衡,平衡移动的方向是___,采取的措施是___;
(5)比较第Ⅱ阶段反应温度(T2)和第Ⅲ阶段反应温度(T3)的高低:T2__T3(填“>”“<”“=”),判断的理由是___。
【答案】![]() vⅢ(A)、vⅡ(A)、vⅠ(A) αⅠ(B) 向正反应方向 从反应体系中移出产物C > 此反应为放热反应,降低温度,平衡向正反应方向移动
vⅢ(A)、vⅡ(A)、vⅠ(A) αⅠ(B) 向正反应方向 从反应体系中移出产物C > 此反应为放热反应,降低温度,平衡向正反应方向移动
【解析】
(1)由图第Ⅰ阶段,达到平衡时各物质的浓度,根据平衡常数=![]() 计算
计算
(2)根据化学反应速率为单位时间浓度的变化值,可计算三个阶段用A表示的化学反应速率,据此判断;
(3)转化率是物质的减少量与初始量的比值,计算三个阶段B的转化率,据此解答;
(4)第Ⅱ阶段C是从0开始的,瞬间A、B浓度不变,因此可以确定第一次平衡后从体系中移出了C,即减少生成物浓度,平衡正向移动;
(5) 第Ⅲ阶段的开始与第Ⅱ阶段的平衡各物质的量均相等,根据A、B的量减少,C的量增加可判断平衡是正向移动的,根据平衡开始时浓度确定此平衡移动不可能是由浓度的变化引起的,另外题目所给条件容器的体积不变,则改变压强也不可能,因此一定为温度的影响,此反应正向为放热反应,可以推测为降低温度,另外结合A的速率在三个阶段的情况,确定改变的条件一定为降低温度,根据勒夏特列原理,平衡的移动只能减弱改变,不能抵消改变,因此达到平衡后温度一定比第Ⅱ阶段平衡时的温度低。
(1)由图可知第Ⅰ阶段,平衡时△c(A)=2mol/L-1mol/L=1mol/L,△c(B)=6mol/L-3mol/L=3mol/L,△c(C)=2mol/L,浓度变化量之比等于化学计量数之比,故a:b:c=1mol/L:3mol/L:2mol/L=1:3:2, A(g)+3B(g)![]() 2C(g),根据平衡常数=
2C(g),根据平衡常数=![]() =
=![]() =
=![]() ;
;
(2)vⅠ(A)=![]() =0.05mol/(Lmin),vⅡ(A)=
=0.05mol/(Lmin),vⅡ(A)=![]() =0.0253mol/(Lmin),
=0.0253mol/(Lmin),
vⅢ(A)=![]() =0.012mol/(Lmin),故A的平均反应速率vⅠ(A)>vⅡ(A)>vⅢ(A);
=0.012mol/(Lmin),故A的平均反应速率vⅠ(A)>vⅡ(A)>vⅢ(A);
(3)B的平衡转化率αⅠ(B)=![]() ×100%=50%,αⅡ(B)=
×100%=50%,αⅡ(B)=![]() ×100%=38%,
×100%=38%,
αⅢ(B)=![]() ×100%=19.4%,则B的转化率最大的为αⅠ(B);
×100%=19.4%,则B的转化率最大的为αⅠ(B);
(4)第Ⅱ阶段C是从0开始的,瞬间A、B浓度不变,因此可以确定第一次平衡后从体系中移出了C,即减少生成物浓度,平衡正向移动;
(5)第Ⅲ阶段的开始与第Ⅱ阶段的平衡各物质的量均相等,根据A、B的量减少,C的量增加可判断平衡是正向移动的,根据平衡开始时浓度确定此平衡移动不可能是由浓度的变化引起的,另外题目所给条件容器的体积不变,则改变压强也不可能,因此一定为温度的影响,此反应正向为放热反应,可以推测为降低温度,另外结合A的速率在三个阶段的情况,确定改变的条件一定为降低温度,根据勒夏特列原理,平衡的移动只能减弱改变,不能抵消改变,因此达到平衡后温度一定比第Ⅱ阶段平衡时的温度低。


科目:高中化学 来源: 题型:
【题目】化学知识可以帮助理解和解决日常生活中遇到的许多问题,下列说法正确的是![]()
A.晶体硅是在通信工程中制作光导纤维的主要原料
B.某些天然温泉水中含有游离态的硫,对某些皮肤病有一定的治疗作用
C.水晶项链和餐桌上的瓷盘都是硅酸盐制品
D.工艺师利用盐酸刻蚀石英制作艺术品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2017·天津卷)常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g)![]() Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断正确的是
A. 增加c(CO),平衡向正向移动,反应的平衡常数增大
B. 第二阶段,Ni(CO)4分解率较低
C. 第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
D. 该反应达到平衡时,v生成[Ni(CO)4]=4v生成(CO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与人类生产、生活、科研密切相关,下列有关说法不正确的是
A.维生素C能帮助人体将![]() 转化为易吸收的
转化为易吸收的![]() ,维生素C具有氧化性
,维生素C具有氧化性
B.“火树银花合,星桥铁索开”,其中的“火树银花”涉及到焰色反应
C.中国蓝是人工合成的蓝色化合物,其化学式为![]() ,可改写成
,可改写成![]()
D.赏心悦目的雕花玻璃是使用氢氟酸对玻璃刻蚀而成的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列叙述中正确的是( )
4NO(g)+6H2O(g),下列叙述中正确的是( )
A. 达到化学平衡时4v正(O2)=5v逆(NO)
B. 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达平衡状态
C. 达到化学平衡时,若升高温度,则正反应速率减小,逆反应速率增大
D. 平衡混合物中各物质的量浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各实验操作中错误的是![]()
![]() 实验室制乙烯时,温度计水银球应插入混合液中
实验室制乙烯时,温度计水银球应插入混合液中
![]() 配制氢氧化铜悬浊液时,向硫酸铜溶液中逐滴滴加氢氧化钠溶液,直到沉淀完全为止
配制氢氧化铜悬浊液时,向硫酸铜溶液中逐滴滴加氢氧化钠溶液,直到沉淀完全为止
![]() 配制银氨溶液时,向硝酸银溶液中逐滴滴加氨水,边滴边振荡,直到生成的沉淀溶解为止
配制银氨溶液时,向硝酸银溶液中逐滴滴加氨水,边滴边振荡,直到生成的沉淀溶解为止
![]() 用醋酸、碳酸氢钠、苯酚钠和必须的仪器可以检验苯酚、醋酸、碳酸的酸性强弱
用醋酸、碳酸氢钠、苯酚钠和必须的仪器可以检验苯酚、醋酸、碳酸的酸性强弱
![]() 做过银镜反应的试管用浓硝酸清洗
做过银镜反应的试管用浓硝酸清洗
![]() 卤代烃与氢氧化钠溶液共热后,再滴入硝酸银溶液,可检验卤原子的种类
卤代烃与氢氧化钠溶液共热后,再滴入硝酸银溶液,可检验卤原子的种类
![]() 若苯酚不慎沾到皮肤上,应立即用酒精洗涤
若苯酚不慎沾到皮肤上,应立即用酒精洗涤
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学反应的描述中正确的是( )
A.需要加热才能发生的反应一定是吸热反应
B.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=-57.3 kJ/mol,则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出57.3 kJ的热量
C.CO(g)的燃烧热是283.0 kJ/mol,则表示CO(g)的燃烧热的热化学方程式为2CO(g)+O2(g)=2CO2(g) △H=-283.0 kJ/mol
D.已知2C(s)+2O2(g)=2CO2(g) △H=a,2C(s)+O2(g)=2CO(g) △H=b,则b>a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用电化学原理,将NO2、O2和熔融KNO3制成燃料电池,模拟工业电解法来处理含Cr2O72-废水,如下图所示;电解过程中溶液发生反应:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
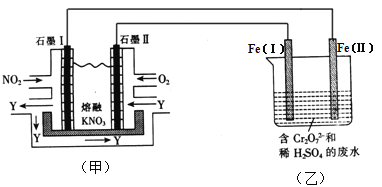
(1)甲池工作时,NO2转变成绿色硝化剂Y,Y是N2O5,可循环使用。则石墨Ⅱ是电池的 极;石墨Ⅰ附近发生的电极反应式为 。
(2)工作时,甲池内的NO3-离子向 极移动(填“石墨Ⅰ”或“石墨Ⅱ”);在相同条件下,消耗的O2和NO2的体积比为 。
(3)乙池中Fe(Ⅰ)棒上发生的电极反应为 。
(4)若溶液中减少了0.01 mol Cr2O72-,则电路中至少转移了 mol电子。
(5)向完全还原为Cr3+的乙池工业废水中滴加NaOH溶液,可将铬以Cr(OH)3沉淀的形式除去,已知Cr(OH)3存在以下溶解平衡:Cr(OH)3(s) ![]() Cr3+(aq)+3OH-(aq),常温下Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH-)=1.0×10-32,要使c(Cr3+)降至10-5mol·L-1,溶液的pH应调至 。
Cr3+(aq)+3OH-(aq),常温下Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH-)=1.0×10-32,要使c(Cr3+)降至10-5mol·L-1,溶液的pH应调至 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com