
����Ŀ��2007��ŵ������ѧ���������������������¡��ĵ¹���ѧ�Ҹ���°��ض������ijɾ�֮һ��֤ʵ�������ڹ������������еķ�Ӧ�������˱��滯ѧ�ķ����ۣ�������β������װ��������ڴ�������������������õĹ�����ͼ��ʾ������˵����ȷ���ǣ� ��
A.NO2�Ǹù��̵����ղ���
B.NO��O2�����ڴ���������ܷ�Ӧ
C.����β������Ҫ��Ⱦ�ɷ���CO2��NO
D.�ô�ת�����ܷ�Ӧ����ʽΪ��2NO+O2+4CO ![]() 4CO2+N2
4CO2+N2
���𰸡�D
���������⣺A�������ڴ�������������������õĹ����������ɶ���������Ȼ���ڴ��������һ����̼��Ӧ���������������壬��β�����������ã����м������������ղ����A����
B��NO��O2�ڳ����¾ͻᷢ����Ӧ����B����
C������β������Ҫ��Ⱦ�ɷ���CO��NO��NO2�ȣ�������̼������Ⱦ���壬��C����
D��β������������Ŀ���ǰ��ж�����Ⱦ�����ڴ���������ת��Ϊ�����е����ɷ֣���Ӧ����ʽ2NO+O2+4CO ![]() 4CO2+N2�����ǹ���ͼ�еı仯����D��ȷ��
4CO2+N2�����ǹ���ͼ�еı仯����D��ȷ��
��ѡD��


 �Ǽ�����������ϵ�д�
�Ǽ�����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Һ��ˮϡ��ʱ�����¶Ȳ��䣬�������������ֲ������(����)
A. ��Һ���� B. �ܼ�����
C. �����ܽ�� D. ��Һ��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ��IIV��ʵ������Ԥ����ȷ���ǣ� �� 
A.ʵ�����εμ�����ʱ���Թ�������������������
B.ʵ�������ã��²���ҺΪ�Ⱥ�ɫ���ϲ���ɫ
C.ʵ��ӱ���ʳ��ˮ����ȡNaCl����
D.װ�â�������KMnO4��Һ�������ݳ��֣�����Һ��ɫ����dz������ȥ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڹ�ҵ�ϳ���CO��H2�ϳɼ״�����Ӧ����ʽΪ��
CO��g��+2H2��g��![]() CH3OH��g�� ��H = akJ/mol
CH3OH��g�� ��H = akJ/mol
��֪����CO��g��+![]() O2��g��== CO2��g�� ��H1=��283.0kJ/mol
O2��g��== CO2��g�� ��H1=��283.0kJ/mol
��H2��g��+![]() O2��g��== H2O��g����H2=��241.8kJ/mol
O2��g��== H2O��g����H2=��241.8kJ/mol
��CH3OH��g��+![]() O2��g��== CO2��g��+ 2H2O��g����H3=��192.2kJ/mol
O2��g��== CO2��g��+ 2H2O��g����H3=��192.2kJ/mol
�ش��������⣺
(1)a = _______
(2)��˵����ӦCO��g��+2H2��g��![]() CH3OH��g���Ѵ�ƽ��״̬����___������ĸ����
CH3OH��g���Ѵ�ƽ��״̬����___������ĸ����
A����λʱ��������1mol CH3OH��g����ͬʱ������1mol CO��g��
B���ں��º��ݵ������У����������ܶȱ��ֲ���
C���ھ��Ⱥ��ݵ������У���Ӧ��ƽ�ⳣ�����ٱ仯
D���ں��º�ѹ�������У������ƽ��Ħ���������ٱ仯
(3)��T1��ʱ�����Ϊ2L�ĺ��������г������ʵ���֮��Ϊ3mol��H2��CO����Ӧ�ﵽƽ��ʱCH3OH�����������V%����![]() �Ĺ�ϵ��ͼ1��ʾ��
�Ĺ�ϵ��ͼ1��ʾ��
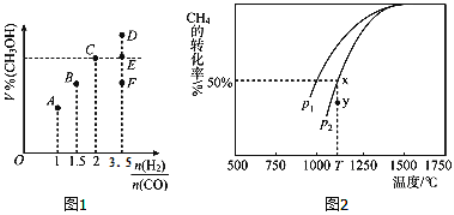
�ٵ���ʼ![]() =2ʱ������5min�ﵽƽ�⣬CO��ת����Ϊ0.6����0��5min��ƽ����Ӧ����v��H2��=_____________������ʱ���������м���CO��g����CH3OH��g����0.4mol������ƽ��ʱH2��ת���ʽ�____________��ѡ����������������С����������������
=2ʱ������5min�ﵽƽ�⣬CO��ת����Ϊ0.6����0��5min��ƽ����Ӧ����v��H2��=_____________������ʱ���������м���CO��g����CH3OH��g����0.4mol������ƽ��ʱH2��ת���ʽ�____________��ѡ����������������С����������������
�ڵ�![]() = 3.5ʱ���ﵽƽ��״̬��CH3OH���������������ͼ���е�_______�㣨ѡ����D������E������F������
= 3.5ʱ���ﵽƽ��״̬��CH3OH���������������ͼ���е�_______�㣨ѡ����D������E������F������
(4)CO��H2��������Ȼ������֪CO2��g��+CH4��g��![]() 2CO��g��+2H2��g�������ܱ���������Ũ�Ⱦ�Ϊ0.1molL��1��CH4��CO2����һ�������·�Ӧ�����CH4��ƽ��ת�������¶ȼ�ѹǿ�Ĺ�ϵ��ͼ2����ѹǿp1_______________p2��ѡ��������������С����������ѹǿΪp2ʱ����y�㣺v������______________v���棩��ѡ��������������С��������������������p2=3MPa����T��ʱ�÷�Ӧ��ƽ�ⳣ��Kp=_________MPa2����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�����������
2CO��g��+2H2��g�������ܱ���������Ũ�Ⱦ�Ϊ0.1molL��1��CH4��CO2����һ�������·�Ӧ�����CH4��ƽ��ת�������¶ȼ�ѹǿ�Ĺ�ϵ��ͼ2����ѹǿp1_______________p2��ѡ��������������С����������ѹǿΪp2ʱ����y�㣺v������______________v���棩��ѡ��������������С��������������������p2=3MPa����T��ʱ�÷�Ӧ��ƽ�ⳣ��Kp=_________MPa2����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�����������
(5)���м״��ķ�ˮ����ɻ�����Ⱦ����ͨ��ClO2���彫������ΪCO2��д����ط�Ӧ�����ӷ���ʽ_________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯���������仯���ǣ� ��
A.������ˮB.������ȷֽ�
C.Һ��ӷ�D.ʯ�ʹ��ѻ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������Ȫʵ�飬�������ð���(����)
A. ��Һ�� B. �ȿ����� C. ��������ˮ D. �ܸ�ˮ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���ֽ�����ĩ�Ļ����25g��Ͷ��������ϡ�����У��ڱ���²�������11.2L����û���������
A.����þB.þ����C.����ͭD.����п
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪: 25�桢101 kPa�£��� 2 Na(s) + 1/2 O2(g) = Na2O(s) ��H1 = - 414 kJ / mol
�� 2 Na(s) + O2(g) = Na2O2(s) ��H2 = - 511 kJ / mol
����˵����ȷ����
A. ������������������Ӹ����Ȳ����
B. ���������ɵ����ʵ����IJ��ת�Ƶ�������ͬ
C. ������Na������O2��Ӧ����Na2O�����¶���������Na2O�������ӿ�
D. 25�桢101 kPa�£�Na2O2(s) + 2 Na(s) = 2 Na2O(s) ��H = -317 kJ / mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NH4Cl������ˮ(D2O)������һˮ�ϰ���ˮ�������Ӿ���ȷ����(����)
A. NH2D��H2O��D3O+ B. NH3��D2O��HD2O+
C. NH3��HDO��D3O+ D. NH2D��HDO��H2DO+
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com