
下列有关实验操作设计、现象记录、结论解释都正确的是
实验操作设计 | 现象记录 | 结论解释 | |
A | 用坩埚钳夹住铝箔在酒精灯 上加热 | 铝箔熔化但并不滴落 | 熔点:Al2 O3>Al |
B | 把浓硫酸滴到pH试纸上 | 试纸变红 | 浓硫酸具有酸性 |
C | 向某氯化亚铁溶液中加入 Na2O2粉末 | 出现红褐色沉淀 | 加入Na2O2粉末前,原氯化 亚铁溶液已经变质 |
D | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中含有Na+,无K+ |
科目:高中化学 来源:2015-2016学年山东省高一上12月月考化学试卷(解析版) 题型:实验题
某校化学小组的同学开展测定Na2CO3和NaCl的固体混合物中Na2CO3的质量分数的探究实验,他们提出下列实验方案。

【方案一】气体分析法。
(1)甲同学用图1所示装置,把xg的混合物与足量稀硫酸反应后,测定产生的C02气体的体积.实验开始时检查该装置气密性的方法是 _____________________;
(2)乙同学用图2代替图1中的收集装置,则所测CO2气体的体积_________(填“偏大”、“偏小”、“不变”),你的改进方案是_____________________;
(3)丙同学用图3装置测定CO2的质量,该装置存在较多缺陷,从而导致实验误差,请你填写其中的三点缺陷:I _____________________,Ⅱ_____________________,Ⅲ_____________________;
【方案二】沉淀分析法(如图所示).

(4)操作1的名称是______________,操作2的名称是___________,在进行操作2之前,应判断是否沉淀完全,判断的方法是_____________________;
(5)根据沉淀分析法,该固体混合物中Na2CO3质量分数的计算式为_____________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏六盘山中学高二上第二次月考化学试卷(解析版) 题型:选择题
25℃时,向V mL pH=a的盐酸中,滴加10V mL pH=b的NaOH溶液,所得溶液中Cl-的物质的量恰好等于Na+的物质的量,则a+b的值是
A.15 B.14 C.13 D.不能确定
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一上12月月考化学试卷(解析版) 题型:选择题
下列关于物质或离子检验的叙述正确的是
A.在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+
B.气体通过无水CuSO4,粉末变蓝,证明原气体中含有水蒸气
C.灼烧白色粉末,火焰呈黄色,证明原粉末中有Na+,无K+
D.某溶液中加入稀硫酸,放出无色无味气体,将该气体通入澄清石灰水,溶液变浑浊,证明原溶液中一定含有CO32-
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省高三上学期12月模拟化学试卷(解析版) 题型:实验题
空气污染问题日益引起全民关注。工业生产中产生的SO2、NO等为主要污染物。根据你所学化学知识完成下列问题:
Ⅰ.(1)PM2.5是指大气中直径小于或等于2.5μm(1μm=103nm)的颗粒物。下列说法不正确的是_________(填字母序号)。
a.PM2.5主要来源于火力发电、工业生产、汽车尾气排放等过程
b.PM2.5颗粒小,所以对人体无害
c.直径介于1~2.5μm的颗粒物分散到空气中可形成胶体
d.推广使用电动汽车,可以减少PM2.5的污染
(2)SO2为重要的含硫化合物,是形成酸雨的主要污染物之一。在实验室中,若用70%的硫酸溶液和亚硫酸钠粉末反应制取二氧化硫,并要求方便控制反应速率,可选用如图所示气体发生装置中的_______(填下列序号字母)。

(3)为研究SO2的性质,如图在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条火准)。
下列有关说法正确的是___________

A.蓝色石蕊试纸先变红后褪色
B.湿润的品红试纸、蘸有KMnO4溶液的滤纸均褪色证明SO2具有漂白性
C.湿润的淀粉KI-试纸未变蓝说明SO2的氧化性强于I2
D.NaOH溶液可用于除去实验中多余的SO2
(4)一定温度下,在密闭容器中SO2与O2反应生成1molSO3气体时,放出akJ热量。
①该温度下SO2与O2反应的热化学方程式为__________________________。
②已知:2NO(g)+O2(g)═2NO2(g) △H= -b kJ•mol-1 (a>b>0)
则反应NO2(g)+SO2(g)═SO3(g)+NO(g) 的△H=________________。
Ⅱ.硫酸工业尾气中二氧化硫的含量超过0.05%(体积分数)时需要处理后才能排放。某校化学兴趣小组欲测定某硫酸工厂排放尾气中的二氧化硫的含量,采用以下方案:
实验步骤如下图流程图所示:

(1)步骤①中反应的离子方程式为____________________________。
(2)步骤②中Ba(OH)2是否足量的判断方法是____________________________。
Ⅲ.工业生产中产生的SO2、NO直接排放将对大气造成严重污染。利用电化学原理吸收SO2和NO,同时获得 Na2S2O4和 NH4NO3产品的工艺流程图如下(Ce为铈元素).

请回答下列问题.
(1)装置Ⅱ中的反应在酸性条件下进行,写出NO被氧化为NO2-的离子方程式__________。
(2)装置Ⅲ的作用之一是再生Ce4+,其原理如图所示;
图中A为电源的______(填“正”或“负”)极.右侧反应室中发生的主要电极反应式为__________。
(3)已知进人装置Ⅳ的溶液中NO2-的浓度为 0.75mol/L,要使 1m3该溶液中的NO2-完全转化为 NH4NO3,需至少向装置Ⅳ中通入标准状况下的 O2的体积为_______L。
查看答案和解析>>
科目:高中化学 来源:2016届陕西省高三上学期12月月考化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A.CO2分子的比例模型:
B.过氧化氢的电子式: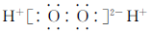
C.氟原子的结构示意图: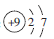
D.H2CO3的电离方程式:H2CO3 2H++CO32-
2H++CO32-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北邯郸魏县一中、曲周县一中高一上期中化学试卷(解析版) 题型:选择题
下列说法正确的是
A.向NaOH溶液中慢慢滴加FeCl3饱和溶液,可制得Fe(OH)3胶体
B.胶体与其他分散系的本质区别是胶体能发生丁达尔效应
C.除去Fe(OH)3胶体中的Na+和Cl﹣可用过滤的方法
D.Fe(OH)3胶体中逐滴加入稀硫酸,会产生沉淀而后沉淀溶解
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省枣阳市高一上学期期中考试化学试卷(解析版) 题型:选择题
下列物质的分类正确的是
碱 | 酸 | 盐 |
| 酸性氧化物 | |
A | NaOH | H2SO4 | BaCO3 | SO2 | CO2 |
B | NaOH | HCl | NaCl | Na2O | CO |
C | NaOH | CH3COOH | CaCl2 | CO | SO2 |
D | KOH | HNO3 | CaCO3 | CaO | SO3 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一上第三次月考化学试卷(解析版) 题型:选择题
溶液中能大量共存,加入OHˉ有沉淀析出,加入H+能放出气体的是
A. Na+、HCO3-、Ca2+、Cl-
B. Ba2+、K+、OH-、NO3-
C. H+、Fe3+、NH4+、SO42-
D. Mg2+、Na+、Cl-、CO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com