
| A、测所得溶液的pH |
| B、取溶液滴入酚酞观察是否变红 |
| C、取溶液加入盐酸观察是否有气泡 |
| D、取溶液加入CuSO4观察是否有沉淀 |


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源: 题型:
| 实验次数 | m(CuO)/(g) | 硫酸溶液/(ml) | m(CuSO4)/(g) |
| ① | 2.0 | 120 | 4.0 |
| ② | 4.0 | 120 | 8.0 |
| ③ | 6.0 | 120 | 9.6 |
| ④ | 8.0 | 200 | 16.0 |
| A、① | B、② | C、③ | D、④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
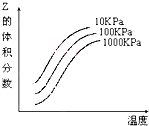 如图是温度和压强对X+Y?2Z 反应影响的示意图.图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数.下列叙述正确的是( )
如图是温度和压强对X+Y?2Z 反应影响的示意图.图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数.下列叙述正确的是( )| A、上述可逆反应的正反应为放热反应 |
| B、X、Y、Z均为气态 |
| C、X和Y中至多有一种是气态,Z必为气态 |
| D、上述反应的逆反应为吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、78g苯含有C=C双键的数目为3NA |
| B、室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA |
| C、0.1molMg在空气中完全燃烧生成MgO和Mg3N2,转移的电子数为0.2NA |
| D、50mL18.4mol?L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| 高温 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1L0.1mol/L醋酸 |
| B、0.1L0.1mol/LH2SO4溶液 |
| C、0.5L0.1mol/LHCl |
| D、2L0.1mol/LH2SO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、当一个反应是燃烧反应时,该燃烧反应的反应热就是燃烧热 |
| B、燃烧热是反应热的一种类型 |
| C、燃烧热不属于反应热,反应热是在25℃、101 kPa下测定的,而燃烧反应的温度要高 |
| D、反应热有正负之分,燃烧热全部是正值 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、和KI溶液反应的离子方程式:Fe3++2I-═Fe2++I2 |
| B、硫酸铁和Ba(OH)2溶液反应的离子方程式:Fe3++SO42-+Ba2++3OH-═Fe(OH)3↓+BaSO4↓ |
| C、1L0.1mol/L该溶液和足量的Zn充分反应,生成11.2gFe |
| D、该溶液中,K+、Fe3+、C6H5OH、Br-可以大量共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com