
 某化学兴趣小组为了测定某草酸晶体的纯度设计了如下实验.化学反应如下:KMnO4+H2C2O4+H2SO4-K2SO4+MnSO4+CO2↑+H2O(未配平)实验主要步骤如下:
某化学兴趣小组为了测定某草酸晶体的纯度设计了如下实验.化学反应如下:KMnO4+H2C2O4+H2SO4-K2SO4+MnSO4+CO2↑+H2O(未配平)实验主要步骤如下:| 2 |
| 5 |
| 5 |
| 2 |
| c(KMnO4)v(KMnO4) |
| V(H2C2O4) |
| 2 |
| 5 |
| 5 |
| 2 |
| c(KMnO4)v(KMnO4) |
| V(H2C2O4) |
| 100 |
| 25 |
| 0.02mol×126g/mol |
| 2.80g |


科目:高中化学 来源: 题型:
| A、7.84L |
| B、8.96L |
| C、15.68L |
| D、17.92L |
查看答案和解析>>
科目:高中化学 来源: 题型:
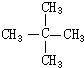 b.CH3CH2CH2CH2CH3 c.CH3CH=CHCH3 d.CH3CH=CH2
b.CH3CH2CH2CH2CH3 c.CH3CH=CHCH3 d.CH3CH=CH2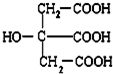
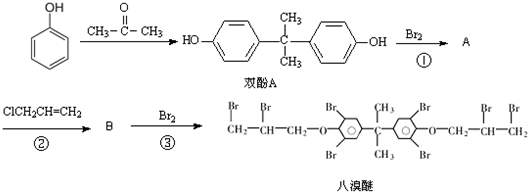
查看答案和解析>>
科目:高中化学 来源: 题型:
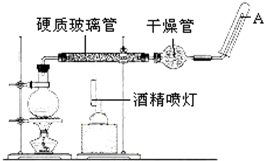 在高温下,Fe与水蒸气可发生反应.应用右边装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.
在高温下,Fe与水蒸气可发生反应.应用右边装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
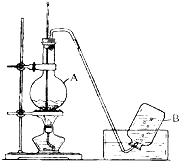 实验室用乙醇制取乙烯的装置如图,回答下列问题.
实验室用乙醇制取乙烯的装置如图,回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
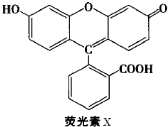
| A、1molX与足量的NaOH溶液在常温常压下反应,最多消耗3molNaOH |
| B、1molX最多能与9mol氢气反应 |
| C、X与足量的浓溴水反应,最多消耗4molBr2 |
D、X能与糠醛(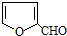 )发生缩聚反应 )发生缩聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com