
【题目】在密闭容器中进行反应:X2(g)+3Y2(g)![]() 2Z2(g),若X2、Y2、Z2的初始浓度分别为0.1 molL-1、0.3 molL-1、0.2 molL-1,当反应达到平衡后,各物质的浓度有可能的是( )
2Z2(g),若X2、Y2、Z2的初始浓度分别为0.1 molL-1、0.3 molL-1、0.2 molL-1,当反应达到平衡后,各物质的浓度有可能的是( )
①X2为0.2 molL-1 ②Y2为0.1 molL-1 ③Z2为0.3 molL-1 ④Y2为0.6 molL-1
A. ①② B. ②③ C. ③④ D. ①④
【答案】B
【解析】
根据反应X2(g)+3Y2(g)2Z2(g)为可能反应,反应体系中的各组分浓度不可能为0,根据初始浓度分别为0.1molL-1、0.3molL-1、0.2molL-1,结合反应方程式中各物质的化学计量数进行判断。
由于该反应是可逆反应,则反应物或生成物的浓度不可能是0,①中X2为0.2 mol/L,则需要消耗0.2 mol/L的Z2 ,此时生成物Z的浓度0,不可能,故①错误;②Y2为0.1molL-1,反应消耗0.2 mol/L×![]() =
=![]() molX2,由于X2为0.1molL-1,有可能,故②正确;③Z2为0.3molL-1,需要消耗0.05molL-1X2、0.15mol/L的Y2,此时反应物的浓度都不为0,有可能,故③正确;④Y2为0.6molL-1,需要消耗0.2mol/L的Z2 ,此时生成物Z的浓度0,不可能,故④错误;答案选B。
molX2,由于X2为0.1molL-1,有可能,故②正确;③Z2为0.3molL-1,需要消耗0.05molL-1X2、0.15mol/L的Y2,此时反应物的浓度都不为0,有可能,故③正确;④Y2为0.6molL-1,需要消耗0.2mol/L的Z2 ,此时生成物Z的浓度0,不可能,故④错误;答案选B。


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
【题目】三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42—可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。

下列叙述正确的是( )
A. 通电后中间隔室的SO42-离子向正极迁移,正极区溶液pH增大
B. 该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C. 负极反应为2H2O 4e– = O2+4H+,负极区溶液pH降低
D. 当电路中通过1mol电子的电量时,会有0.5mol的O2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
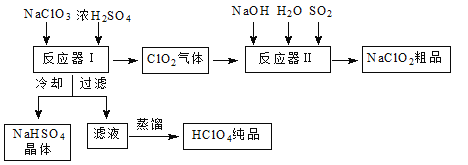
【题目】工业上生产高氯酸时,还同时生产了一种常见的重要含氯消毒剂和漂白剂亚氯酸钠(NaClO2),其工艺流程如下:
已知:①NaHSO4溶解度随温度的升高而增大,适当条件下可结晶析出。
②高氯酸是至今为止人们已知酸中的最强酸,沸点90 ℃。
请回答下列问题:
(1)反应器Ⅰ中发生反应的化学方程式为 ,冷却的目的是 ,能用蒸馏法分离出高氯酸的原因是___________________。
(2)反应器Ⅱ中发生反应的离子方程式为__________________。
(3)通入反应器Ⅱ中的SO2用H2O2代替同样能生成NaClO2,请简要说明双氧水在反应中能代替SO2的原因是_________________________。
(4)Ca(ClO)2、ClO2、NaClO2等含氯化合物都是常用的消毒剂和漂白剂,是因为它们都具有________________,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NOx、SO2是常用的化工原料,含NOx、SO2的烟气大量排放能造成严重的大气污染。
(1)含NH3、NOx、SO2的烟气在大气中相互作用,产生的雾霾颗粒中有多种无机盐,其中无机铵盐主要是_____________(填化学式,只写两种)。
(2)SO2催化氧化反应2SO2(g)+O2(g)![]() 2SO3(g)的能量与反应进程如图所示:
2SO3(g)的能量与反应进程如图所示:

①该反应的正反应为____热(填“放”或“吸”)反应。
②若该反应在恒温恒容密闭容器中进行,能说明该 反应已达到化学平衡状态的是____(填标号)。
A.SO2的v(正)=v(逆)
B.混合气体中同时存在SO2、O2、SO3
C.容器内混合气体密度不随时间而变化
D.容器内混合气体总压强不再随时间而变化
(3)Wang c H等研究发现用Fe2O3/CeO2作催化剂,可用乙烯脱除烟气中SO2并回收单质硫。反应原理为:CH2=CH2+3SO2![]() 3S+2CO2+2H2O。某兴趣小组同学设计实验验证该反应并检验产物中的CO2,实验装置(夹持装置已略)如图所示:
3S+2CO2+2H2O。某兴趣小组同学设计实验验证该反应并检验产物中的CO2,实验装置(夹持装置已略)如图所示:
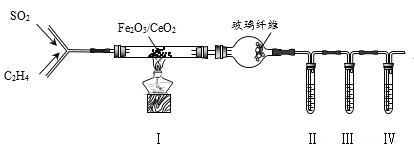
①实验中所需SO2可由Cu与浓硫酸反应制取,该反应的化学方程式为________。
②已知:酸性KMnO4可将CH2=CH2氧化为CO2;装置Ⅱ、Ⅲ中试剂均足量;装置(Ⅰ)的尾气中还含有未反应的SO2和CH2=CH2。检验CO2时,Ⅱ、Ⅲ、Ⅳ中盛放的试剂依次可以是_____(填标号)。
A.酸性KMnO4溶液、品红溶液、澄清石灰水
B.NaOH溶液、酸性KMnO4溶液、澄清石灰水
C.Br2的H2O溶液、品红溶液、澄清石灰水
D.Br2的CCl4溶液、酸性KMnO4溶液、澄清石灰水
(4)取用氨水脱除烟气中SO2得到的副产品[只含(NH4)2SO4和NH4HSO4] 3.875g,与足量NaOH混合后加热充分反应,共收集到氨气1.232L(已折合为标准状况),则该副产品中(NH4)2SO4和NH4HSO4的物质的量之比n[(NH4)2SO4]∶n(NH4HSO4)=______(写出计算结果即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaN3是一种易溶于水(NaN3=Na++N3-)的白色固体,可用于有机合成和汽车安全气囊的产气药等。钠法(液氨法)制备NaN3的工艺流程如下:

(1)钠元素位于周期表第______周期______族。
(2)NaNH2中氮元素的化合价为_______;Na+的结构示意图为_____。
(3)NaOH的电子式为______。
(4)反应NH4NO3![]() N2O↑+2H2O↑中,每生成1molN2O转移电子数为_____个。
N2O↑+2H2O↑中,每生成1molN2O转移电子数为_____个。
(5)反应①的化学方程式为______。
(6)销毁NaN3可用NaClO溶液,该销毁反应的离子方程式为______(N3-被氧化为N2)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于C60、H3、O2-、N5+等微粒的叙述错误的是
A. 碳、氢、氧、氮元素各含有不同核素
B. H3与H2化学性质相同,互为同位素
C. C60与N5+中都含有共价键
D. KO2属于含有共价键的离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸铵(NH4ClO4)常作火箭发射的推进剂,在400℃时开始分解,产物为N2、Cl2、O2、H2O,用以下装置进行NH4ClO4分解实验。下列有关叙述正确的是

A. 高氯酸铵分解产生的Cl2、N2、O2都可用排空气法收集
B. 可按①③②④的连接顺序制得干燥纯净的N2
C. 1mol NH4ClO4分解,标准状况下收集到气体体积为44.8L
D. 装置①也可用于实验室加热NH4Cl或NH4NO3制备NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图表示反应N2(g)+3H2(g)![]() 2NH3(g); ΔH=-92.2kJ/mol。 在某段时间t0~ t6中反应速率与反应过程的曲线图,则氨的百分含量最高的一段时间是 ( )
2NH3(g); ΔH=-92.2kJ/mol。 在某段时间t0~ t6中反应速率与反应过程的曲线图,则氨的百分含量最高的一段时间是 ( )

A、t0—t1 B t2—t3 C t3—t4 D t5—t6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】500℃条件下,在恒容密闭容器中,充入1molNO2存在如下平2NO2(g)![]() N2O4(g) ,平衡后,向容器内再充入1molNO2,下列说法不正确的
N2O4(g) ,平衡后,向容器内再充入1molNO2,下列说法不正确的
A. 平衡向正反应方向移动 B. 平衡常数K增大
C. NO2的转化率变大 D. 容器内气体颜色先变深后变浅,最后比原来还要深
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com