
【题目】四种短周期元素X、Y、Z、W在周期表中的位置如图所示,其中Z元素的最外层电子数是内层电子总数的1/2。下列说法不正确的是
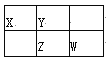
A. Z元素位于周期表的第3周期第VA族
B. X与W形成共价化合物XW2, X的原子半径比Y小
C. Y元素的气态氢化物的热稳定性比Z的高
D. X、W元素的最高价氧化物对应水化物的酸性:W强于X
科目:高中化学 来源: 题型:
【题目】同学们在实验室里用不同的方法分别制取Cu(NO3)2,并在此基础上探究Cu(NO3)2的化学性质。
(1)甲组同学直接用铜屑与稀硝酸反应制取Cu(NO3)2,反应的化学方程式是_____________。
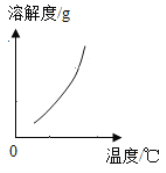
(2)乙组同学查阅了硝酸铜晶体的溶解度曲线(右图),据此设计了以下实验方案,先将铜粉在空气中充分灼烧,再将灼烧后的物质与适量稀HNO3反应,欲从反应后的溶液中得到Cu(NO3)2晶体,依次进行的操作是:蒸发浓缩、____________、过滤、洗涤、干燥。乙组同学认为此方案优于甲组的方案,理由之一是__________________________。
(3)丙组同学用Cu(NO3)2晶体,探究其热稳定性,实验装置如下所示。(夹持装置和加热仪器未画出)

①充分加热Cu(NO3)2晶体一段时间后,观察到U形管中气体变为红棕色,红棕色气体是____________。
②集气瓶最终被水充满,无气体剩余,则晶体分解的生成的气体还有________。
③欲证明试管中残留的黑色粉末是CuO[假设Cu(NO3)2晶体已全部分解],实验方案是 _________。
④由该实验可得出的结论是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将51.2gCu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.8mol,这些气体恰好能被500mL2mol/LNaOH溶液完全吸收,生成NaNO3和NaNO2的混合溶液,其中生成的NaNO3的物质的量为( )
已知NO+NO2+2NaOH=2NaNO2+H2O,2NO2+2NaOH= NaNO3+NaNO2+H2O,
A. 0.2mol B. 0.4mol C. 0.6mol D. 0.8mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按要求填空(化学方程式需注明反应条件):
(1) 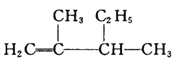 的系统名法名称是___________。
的系统名法名称是___________。
(2)反-2-丁烯的结构简式___________ 。
(3)分子式为C8H11N的有机物,含有苯环和—NH2结构的同分异构体有_________种。
(4)乙酸乙酯在酸性条件下水解的化学方程式____________ 。
(5)苯乙烯和1,3-丁二烯在一定条件下共聚合成丁苯橡胶的化学方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由核电荷数1~18的某些元素组成的单质 A、B、C和甲、乙、丙、丁、戊五种化合物有下图所示的转换关系,A是地壳中含量最多的金属元素。 请回答下列问题:
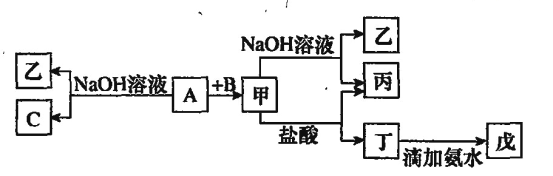
(1)写出下列物质的化学式:乙__________、丁__________、戊__________.
(2)写出甲物质在工业上的一种主要用途:__________。
(3)写出甲→乙+丙反应的离子方程式:__________。
(4)A→乙+C反应的化学方程式:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型的电池,总反应为: 3Zn+2FeO42-+8H2O=2Fe(OH)3↓+3Zn(OH)2↓+4OH—,其工作原理如图所示。下列说法不正确的是
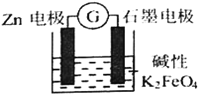
A. Zn极是负极,发生氧化反应
B. 随着反应的进行,溶液的pH增大
C. 电子由Zn极流出到石墨电极,再经过溶液回到Zn极,形成回路
D. 石墨电极上发生的反应为:FeO42—+3e—+4H2O=Fe(OH)3↓+5OH—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质可以实现一步转化的是( )
A. N2→NO2→HNO3→NH4ClB. Al→Al2O3→Al(OH)3→AlCl3
C. Cu→CuCl2→Cu(OH)2→CuOD. Si→SiO2→H2SiO3→NaSiO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学平衡常数K的说法中,正确的是
A. K的大小与起始浓度有关
B. 温度越高,K值越大
C. K值越大,反应正向进行的程度越大
D. K值越大,反应正向进行的程度越小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为了探究常温下某非金属氧化物形成的未知气体的成分,将气体通入澄清石灰水,发现澄清石灰水变浑浊,持续通入发现浑浊又变澄清,由此该小组成员对气体的成分提出猜想。
[提出猜想]
猜想1:该气体为CO2;
猜想2:该气体为SO2;
猜想3:_________________________________________。
为了验证猜想,该小组设计实验加以探究:
[实验探究]该小组同学按如图所示装置,将气体从a端通入,则
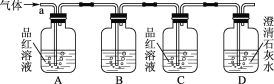
(1)B中应该装下列________试剂(填编号)。
A.NaCl溶液 B.酸性KMnO4溶液 C.盐酸 D.澄清石灰水
(2)A中品红溶液的作用是____________________________________。
(3)D中澄清石灰水的作用是________________________________________。
通过该实验,该小组同学观察到以下三个实验现象:①A中品红溶液褪色;②C中品红溶液不褪色;③D中澄清石灰水变浑浊,由上述现象该小组同学确认该气体的成分为________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com