
| A. | 法国化学家维勒首次提出有机化学的概念;德国化学家贝采里乌斯由氰酸铵合成了尿素,首次打破了有机物和无机物的界限 | |
| B. | 李比希用燃烧法来测定有机化合物中碳氢元素质量分数 | |
| C. | 用核磁共振氢谱和红外光谱法可以区别乙醇和二甲醚(CH3OCH3) | |
| D. | 用“同位素示踪法”是研究有机化学反应历程的手段之一 |
分析 A、贝采里乌斯被称为“有机化学之父”,提出了有机化学概念,法国化学家维勒由氰酸铵合成了尿素,首次打破了有机物和无机物的界;
B、化学家李比希,他创立了有机化学,.改进了有机分析的若干方法;
C、核磁共振氢谱区别不同环境的氢;
D、“同位素示踪法”可以追踪原子的去向.
解答 解:A、贝采里乌斯被称为“有机化学之父”,提出了有机化学概念,法国化学家维勒由氰酸铵合成了尿素,首次打破了有机物和无机物的界限,故A错误;
B、化学家李比希,作过大量的有机化合物的准确分析,改进了有机分析的若干方法,如用燃烧法来测定有机化合物中碳氢元素质量分数,故B正确;
C、乙醇有3种不同环境的氢,而二甲醚(CH3OCH3)只有一种,可以用核磁共振氢谱区分,故C正确;
D、“同位素示踪法”可以追踪原子的去向,了解有机化学反应历程,故D正确;
故选A.
点评 本题考查了化学史、化学结构和反应历程等物理探测手段、蛋白质的结构等性质,均属于记忆的知识,题目难度不大,注意基础知识的积累.


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:解答题
 (1)炒过菜的铁锅未及时洗净,不久便会因腐蚀而出现红褐色锈斑.请回答:铁锅的锈蚀是吸氧腐蚀(填“析氢”或“吸氧”).写出铁锅腐蚀正极的电极反应式:2H2O+O2+4e-=4OH-
(1)炒过菜的铁锅未及时洗净,不久便会因腐蚀而出现红褐色锈斑.请回答:铁锅的锈蚀是吸氧腐蚀(填“析氢”或“吸氧”).写出铁锅腐蚀正极的电极反应式:2H2O+O2+4e-=4OH-查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5.6 L | B. | 11.2 L | C. | 22.4 L | D. | 33.6 L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨是极性分子,其在水中的溶解度很大 | |
| B. | DNA中的碱基互补配对是通过氢键来实现的 | |
| C. | 气体单质中,一定有σ键,可能有π键 | |
| D. | 元素“氦、铷、铯”等是用光谱分析方法发现的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入20g 固体NaOH,搅拌、溶解 | |
| B. | 将溶液加热浓缩至0.6 L | |
| C. | 加入10mol/L的NaOH溶液0.1 L,再稀释至1.5 L | |
| D. | 加入1 L 1.5 mol/L的NaOH溶液混合均匀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4 L | B. | 2.24 L | C. | 44.8 L | D. | 4.48 L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 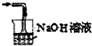 用装置吸收二氧化硫气体 | |
| B. |  用装置除去氯气中的氯化氢杂质 | |
| C. |  用装置可以对硫化氢气体进行尾气处理 | |
| D. |  用装置制备并收集氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
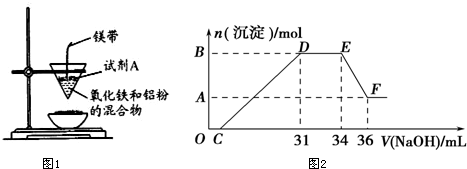
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
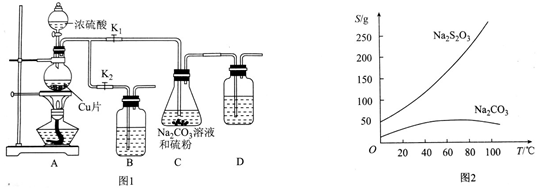
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com