
在下图所示的原电池中,正极发生的反应是
A.2H++2e― H2↑ H2↑ | B.Cu–2e― Cu2+ Cu2+ |
C.Cu2++2e― Cu Cu | D.Zn–2e― Zn2+ Zn2+ |
科目:高中化学 来源: 题型:实验题
滴定实验是化学学科中重要的定量实验。
请回答下列问题:
(1)酸碱中和滴定——用标准盐酸滴定未知浓度的NaOH溶液,下列操作造成测定结果偏高的是 (填选项字母)
A.滴定终点读数时,俯视滴定管刻度,其他操作正确。
B.盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗
C.酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗
D.滴定前,滴定管尖嘴有气泡,滴定后气泡消失
(2)氧化还原滴定——取草酸溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1mol·L-1的高锰酸钾溶液滴定,发生的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。表格中记录了实验数据:
| 滴定次数 | 待测液体积 (mL) | 标准KMnO4溶液体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 25.00 | 0.50 | 20.40 |
| 第二次 | 25.00 | 3.00 | 23.00 |
| 第三次 | 25.00 | 4.00 | 24.10 |
| 难溶物 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
| 颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
| Ksp | 1.77×10-10 | 5.35×10-13 | 1.21×10-16 | 1.12×10-12 | 1.0×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
如图,将纯Fe棒和石墨棒插入1 L饱和NaCl溶液中。下列说法正确的是( )
| A.M接负极,N接正极,当两极产生气体总量为22.4 L(标准状况)时,生成1 mol NaOH |
| B.M接负极,N接正极,在溶液中滴人酚酞试液,C电极周围溶液变红 |
| C.M接负极,N接正极,若把烧杯中溶液换成1 L CuSO4溶液,反应一段时间后,烧杯中产生蓝色沉淀 |
| D.M接电源正极,N接电源负极,将C电极换成Cu电极,电解质溶液换成CuSO4溶液,则可实现在铁上镀铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
钢铁发生吸氧腐蚀时,正极发生反应的电极反应式为
| A.Fe-2e-=Fe2+ | B.Fe-3e-=Fe3+ | C.O2+2H2O+4e-=4OH- | D.2H++2e-= H2 ↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在25ºC时,将两根铂电极插入一定量的硫酸钠饱和溶液中进行电解,当电路中有a mol电子转移时,溶液中析出mg Na2SO4 ·10 H2 O晶体。若温度不变,在剩余溶液中溶质的质量分数为
A.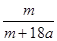 ×100% ×100% | B. ×100% ×100% |
C. ×100% ×100% | D.71m/161(m+9a) ×100% |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某原电池装置如下图所示。下列有关叙述中,正确的是
A. 作正极,发生氧化反应 作正极,发生氧化反应 | B.工作一段时间后,两烧杯中溶解 均不变 均不变 |
C.负极反应: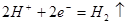 | D.工作一段时间后,NaCl溶液中c(Cl-)增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
一种氢氧燃料电池用30%KOH溶液为电解质溶液,有关这种电池的说法中错误的是
| A.H2在负极发生氧化反应 | B.供电时的总反应为:2H2 + O2 = 2H2O |
| C.产物为无污染的水,属于环境友好电池 | D.负极反应为:H2 - 2e- = 2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
观察下列几个装置示意图,有关叙述正确的是
| A.装置①中阳极上析出红色固体 |
| B.装置②的待镀铁制品应与电源负极相连 |
| C.装置③中外电路电子由b极流向a极 |
| D.装置④的离子交换膜允许阳离子、阴离子、水分子自由通过 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
 从H+、K+、Cu2+、Cl-、SO中选取适当的离子组成符合下列情况的电解质。惰性电解,电 解质的物质的量减少,水的物质的量也减少,pH下降,则电解质的化学式为( )
从H+、K+、Cu2+、Cl-、SO中选取适当的离子组成符合下列情况的电解质。惰性电解,电 解质的物质的量减少,水的物质的量也减少,pH下降,则电解质的化学式为( )
| A.HCl | B.K2SO4 | C.CuSO4 | D.KCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com