
【题目】MnO2和Zn是制造普通干电池的重要原料,现用软锰矿(主要成分为MnO2)和闪锌矿(主要成分为ZnS)制备MnO2和Zn的工艺流程如图:
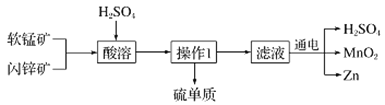
下列说法不正确的是( )
A.干电池是一种将化学能转变为电能的装置
B.酸溶时,ZnS作还原剂,每析出12.8gS沉淀,共转移0.8mol电子
C.通电电解时MnO2在阳极处生成,电极反应为:Mn2+-2e-+2H2O═MnO2+4H+
D.原料硫酸可以循环使用,且可用盐酸代替硫酸进行酸溶
 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源: 题型:
【题目】能源危机是当前全球性的问题,“开源节流”是应对能源危机的重要举措。
(1)下列做法有助于能源“开源节流”的是____(填序号)。
a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
b.大力开采煤、石油和天然气以满足人们日益增长的能源需求
c.开发太阳能、水能、风能、地热能等新能源,减少使用煤、石油等化石燃料
d.减少资源消耗,增加资源的重复使用、资源的循环再生
(2)科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO+2CO![]() 2CO2+N2△H<0。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2△H<0。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
C(NO)(×10-4mol·L-1) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
C(CO)(×10-3mol·L-1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
前2s内的平均反应速率v(N2)=______;达到平衡时,NO的转化率为_____,气相中NO所占的体积分数为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正常人心脏在一次搏动中泵出血液约80 mL,正常人血压(可看作心脏压送血液的压强)平均值为1.6×104Pa,心跳每分钟约70次。设人类消耗体内的葡萄糖产生的热量最高可有80%(睡眠时)用来维持心脏的跳动,葡萄糖与氧气反应产生热量的化学方程式为:C6H12O6(s)+6O2(g)―→6CO2(g)+6H2O(g)(放出热量2804 kJ)
(1)心脏工作的平均功率约为______________;
(2)由于心脏跳动每天需消耗葡萄糖的质量是____________________________;
(3)维持生命每天需消耗氧气的体积是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“神十搭载的长征F改进型火箭推进剂之一为无色气体N2O4,N2O4与NO2转换的热化学方程式为:N2O4(g)![]() 2NO2(g) △H=+24.4KJ/mol。
2NO2(g) △H=+24.4KJ/mol。
(1)将一定量N2O4投入固定容积的真空容器中,下述现象能说明反应达到平衡的是________。
a.v正(N2O4)=2v逆(NO2) b.体系颜色不变c.气体平均相对分子质量不变 d.气体密度不变
达到平衡后,保持体积不变升高温度,再次到达平衡时,则混合气体颜色____(填“变深”、“变浅”或“不变”),判断理由________。
(2)T℃时,向1L恒容密闭容器中投入1molCH4和1molH2O(g),发生反应:CH4(g)+H2O(g) ![]() CO(g)+3H2(g),经过3min,反应达到平衡。已知平衡时,c(CH4)=0.5mol/L则0~3min内,该反应的平均反应速率v(H2)=___。
CO(g)+3H2(g),经过3min,反应达到平衡。已知平衡时,c(CH4)=0.5mol/L则0~3min内,该反应的平均反应速率v(H2)=___。
(3)在一定条件下用CO和H2可以制得甲醇,CH3OH和CO的燃烧热为别725.8 kJ/mol,283.0 kJ/mol,1 mol液态水变成气态水吸热44.0 kJ,写出甲醇不完全燃烧生成一氧化碳和气态水的热化学方程式:____。
(4)工业上用CO与H2在催化剂作用下合成CH3OH,其反应为:CO(g)+2H2(g) ![]() CH3OH(g)。按n(CO) : n(H2)=1 : 2向密闭容器中充入反应物,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。则P1_____P2(填“<”“>”或“=”)
CH3OH(g)。按n(CO) : n(H2)=1 : 2向密闭容器中充入反应物,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。则P1_____P2(填“<”“>”或“=”)

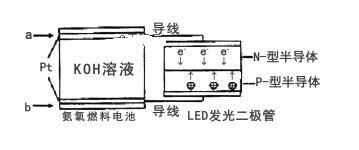
(5)一种氨燃料电池,使用的电解质溶液是2mol/L的KOH溶液。电池反应为:4NH3+3O2=2N2+6H2O;请写出通入a气体一极的电极反应式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,有下列物质:①8gCH4、②6.02×1023个HCl分子、③2mol O2。按由小到大的顺序填写下列空白(填写序号):
(1)摩尔质量____________________。
(2)物质的量____________________。
(3)分子数目____________________。
(4)原子数目____________________。
(5)质量____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物的结构简式为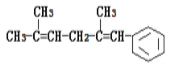 ,判断下列说法中不正确的是( )
,判断下列说法中不正确的是( )
A.它可以使酸性KMnO4溶液褪色
B.它可发生取代反应、加成反应、加聚反应、氧化反应
C.1mol该有机物燃烧消耗氧气为18.5mol
D.它与氢气发生加成反应,最多可以消耗4mol氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)烃A的结构简式为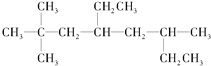 ,用系统命名法命名烃A:__。
,用系统命名法命名烃A:__。
(2)某烃的分子式为C5H12,核磁共振氢谱图中显示4个峰,则该烃的一氯代物有__种,该烃的结构简式为__。
(3)麻黄素又称黄碱,是我国特定中药材麻黄中所含有的一种生物碱。经科学家研究发现其结构为: ,下列各物质:
,下列各物质:
A.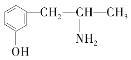 B.
B.![]() C.
C. D.
D. E.
E.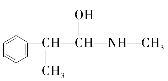
与麻黄素互为同分异构体的是__(填字母,下同),互为同系物的是__(填字母)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乳酸是天然的酸味调节剂,乳酸的结构简式为![]() ,下列关于乳酸的说法正确的是( )
,下列关于乳酸的说法正确的是( )
A.含有醛基官能团
B.1mol乳酸可以和2molNaOH 溶液恰好完全反应
C.1mol乳酸和碳酸氢钠溶液充分反应生成2molCO2
D.乳酸和乙酸都显酸性,但它们在浓硫酸作用下经加热可以发生化学反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】麻黄素M是拟交感神经药。合成M的一种路线如图所示:
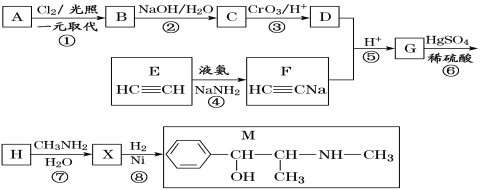
已知:I.R—CH2OH![]() RCHO
RCHO
II.R1-CHO+R-C≡CNa![]()
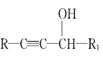
IV.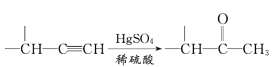
V.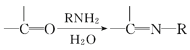
请回答下列问题:
(1)D的名称是_______;G中含氧官能团的名称是_______。
(2)反应②的反应类型为_______;A的结构简式为_______。
(3)写出反应⑦的化学方程式:______________________________。
(4)X分子中最多有_______个碳原子共平面。
(5)在H的同分异构体中,同时能发生水解反应和银镜反应的芳香族化合物中,核磁共振氢谱上有4组峰,且峰面积之比为1∶1∶2∶6的有机物的结构简式为_________________。
(6)已知:![]() 仿照上述流程,设计以苯、乙醛为主要原料合成某药物中间体
仿照上述流程,设计以苯、乙醛为主要原料合成某药物中间体![]() 的路线________________。
的路线________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com