
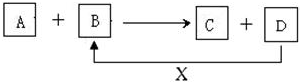
分析 (1)A为金属铝,B为氧化铁,考虑铝热反应,反应可以生成氧化铝与铁,铁与氧气反应生成Fe3O4,符合转化;
(2)A为两性氢氧化物,A为Al(OH)3,B为NaOH溶液,反应生成偏铝酸钠和水;
(3)A为金属单质,B、C、D都是化合物,A与B发生的反应常用于制作印刷电路板,则A为Cu,B含有Fe3+,B为FeCl3,反应生成Cu2+与Fe2+,Fe2+与Cl2反应生成FeCl3,符合转化;
(4)A、B、C为化合物,D、X为单质,由转化关系可知,单质D、X化合生成B,B中含有X元素,根据元素守恒可以,C中一定含有X元素.
解答 解:(1)A为金属铝,B为氧化铁,发生铝热反应,生成氧化铝与铁,可以用来焊接钢轨、炼铁等,
故答案为:焊接钢轨、炼铁等;
(2)A为两性氢氧化物,A为Al(OH)3,B为NaOH溶液,反应生成偏铝酸钠和水,反应离子方程式为Al(OH)3+OH-=AlO2-+2H2O,故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(3)A为金属单质,B、C、D都是化合物,A与B发生的反应常用于制作印刷电路板,则A为Cu,B含有Fe3+,B为FeCl3,反应生成Cu2+与Fe2+,离子方程式为:Cu+2Fe3+═Cu2++2Fe2+,
故答案为:Cu+2Fe3+═Cu2++2Fe2+;
(4)A、B、C为化合物,D、X为单质,由转化关系可知,单质D、X化合生成B,B中含有X元素,根据元素守恒可以,C中一定含有X元素,故答案为:B、C.
点评 本题是无机框图推断题,考查物质推断与性质,难度较大,掌握元素化合物的性质是解题的关键,需要学生熟练掌握元素化合物知识.


科目:高中化学 来源: 题型:解答题
 某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应,其中①②③属于同种反应类型.根据如图回答下列问题:
某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应,其中①②③属于同种反应类型.根据如图回答下列问题: (填电子式),B
(填电子式),B (填结构式),E
(填结构式),E (填结构简式).
(填结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 尽管NO2能与水反应生成硝酸,但NO2不属于酸性氧化物 | |
| B. | Na2O2粉末加入到FeSO4溶液中,产生白色沉淀,并放出大量气泡 | |
| C. | 氨气和氯化氢气体混合后生成的NH4Cl是离子化合物,因此该反应为离子反应 | |
| D. | 往酸性KMnO4溶液中通入SO2验证SO2的漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 HSO3-+OH-
HSO3-+OH-| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置. | |
| 步骤2:取适量步骤1所得溶液于试管中,加入少量的酸性高锰酸钾溶液. | 若溶液褪色,说明其有Na2SO3 若溶液不褪色,说明其中没有Na2SO3 |
| 步骤3:再取适量步骤1所得溶液于另一试管中,先加入足量的稀盐酸,再滴加氯化钡溶液. | 如果有白色沉淀生成,则说明其中有Na2SO4,已经变质. 如果没有白色沉淀生成,则说明其中没有Na2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,pH=7的NH4Cl与NH3•H2O混合溶液:c(H+)=c(OH-)=c(NH4+)=c(Cl-) | |
| B. | 25℃时,向10mL pH=12的NaOH溶液中滴加等体积pH=2的CH3COOH溶液;c(CH3COO-)>c(Na+)>c(OH-)>c(H+) | |
| C. | 0.1mol•L-1的CH3COONa溶液与0.1mol•L-1的CaCl2溶液等体积混合:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-) | |
| D. | 浓度均为0.1mol•L-1的①(NH4)2CO3、②(NH4)2SO4、③(NH4)2Fe(SO4)2溶液中,c(NH4+)的大小顺序为③>②>① |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| ① | ② | ③ | ④ | |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| A. | ①、②中分别加入适量的氯化铵晶体后,两溶液的pH均减小 | |
| B. | 分别加水稀释10倍,四种溶液的pH ①>②>④>③ | |
| C. | VaL④与VbL②溶液混合后,若混合后溶液pH=4,则Va:Vb=9:11 | |
| D. | ①、④两溶液等体积混合,所得溶液中c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com