
�������п�����������Ҫ��Ⱦ��Ϊ�����������pm2.5��SO2��NOx�ȣ�����Ҫ��ԴΪȼú�ͻ�����β���ŷŵȡ�
��1��ijͬѧΪ��������������ɷݣ�������������ˮ�����Ƴɴ������������ʵ�鼰ʵ���������£�
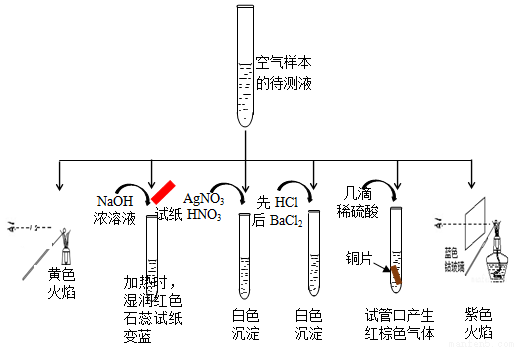
�� ��ʵ����ȷ�ϴ��ڵ��������� ��
�� ��ʵ�������������NO3���������ǣ��û�ѧ����ʽ���ͣ� ��
�� ���ݸ�ʵ���ܷ�ȷ�������к���SO32���� (��ܡ���) ����Ҫȷ��SO32���������ʵ��ҩƷ������ ��
��2��ȼú��Ϊ����SO2���ŷţ��ɲ�ȡ�Ĵ�ʩ�ǣ�
�� ϴ�Ӻ�SO2���������������ʿ���ϴ�Ӽ�����______��
a��ŨNH3?H2O b��NaHCO3 c��FeCl3 d��NaHSO3
�� ��úת��Ϊ�������ȼ�ϣ�������ͼ��ʾ��

��֪����Ӧ������1molCO(g)�ķ�Ӧ�ȡ�H= -110.5KJ/mol��Ӧ������1molH2O(g)�ķ�Ӧ�ȡ�H=  -241.6KJ/mol��̿��ˮ������Ӧ���Ȼ�ѧ����ʽ��________________��
-241.6KJ/mol��̿��ˮ������Ӧ���Ȼ�ѧ����ʽ��________________��
��3�� ����β������ϵͳ�ɽ�CO��NOת���������ʣ��仯ѧ��Ӧ����ʽ��________________
��4��Ϊ��CO��NOת��Ϊ�����ʣ�ijͬѧ�������ͼװ�á�

�ٵ缫a��________����
�ڼĻ�ѧʽ�� ��
�۵缫b�ĵ缫��Ӧʽ��____________��
 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016�������������ʦ���и�����ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ��ƶ���
A��H��Ϊ������Ԫ�أ�A��F��Ԫ�����ڱ��е����λ����ͼ��ʾ��G����������Ԫ�ز���ͬһ���ڣ�H�Ƕ�������ԭ�Ӱ뾶��������Ԫ�ء���B��G��ɵ���̬�������ˮ��Һ�ʼ��ԡ�
A | B | C | |
D | E | F |
��ش��������⣺
��1��д���ĵ���ʽ ��ʵ������ȡ����Ļ�ѧ����ʽΪ ��
��2��B��C��G������Ϊ1:1:5�γɵĻ�����Ļ�ѧ������Ϊ ��
A�����Ӽ� B�� ���Լ� C�� �Ǽ��Լ�
��3�����õ���ʽ��ʾAE2���γɹ��� ��
��4�������ӷ��ű�ʾC��E��F��H�������ӵİ뾶�ɴ�С��˳�� ��
��5����һ�����ӷ���ʽ����A��D�ǽ�����ǿ��ԭ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016����������ɽ����ѧ������ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
ij��ҵ��ˮ�п��ܺ������¼����������ӣ�
������ | Fe3+��Al3+��Fe2+��Ba2+��Na+ |
������ | Cl����CO32����NO3����SO42����SiO32�� |
�ֶԸ÷�ˮ��Ʒ���������о���
��ȡ�����ķ�ˮ���Թ��У��۲���ɫ������ζ������ͨˮ���Բ�ͬ��
�����Թ��еμ�Ũ���ᣬ����������ɫ�������ɣ�����������������Ϊ����ɫ��
������II���õ���Һ�м���BaCl2��Һ���а�ɫ�������ɣ�
��������II���õ���Һ�м��������NaOH��Һ���к��ɫ�������ɡ����˺���������Һ��ͨ�������CO2���壬�а�ɫ��״�������ɡ�
��������ʵ�飬�ش��������⣺
��1���÷�ˮ��һ�����е��������� ��һ�������е��������� ��
��2��д��IV��������Һ��ͨ�������CO2�������ɰ�ɫ��״���������ӷ���ʽ��ֻд��һ������ ��
��3��������ˮ�е���Ԫ����ȫת����Fe3+����ʱ���c(Fe3+����1��0��10��2mol��L��1��Ҫ�뽫��ת��ΪFe(OH��3��������ȥ����Ӧ������ҺpHԼΪ ������֪������Fe(OH��3��Ksp��1��0��10��38��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016�㽭����Чʵ��ѧ�߶������п��Ի�ѧ�Ծ����������棩 ���ͣ�ѡ����
�����£��й�����������Һ��������ȷ���ǣ�������Һ��ϵ�����仯��
�� | �� | �� | �� | |
pH | 12 | 12 | 2 | 2 |
��Һ | ��ˮ | ����������Һ | ���� | ���� |
A���ڢ١����зֱ�����Ȼ�茶��壬����Һ��pHֵ������
B���ֱ�����Ģٺ͢ڼ�ˮϡ��100����������Һ��pH����>��
C���Ѣ١�������Һ�������Ϻ�������Һ������
D������Һ�ں���Һ�۵������ϣ���Ϻ�������ҺpH=7
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016���Ļ�����������һ�и�һ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
������Һ�е�Cl�� ��Ŀ��25mL 0��1 mol��L��1��AlCl3��Һ��Cl����Ŀ��ȵ���
A��50mL 0��15mol��L��1��BaCl2��Һ
B��50mL 0��3mol��L��1��NaCl��Һ
C��25 mL0��3mol��L��1��FeCl3��Һ
D��75 mL 0��1mol��L��1��KCl��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�챱���г�����������ѧ������ͳ����ѧ�Ծ��������棩 ���ͣ�ѡ����
����ͼʾ���й��Ŵ����������������漰����ѧ�仯����
A����ʳ��� | B����ĥͭ�� | C��˿��֯�� | D���� |
|
|
|
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ�����и�����ѧ�ڵ�һ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪��ԭ��Cl-< Br-< Fe2+<I-��������Cl2>Br2>Fe3+> I2��������˵����ȷ����
A���ں���Br��Fe2+��I-����Һ����ֻ����I-��������Br��Fe2+������FeBr3���Լ�
B����FeI2��Һ��ͨ������Cl2����Ӧ�����ӷ���ʽΪ��2Fe2++ Cl2=2Fe3++ 2C1-
C����FeBr2��Һ��ͨ������Cl2����Ӧ�����ӷ���ʽΪ��2Fe2+ +2Br-+2Cl2=2Fe3++ Br2+4Cl-
D����FeCl2��Һ�еμ�������ˮ���ܷ�����Ӧ��2Fe2++ I2=2Fe3++ 2I-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʡ��̨�и�����ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
ij����С��̽�����÷ϺϽ�(������������ͭ)��ĩ��ȡ�������Ȼ�����Һ���̷�����͵������壬��ʵ�鷽�����£�
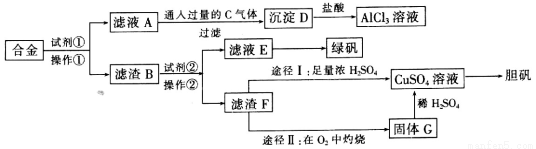
�Իش��������⣺
��1�������Լ��١��ڷֱ���___________��____________��
��2�������ٵ�����Ϊ__________�����õ�����������̨����Ȧ���ձ�������Ҫ����Ʒ��______________��
��3��д��A��D��Ӧ���ӷ���ʽ____________��
��4����ҺE������Ũ����_________���̷����壬Ȼ���پ����ˡ�ϴ�ӡ����T�ó�Ʒ��ϴ��ʱ�������Լ����ѡ��___________��
a��ϡH2SO4 b������ˮ c���ƾ� d��NaOH��Һ
��5��������F��CuSO4��Һ��;��I��;�������֣�����Ϊ���;����________��������_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�챱���к�����������ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£����и����������ƶ���Һ��һ���ܴ����������
A����pH =12��Һ�У�Na+ ��Ca2+ ��HCO3 ? ��ClO?
B������ʹʯ�������Һ�У�Mg2+��K+��Br?��SO4 2 ?
C����0.1mol ��L?1��NaHCO3 ��Һ�У�K+��Al3+��I?��Cl?
D������Al ��Ӧ�ܷų�H2 ����Һ�У� Fe2+ ��K+ ��NO3? ��SO4 2 ?
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com