
����Ŀ������ָ����Ӧ�����ӷ���ʽ��ȷ����(����)
A. ��������ˮ��Cl2+H2O2H++Cl��+ClO��
B. ��FeSO4��Һ�м���H2SO4�ữ��KMnO4��Һ��5Fe2++MnO4��+8H+�T5Fe3++Mn2++4H2O
C. ����������ʯ��ˮ�м���������NaHCO3��Һ��Ca2++OH��+HCO3���TCaCO3��+H2O
D. ��ͭ���缫���NaCl��Һ��2Cl��+2H2O![]() H2��+Cl2��+2OH��
H2��+Cl2��+2OH��
���𰸡�B
��������
A��HClO��������ʣ�д��ѧʽ�����ӷ���ʽΪCl2+H2OH++Cl��+HClO����A����
B������������ԭ��Ӧ���������ӡ������Ӻ�ˮ�����ӷ���ʽΪ5Fe2++MnO4��+8H+�T5Fe3++Mn2++4H2O����B��ȷ��
C�����߷�Ӧ����̼��ơ�̼���ƺ�ˮ�����ӷ���ʽΪCa2++2OH��+2HCO3���TCaCO3��+2H2O+CO32������C����
D��������Cuʧ���ӷ���������Ӧ�����ӷ���ʽΪCu+2H2O![]() Cu(OH)2��+H2������D����
Cu(OH)2��+H2������D����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2001����ΰ��Ļ�ѧ�ҡ�1954��ŵ������ѧ�������������Ļ�ѧ�ṹ��ʦ��20���͵Ŀ�ѧ�ֽܱ���(L.Pauling)���ڵĵ���100���ꡣ1994����λ����л�������Ǵ����İ칫�ң�����������һ��ڰ壬���������ģ�����һ���ṹʽ��ͼ��ʾ������Ϊʲô������ṹʽ�����ܺϳ�������ʲô���ʣ����ö�֪�����DZ����������˵�һ���գ�Ҳ��������Զ������գ�Ҳ���г�һ������ܽ�������ܽ����Σ��������ȶ�����ṹ��һ���˽⡣

(1)���ķ���ʽ��__________________________________________________________��
(2)��������ԭ���Ƿ���ܴ���ͬһ��ƽ���ϣ�________(����ܡ������ܡ�)��
(3)���Ƿ���е�ɣ�________(��ǡ���)��
(4)�÷�����sp�ӻ��ĵ�ԭ����___����sp2�ӻ��ĵ�ԭ����___����sp3�ӻ��ĵ�ԭ����_____����
(5)Ϊʲô�����Ʋ�����ըҩ��______________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Li4Ti5O12��LiFePO4��������ӵ�صĵ缫���ϣ���������������Ҫ�ɷ�ΪFeTiO3������������MgO��SiO2�����ʣ����Ʊ��������������£�
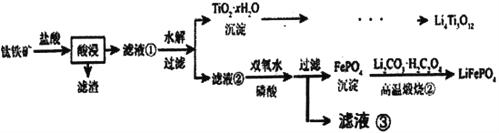
��֪���������������Ҫ��TiOCl42-��ʽ����
FeTiO3+4H++4C1-=Fe2++ TiOCl42-+2H2O
����˵������ȷ����
A. Li2Ti5O15��Ti�Ļ��ϼ�Ϊ+4��������4��������
B. ��Һ���е������ӳ���Fe2+��H+������Mg2+
C. ��Һ����Ҳ����ֱ�Ӽ���������ˮ����˫��ˮ
D. ���������բڡ������У�FeԪ�ر�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���û�ѧ�����ʾ2Na+2H2O�T2NaOH+H2���е��������������ȷ����(����)
A. ������Ϊ8����ԭ�ӣ�88O
B. NaOH�ĵ���ʽ��![]()
C. H2O�Ľṹʽ��![]()
D. Na+�Ľṹʾ��ͼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����Ȼ�ѧ��Ӧ����������ȷ����
A. HCl��NaOH��Ӧ���к��ȡ�H����57.3 kJ��mol1����H2SO4��Ca(OH)2��Ӧ���к��ȡ�H=2��(��57.3)kJ��mol1
B. ����ı�ȼ���Ȧ�H����890.3 kJ��mol1����CH4(g)��2O2(g)��CO2(g)��2H2O(g) ��H����890.3 kJ��mol1
C. ��֪��500�桢30MPa�£�N2(g)��3H2(g)![]() 2NH3(g) ��H����92.4kJ��mol��1����1.5 mol H2������N2�ڴ������³�ַ�Ӧ���ų�����46.2 kJ
2NH3(g) ��H����92.4kJ��mol��1����1.5 mol H2������N2�ڴ������³�ַ�Ӧ���ų�����46.2 kJ
D. CO(g)��ȼ������283.0kJ��mol1����2CO2(g) ===2CO(g)+O2(g)��Ӧ�ġ�H��+566.0 kJ��mol1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾ���Ӧ�������������(����)
A.  ��ʾH2��O2������Ӧ�����е������仯����H2O(g)�TH2(g)+1/2O2(g)�ġ�H����241.8 kJmol��1
��ʾH2��O2������Ӧ�����е������仯����H2O(g)�TH2(g)+1/2O2(g)�ġ�H����241.8 kJmol��1
B.  ��ʾA��B�����ʵ��ܽ�����¶ȱ仯�������T1 KʱA��B�ı�����Һ�ֱ�������T2 Kʱ�����ʵ���������B��A
��ʾA��B�����ʵ��ܽ�����¶ȱ仯�������T1 KʱA��B�ı�����Һ�ֱ�������T2 Kʱ�����ʵ���������B��A
C.  ��ʾþ��������������������������ʱ��ı仯��0��t1��Ӧ���ʼӿ��ԭ������Ǹ÷�ӦΪ���ȷ�Ӧ
��ʾþ��������������������������ʱ��ı仯��0��t1��Ӧ���ʼӿ��ԭ������Ǹ÷�ӦΪ���ȷ�Ӧ
D.  ��ʾ������ϡ��pH��ͬ�������������ʱ��ҺpH�����ˮ����Ĺ�ϵ���������Ϊ���ᣬ��a��Kw����ֵ��b��Ĵ�
��ʾ������ϡ��pH��ͬ�������������ʱ��ҺpH�����ˮ����Ĺ�ϵ���������Ϊ���ᣬ��a��Kw����ֵ��b��Ĵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������(H2C2O4)��һ�ֶ�Ԫ���ᡣ�����£���H2C2O4��Һ����μ���NaOH��Һ�������Һ��lgX[XΪc(HC2O4-)/c(H2C2O4)��c(C2O42-)/c(HC2O4-)]��pH�ı仯��ϵ��ͼ��ʾ������˵��һ����ȷ����(����)

A. ���ʾlgc(HC2O4-)/c(H2C2O4)��pH�ı仯��ϵ
B. pH��1.22����Һ�У�2c(C2O42��)+c(HC2O4��)��c(Na+)
C. 1.22��pH��4.19����Һ�У�c(HC2O4��)��c(C2O42��)��c(H2C2O4)
D. pH��4.19����Һ�У�c(Na+)��3c(HC2O4��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������NaBH4��ZnCl2�������¿�ת��Ϊ��������NaBH4ת��ΪH3BO3��

(1)Zn2+��̬��������Ų�ʽΪ_____��
(2)���״�(![]() )��̼ԭ�ӵ��ӻ��������Ϊ_____��
)��̼ԭ�ӵ��ӻ��������Ϊ_____��
(3)1mol���������(![]() )�����к�����������ĿΪ_____mol��
)�����к�����������ĿΪ_____mol��
(4)��BH4����Ϊ�ȵ������������Ϊ_____(�ѧʽ)��BH4�����ӵĿռ乹��Ϊ(����������)_____��
(5)������һ�ֲ�״�ṹ��ɫ���壬���ڵ�H3BO3����ͨ���������(��ͼ��ʾ)��1molH3BO3��������_____mol�����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʯ�е�һ�֣�����Ҫ�ɷ�Ϊ��������NaAl(Si2O6)��������Cr��Ni��Mn��Mg��Fe��Ԫ�ء��ش��������⣺
(1)Cr3+�����Ų�ʽΪ______________________����̬Siԭ���У�����ռ�ݵ�����ܲ����Ϊ______________________��
(2)�������Ҫ�ɷ�Ϊ�������ƣ�����Ԫ�صĵ�һ�������ɴ�С��˳��___________��
(3)�̵�һ�ֻ�����Ļ�ѧʽΪMn(BH4)2(THF)3��THT�Ľṹ��ʽ��ͼ��ʾ��

��THF��Cԭ�ӵ��ӻ��������Ϊ___________����BH4���Ŀռ乹��Ϊ___________
��NaBH4������ѧ��������_____________
A�����Ӽ� B�����ۼ� C����� D����λ��
(4)MnO���۵�(1660��)��MnS���۵�(1610��)�ߣ�ԭ��______________________��
(5)Ni�����γɶ������������һ��NixO����ľ����ṹΪNaCl�ͣ����ھ���ȱ�ݣ�xΪ0.88���Ҿ�����Ni�Ĵ�����ʽΪNi2+��Ni3+��������N i2+��Ni3+���������Ϊ___________���þ���ľ�������Ϊ428pm�������ܶ�Ϊ___________g��cm��3(NA��ʾ�����ӵ�������ֵ���г�����ʽ����)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com