
【题目】下列烷烃在光照条件下与氯气反应,生成一氯代烃不止一种的是
A.CH4B.CH3CH3C.C3H8D.C(CH3)4
科目:高中化学 来源: 题型:
【题目】下列各组中的离子,因发生氧化还原反应而不能大量共存同一溶液中的是:( )
A. Fe2+、SO42-、Fe3+、Cl- B. S2-、Cu2+、Na+、Cl-
C. H+、SO42-、Cu2+、OH- D. Fe2+、H+、Mg2+、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于晶体的说法一定正确的是( )
A. 在晶体中只要有阳离子就一定有阴离子
B. CaTiO3晶体(如图)中每个Ti4+和12个O2-相紧邻

CaTiO3的晶体结构模型(图中Ca2+、O2-、Ti4+分别位于立方体的体心、面心和顶点)
C. 金属晶体中金属离子电荷数越多,离子半径越小,金属键就越弱
D. 金属晶体的熔点都比分子晶体的熔点高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. “火树银花”中的焰火实质上是金属元素的焰色反应
B. 合成纤维、淀粉,蛋白质和地沟油都是高分子化合物
C. 去皮苹果放在空气久置变黄与纸张变黄原理相似
D. 煤经过气化、液化和干馏等物理变化过程,可以转化为清洁能源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙酮和水杨酸(邻羟基苯甲酸)都是医药工程的重要原料,以其为起点可合成重要的医药中间体4-羟基香豆素。根据以下合成路线,回答问题:

已知:
(1)C中含有的官能团名称为_______________,B→C的反应类型为_____________。
(2)E→F的化学方程式为______________________ 。
(3)F+D→G的化学方程式为_________________________________。
(4)1 mol H最多能与________molNaOH发生反应。
(5)同时满足下列条件的E的同分异构体有_________种,写出其中一种核磁共振氢谱有4组峰的结构简式:____________________。
①能发生银镜反应;②能与FeCl3溶液发生显色反应。
(6)结合题给信息,请设计合理方案,由![]() 合成
合成![]() ,其他无机试剂自选。合
,其他无机试剂自选。合
成路线图示例如下:![]() 。________________________________________。
。________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、Q、R、T是前四周期原子序数依次增大的六种元素,其中X元素形成的气体单质密度最小,Y元素氢化物的水溶液呈碱性,Z、R元素最外层电子数相同且Z的原子序数为R的一半,Q的原子半径在第三周期中最大,T是目前应用最广泛的金属。回答下列问题:
(1)T在周期表中的位置是___________________,其M层上的电子排布式为_______________。
(2)Y、Z、R的第一电离能由大到小的顺序为_________________(用元素符号表示)。
(3)根据等电子体原理,Y2Z分子的结构式为________________。
(4)YZ能被TRZ4溶液吸收生成配合物[T(YZ)(X2Z)5]RZ4,该配合物中含有的化学键类型有_______,RZ42-离子中R原子的杂化方式为_____________________。
(5)由Q与Z、R可形成多种化合物,写出Q2Z2的电子式:____________,
Q2Z熔点比Q2R高,其原因是________________________________________。
(6)QX晶体的结构与NaCl相同,若Q+与最邻近X-的核间距离为a pm,阿伏加德罗常数为NA,则QX晶体的密度为______________________g/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】长式周期表共有18个纵行,从左到右排为1—18列,即碱金属为第一列,稀有气体元素为第18列。按这种规定,下列说法正确的是 ( )
A. 第四周期第9列元素是铁元素
B. 只有第二列的元素原子最外层电子排布为ns 2
C. 14列元素所形成的化合物种类最多
D. 第10、11列为ds区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物H[![]() ]是一种重要的液晶材料,工业上合成它的一种路线如下图所示,其中A是不饱和烃,E的苯环上的有2种不同化学环境的氢原子。
]是一种重要的液晶材料,工业上合成它的一种路线如下图所示,其中A是不饱和烃,E的苯环上的有2种不同化学环境的氢原子。
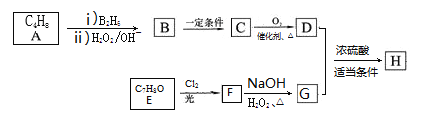
已知:①RCH=CH2![]() RCH2CH2OH
RCH2CH2OH
②一个碳原子上连接有2个-OH时会自动脱去一个水分子形成一个碳氧双键。
(1)H中官能团的名称为____________,E→F的反应类型为____________。
(2)A的名称是____________,E的结构简式为____________ ,B→C中的“一定条件”内容是____________。
(3)F→G的化学方程式为____________。
(4)C还有多种同分异构体,写出其含有碳氧双键的同分异构体的结构简式:____________。
(5)现代物理方法中,能用于区分C、D两种物质的方法是____________(写出一种即可)。
(6)以1—苯基乙醇( )为基本原料制取苯乙醛,仿照C转化为D的形式,表示出合成路线图:_____________________________________________________________。
)为基本原料制取苯乙醛,仿照C转化为D的形式,表示出合成路线图:_____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是三种难溶金属硫化物的溶度积常数(25 ℃):下列有关说法中正确的是
化学式 | FeS | CuS | MnS |
溶度积 | 6.3×10-18 | 1.3×10-36 | 2.5×10-13 |
A. 25 ℃时,将CuS固体用含Mn2+的饱和溶液浸泡可溶解CuS固体
B. 25 ℃时,饱和CuS溶液中,Cu2+的浓度为1.3×10-36 mol·L-1
C. 除去某溶液中的Cu2+,可以选用FeS作沉淀剂
D. 因为H2SO4是强酸,所以反应CuSO4+H2S===CuS↓+H2SO4不能发生
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com