
【题目】下列关于晶体的说法一定正确的是( )
A. 在晶体中只要有阳离子就一定有阴离子
B. CaTiO3晶体(如图)中每个Ti4+和12个O2-相紧邻

CaTiO3的晶体结构模型(图中Ca2+、O2-、Ti4+分别位于立方体的体心、面心和顶点)
C. 金属晶体中金属离子电荷数越多,离子半径越小,金属键就越弱
D. 金属晶体的熔点都比分子晶体的熔点高
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
【题目】某有机化合物的结构简式如右图,有关该化合物的叙述不正确的是( )

A. 该有机物的分子式为C11H12O2
B. 1mol该物质最多能与4molH2发生加成反应
C. 该有机物一定条件下,可以发生取代、氧化、聚合、酯化反应
D. 该有机物能与热的新制氢氧化铜悬浊液反应,生成砖红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于水与生命活动的说法,不正确的是
A. 细胞发生癌变,其自由水含量较正常细胞的低
B. 正在萌发的种子中结合水与自由水的比值降低
C. 在线粒体,叶绿体和核糖体中进行的化学反应都有水生成
D. 自由水和结合水在一定的条件下可以相互转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A、B、C、D四种元素,原子序数依次增大。A是短周期中原子半径最大的元素,B元素3p能级半充满;C是所在周期电负性最大的元素;D是第四周期未成对电子最多的元素。试回答下列有关的问题:
(1)写出D元素价电子的电子排布式:______________。
(2)D可形成化合物[D(H2O)6](NO3)3 。
①[D(H2O)6](NO3)3中阴离子的立体构型是_____________。NO3-中心原子的轨道杂化类型为__________。
②在[D(H2O)6] 3+中D3+与H2O之间形成的化学键称为______,1 mol [D(H2O)6] 3+ 中含有的σ键有________mol。
(3)已知B、C两种元素形成的化合物通常有两种。这两种化合物中________(填化学式)为非极性分子。另一种物质的电子式为_____________。
(4)由A、C两元素形成的化合物组成的晶体中,阴、阳离子都具有球型对称结构,它们都可以看做刚性圆球,并彼此“相切”。如下图所示为A、C形成化合物的晶胞结构图以及晶胞的剖面图:
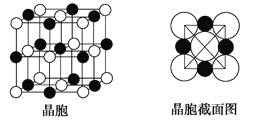
晶胞中距离一个A+最近的C-有________个,这些C-围成的图形是______________,若晶体密度为ρ g·cm-3,阿伏加德罗常数的值用NA表示,则A+的离子半径为________cm(用含NA与ρ的式子表达)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,同种规格的铝片分别与下列物质混合,产生氢气速率最大的是
A. 0.1 mol/L的盐酸15mL B. 0.15 mol/L的硫酸溶液8mL
C. 0.4 mol/L的硝酸12mL D. 18 mol/L的浓硫酸15mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酰氯(COC12),俗称光气,常温下为气体,化学性质不稳定,遇水迅速水解得到强酸,工业用途广泛,是化工制品的重要中间体。
(1)实验室可利用氧气与氯仿(CHCl3)反应得到光气和一种氢化物,写出氧气与氯仿(CHC13)反应的化学反应方程式:_____________________________。
(2)工业上,常用CO与氯气反应得到光气,其热化学方程式为:CO(g)+Cl2(g)![]() COCl2(g) △H=-108 kJ/mol,已知:1 molCl2(g)、1molCO(g)化学键断裂分别需要吸收能量243kJ、1072kJ,则1molCOCl2(g)中化学键断裂需要吸收能量________kJ。
COCl2(g) △H=-108 kJ/mol,已知:1 molCl2(g)、1molCO(g)化学键断裂分别需要吸收能量243kJ、1072kJ,则1molCOCl2(g)中化学键断裂需要吸收能量________kJ。
(3)光气的分解反应为 COCl2(g)![]() CO(g)+Cl2(g) △H=+l08kJ/mol。温度为T1时,该可逆反应在恒容密闭体系中,各物质的浓度与时间关系如下表所示:
CO(g)+Cl2(g) △H=+l08kJ/mol。温度为T1时,该可逆反应在恒容密闭体系中,各物质的浓度与时间关系如下表所示:
浓度/mol L-1 时间/min | COCl2(g) | CO(g) | Cl2(g) |
0 | 0.1300 | 0.0050 | 0.0050 |
5 | 0.0400 |
①在5 min 时恰好达到平衡状态,该反应在此温度下的平衡常数K=________(精确到小数点后两位)。
②0~5min 内,v(COCl2)=_________。
③若保持温度不变,再向容器中充入一定量COCl2 (g),重新达到平衡,此时COCl2 (g)的转化率a(COCl2)_________(填“增大”“减小”或“不变”),试用平衡常数解释原因______________________。
④保持其他条件不变,改变反应温度至T2,反应重新达到平衡,此时测得c(CO)=0.0850 mol/L,则T1________T2(填“>”、“<”、“=”),理由是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C、D的原子序数依次增加。X、Y、Z、W分別是由这四种元素中的两种组成的常见化合物,甲为单质,乙为红棕色气体,Y为淡黄色固体。上述物质之间的转化关系如下图所示(部分反应物或生成物省略),则下列说法中正确的是( )

A. 原子半径:D>C>B>A
B. C. D的氢化物均为共价化合物
C. 相对分子质量W>X,沸点W>X
D. B的氢化物常温下一定为气态,C的氢化物常温下为液态
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com