
【题目】已知:A、B、C、D四种元素,原子序数依次增大。A是短周期中原子半径最大的元素,B元素3p能级半充满;C是所在周期电负性最大的元素;D是第四周期未成对电子最多的元素。试回答下列有关的问题:
(1)写出D元素价电子的电子排布式:______________。
(2)D可形成化合物[D(H2O)6](NO3)3 。
①[D(H2O)6](NO3)3中阴离子的立体构型是_____________。NO3-中心原子的轨道杂化类型为__________。
②在[D(H2O)6] 3+中D3+与H2O之间形成的化学键称为______,1 mol [D(H2O)6] 3+ 中含有的σ键有________mol。
(3)已知B、C两种元素形成的化合物通常有两种。这两种化合物中________(填化学式)为非极性分子。另一种物质的电子式为_____________。
(4)由A、C两元素形成的化合物组成的晶体中,阴、阳离子都具有球型对称结构,它们都可以看做刚性圆球,并彼此“相切”。如下图所示为A、C形成化合物的晶胞结构图以及晶胞的剖面图:
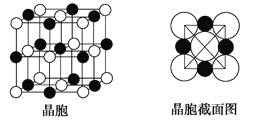
晶胞中距离一个A+最近的C-有________个,这些C-围成的图形是______________,若晶体密度为ρ g·cm-3,阿伏加德罗常数的值用NA表示,则A+的离子半径为________cm(用含NA与ρ的式子表达)。
【答案】 3d54s1 平面三角形 sp2杂化 配位键 18 PCl5 ![]() 6 正八面体
6 正八面体 
【解析】A、B、C、D四种元素,原子序数依次增大。A是短周期中原子半径最大的元素,A为Na元素;B元素3p能级半充满,B为P元素。D是第四周期未成对电子最多的元素,D为Cr元素;C是所在周期电负性最大的元素,C为第ⅦA族元素,C为Cl元素。
(1)D为Cr元素,D元素价电子的电子排布式为3d54s1,故答案为:3d54s1;
(2)①[D(H2O)6](NO3)3中NO3- NO3-中价层电子对个数=3+![]() (5+1-3×2)=3,且不含孤电子对,所以该分子为平面三角形,中心原子采用sp2杂化,故答案为:平面三角形;sp2杂化;
(5+1-3×2)=3,且不含孤电子对,所以该分子为平面三角形,中心原子采用sp2杂化,故答案为:平面三角形;sp2杂化;
②在[Cr (H2O)6] 3+配合离子中Cr3+与H2O之间形成的化学键为配位键;水分子中含有σ键2×6=12,配位键也是σ键,1 mol [D(H2O)6] 3+ 中含有的σ键有12+6=18mol,故答案为:18;
(3)已知B、C两种元素形成的化合物为PCl3和PCl5,PCl3为三角锥形结构,属于极性分子,PCl5为三角双锥结构,属于非极性分子,其中PCl3的电子式为![]() ,故答案为:PCl5;
,故答案为:PCl5; ![]() ;
;
(4)由Na、Cl两元素形成的化合物为NaCl,以中间的黑色球为Na+离子研究,与之最近的氯离子有6个,这些氯离子围成的图形是正八面体;晶胞中Na+离子数目=1+12×![]() =4,Cl-离子数目=8×
=4,Cl-离子数目=8×![]() +6×
+6×![]() =4,故晶胞质量=
=4,故晶胞质量=![]() g,晶胞体积=[
g,晶胞体积=[![]() g÷ρ]cm3=
g÷ρ]cm3=![]() cm3,令Na+离子半径为r,则棱长为
cm3,令Na+离子半径为r,则棱长为![]() ×4r=2
×4r=2![]() r,故(2
r,故(2![]() r)3=
r)3=![]() cm3,解得r=
cm3,解得r=![]() ×
× cm,故答案为:6;
cm,故答案为:6; ![]() ×
× 。
。


科目:高中化学 来源: 题型:
【题目】葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过以下反应制得:C6H12O6(葡萄糖)+Br2+H2O![]() C6H12O7(葡萄糖酸)+2HBr,2C6H12O7(葡萄糖酸)+CaCO3
C6H12O7(葡萄糖酸)+2HBr,2C6H12O7(葡萄糖酸)+CaCO3![]() Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑,相关物质的溶解性见下表:
Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑,相关物质的溶解性见下表:
物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
水中的溶解性 | 可溶于冷水 易溶于热水 | 可溶 | 易溶 | 易溶 |
乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |
实验流程如下:
C6H12O6溶液![]()
![]()
![]()
![]() 悬浊液
悬浊液![]()
![]()
![]() Ca(C6H11O7)2
Ca(C6H11O7)2
请回答下列问题:
(1)第①步中溴水氧化葡萄糖时,下列装置最合适的是________。

制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其它试剂,下列物质中最适合的是____。
A.新制Cu(OH)2悬浊液 B.酸性KMnO4溶液
C.O2/葡萄糖氧化酶 D.[Ag(NH3)2]OH溶液
(2)第②步充分反应后CaCO3固体需有剩余,其目的是__________________________;
本实验中不宜用CaCl2替代CaCO3,理由是__________________。
(3)第③步需趁热过滤,其原因是____________________________________。
(4)第④步加入乙醇的作用是__________________________________。
(5)第⑥步中,下列洗涤剂最合适的是___________________________。
A.冷水 B.热水 C.乙醇 D.乙醇-水混合溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T1和T2温度下(T1>T2),BaSO4在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是( )

A. T1时,c点有沉淀生成
B. T2时,蒸发溶剂可能由d点变到b点
C. T2时,由a点开始加入BaCl2固体,Ksp增大
D. BaSO4的溶解度随温度升高而增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请填写下列空白:
(1)双酚A(也称BPA)常用来生产防碎塑料聚碳酸酯。BPA的结构简式如图所示。

下列关于双酚A的叙述中,不正确的是__________。
A.遇FeCl3溶液变色
B.可以发生还原反应
C.1 mol双酚A最多可与2 mol Br2反应
D.可与NaOH溶液反应
双酚A的一种合成路线如图所示:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
B→C的化学方程式是_______________。
(2)在有机化学分析中,根据反应物的性质和所得的产物,即可确定烯烃中双键的位置,

某有机物X的分子式为C9H14,经催化加氢后得到分子式为C9H18的饱和化合物,X可发生如下变化:

试写出有机物X可能的结构简式:__________________________.
(3)环蕃A(cyclophane)和超蕃B(superphane)是一种光电信息材料,都属于烃(B中氢原子未画出),它们的结构如图所示。

下列有关说法正确的是________。
A、环蕃和超蕃互为同系物
B、环蕃能使酸性高锰酸钾溶液褪色
C、环蕃能与液溴、硝酸发生取代反应
D、超蕃的一氯取代物只有1种,二氯取代物有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于晶体的说法一定正确的是( )
A. 在晶体中只要有阳离子就一定有阴离子
B. CaTiO3晶体(如图)中每个Ti4+和12个O2-相紧邻

CaTiO3的晶体结构模型(图中Ca2+、O2-、Ti4+分别位于立方体的体心、面心和顶点)
C. 金属晶体中金属离子电荷数越多,离子半径越小,金属键就越弱
D. 金属晶体的熔点都比分子晶体的熔点高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2011年为国际化学年,主题为“化学—我们的生活,我们的未来”下列说法正确的是
A. 制作航天服的聚酯纤维和用于光缆通信的晶体硅都是新型无机非金属材料
B. 金刚砂的成分是Al2O3,可用作砂纸、砂轮的磨料
C. 石油化工生产广泛使用过渡元素做催化剂并加入少量稀土元素改善催化剂的性能
D. 福尔马林(甲醛溶液)可用于浸泡生肉及海产品以防腐保鲜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙酮和水杨酸(邻羟基苯甲酸)都是医药工程的重要原料,以其为起点可合成重要的医药中间体4-羟基香豆素。根据以下合成路线,回答问题:

已知:
(1)C中含有的官能团名称为_______________,B→C的反应类型为_____________。
(2)E→F的化学方程式为______________________ 。
(3)F+D→G的化学方程式为_________________________________。
(4)1 mol H最多能与________molNaOH发生反应。
(5)同时满足下列条件的E的同分异构体有_________种,写出其中一种核磁共振氢谱有4组峰的结构简式:____________________。
①能发生银镜反应;②能与FeCl3溶液发生显色反应。
(6)结合题给信息,请设计合理方案,由![]() 合成
合成![]() ,其他无机试剂自选。合
,其他无机试剂自选。合
成路线图示例如下:![]() 。________________________________________。
。________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】证明某溶液含有Fe2+的实验方法是 ( )
A. 先滴加氯水,再滴加KSCN溶液后显红色
B. 先滴加KSCN溶液,不显红色,再滴加氯水后显红色
C. 滴加NaOH溶液,产生白色沉淀
D. 只需滴加KSCN溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com