
【题目】以红土镍矿(含NiO及铁、镁、硅的氧化物等)为原料制备Ni(OH)2的工艺流程如图:
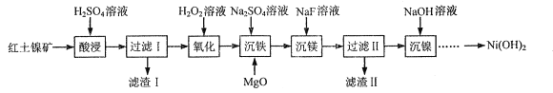
(1)“酸浸”时,H2SO4稍过量的目的是___。
(2)“氧化”时,Fe2+发生反应的离子方程式为___。
(3)“沉铁”时生成黄钠铣矾[Na2Fe6(SO4)4(OH)12]沉淀.该反应的化学方程式为___。
(4)“沉镁”时,需综合考虑镁去除率和镍损失率。不同pH下镁去除率和镍损失率如图所示。
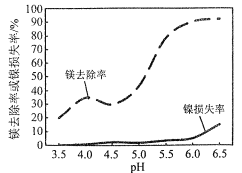
①应控制反应体系的pH约为___(填字母)。
A.5.0 B.6.0 C.6.5
②巳知Ksp(MgF2)=7.4×10-11。要使“沉镁”所得滤液中c(Mg2+)≤7.4×10-7mol·L-1,则应控制滤液中c(F-)不低于___。
(5)“沉镍”所得滤液中,可循环使用的主要溶质为___(填化学式)。
【答案】提高铁和镍元素的浸出率 2H++2Fe2++H2O2===2Fe3++2H2O 3Fe2(SO4)3+Na2SO4+6H2O+6MgO===Na2Fe6(SO4)4(OH)12+6MgSO4 B 0.01mol·L—1 Na2SO4
【解析】
红土镍矿加硫酸溶液酸浸时,除硅的氧化物外,其他均溶解,因此滤渣1为硅的氧化物,而滤液1中含Fe2+、Mg2+和Ni2+,Fe2+被H2O2溶液氧化成Fe3+,沉铁时投入硫酸钠和氧化镁,发生反应3Fe2(SO4)3+Na2SO4+6H2O+6MgO===Na2Fe6(SO4)4(OH)12+6MgSO4,再加NaF溶液沉镁后经过滤得到Mg(OH)2和[Na2Fe6(SO4)4(OH)12]的沉淀,所得滤液再加NaOH可得Ni(OH)2。
(1)“酸浸”时,H2SO4稍过量可提高铁和镍元素的浸出率,故答案为:提高铁和镍元素的浸出率;
(2)Fe2+被H2O2溶液氧化成Fe3+,反应方程式为:2H++2Fe2++H2O2===2Fe3++2H2O;
(3)根据上述分析,“沉铁”时生成黄钠铣矾[Na2Fe6(SO4)4(OH)12]的化学方程式为:3Fe2(SO4)3+Na2SO4+6H2O+6MgO===Na2Fe6(SO4)4(OH)12+6MgSO4;
(4)根据图像可知,镁去除率最高和镍损失率最低的综合pH为6.5,故选B;
(5)Ksp(MgF2)=c(Mg2+)·c2(F—)=7.4×10-11,要使“沉镁”所得滤液中c(Mg2+)≤7.4×10-7mol·L-1,c2(F—) 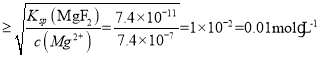 ,故答案为:0.01mol·L—1;
,故答案为:0.01mol·L—1;
(6)“沉镍”所得滤液中主要含Na2SO4,故循环利用的主要成分为Na2SO4。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、Q、R 是周期表中前 36 号元素,核电荷数依次增大,其中 X、Y、Z、 W 都是元素周期表中短周期元素。X 为非金属元素,且 X 原子的核外成对电子数是未成对电子数的 2 倍,Z 的次外层电子数是最外层电子数的![]() ,W 原子的 s 电子与 p 电子数相等,Q 是前四周期中电负性最小的元素,R 的原子序数为 29。 回答下列问题:
,W 原子的 s 电子与 p 电子数相等,Q 是前四周期中电负性最小的元素,R 的原子序数为 29。 回答下列问题:
(1)X的最高价氧化物对应的水化物分子中,中心原子采取______________杂化。
(2)化合物 XZ 与 Y 的单质分子互为______________,1mol XZ 中含有π键的数目为______________。
(3)W 的稳定离子核外有______________种运动状态的电子。W元素的第一电离能比其同周期 相邻元素的第一电离能高,其原因是:_____。
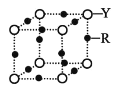
(4)Q 的晶体结构如图所示,则在单位晶胞中 Q 原子的个数为______________,晶体的配位数是______________。
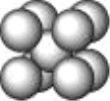
(5)R元素的基态原子的核外电子排布式为________;Y 与 R 形成某 种化合物的晶胞结构如图所示,已知该晶体的密度为ρg·cm-3,阿伏加德罗常数的数值为 NA,则该晶体中 R 原子和 Y 原子之间的最短距离为______________cm。(只写计算式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为提升电池循环效率和稳定性,科学家近期利用三维多孔海绵状Zn(3DZn)可以高效沉积ZnO的特点,设计了采用强碱性电解质的3DZn—NiOOH二次电池,结构如下图所示。电池反应为Zn(s)+2NiOOH(s)+H2O(l)![]() ZnO(s)+2Ni(OH)2(s)。
ZnO(s)+2Ni(OH)2(s)。

A. 三维多孔海绵状Zn具有较高的表面积,所沉积的ZnO分散度高
B. 充电时阳极反应为Ni(OH)2(s)+OH(aq)e![]() NiOOH(s)+H2O(l)
NiOOH(s)+H2O(l)
C. 放电时负极反应为Zn(s)+2OH(aq)2e![]() ZnO(s)+H2O(l)
ZnO(s)+H2O(l)
D. 放电过程中OH通过隔膜从负极区移向正极区
查看答案和解析>>
科目:高中化学 来源: 题型:
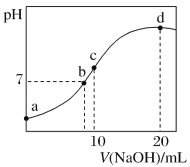
【题目】常温下,向 20 mL 0.1 mol·L-1(NH4)2SO4 溶液中逐滴加入 0.2 mol·L-1NaOH 溶液时,溶液的 pH与所加 NaOH 溶液体积的关系如图所示(不考虑挥发)。下列说法正确的是
A.点 a 所示溶液中:c(NH![]() )>c(SO
)>c(SO![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
B.点 b 所示溶液中:c(NH![]() )=c(Na+)>c(H+)=c(OH)
)=c(Na+)>c(H+)=c(OH)
C.点 c 所示溶液中:c(SO![]() )+c(H+)=c(NH3·H2O)+c(OH)
)+c(H+)=c(NH3·H2O)+c(OH)
D.点 d 所示溶液中:c(SO![]() )>c(NH3·H2O)>c(OH-)>c(NH
)>c(NH3·H2O)>c(OH-)>c(NH![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH![]() 、Cl-、Mg2+、Ba2+、CO
、Cl-、Mg2+、Ba2+、CO![]() 、SO
、SO![]() ,现取三份 100 mL 溶液进行如下实验:
,现取三份 100 mL 溶液进行如下实验:
(1)第一份加足量 NaOH 溶液加热后,收集到气体 0.04 mol。
(2)第二份加足量 BaCl2 溶液后,得干燥沉淀 6.27 g,经足量盐酸洗涤、干燥后,沉淀质量为 2.33 g。
(3)第三份加入 AgNO3 溶液有沉淀产生。根据上述实验,以下推测不正确的是
A.100 mL 溶液中含 0.04 mol NH![]()
B.100 mL 溶液中含 0.01 mol SO42-和 0.02 mol CO32-
C.K+、Cl-可能存在
D.一定不存在Ba2+、Mg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氯酸钾熔化,粒子间克服了_____的作用力;二氧化硅熔化,粒子间克服了_____的作用力;碘的升华,粒子间克服了_____的作用力。三种晶体的熔点由高到低的顺序是_____。
(2)下列六种晶体:①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,它们的熔点从低到高的顺序为_____ (填序号)。
(3)在H2、(NH4)2SO4、SiC、CO2、HF中,五种物质的熔点由高到低的顺序是_____。
(4)A、B、C、D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于CS2,不溶于水
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为3500℃
试推断它们的晶体类型:A_____;B_____;C_____;D_____。
(5)如图中A~D是中学化学教科书上常见的几种晶体结构模型,请填写相应物质的名称:A_____;B_____;C_____;D_____。
A.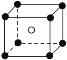 B.
B.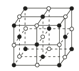 C.
C.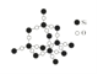 D.
D.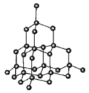
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年度诺贝尔化学奖授予在锂离子电池发展做出贡献的三位科学家。某浓差电池的原理示意如图所示,可用该电池从浓缩海水中提取LiCl溶液。下列有关该电池的说法不正确的是( )
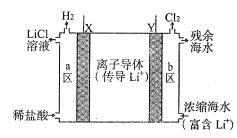
A.该装置可在提取LiCl溶液的同时得电能
B.电子由Y极通过外电路移向X极
C.正极发生的反应为:2H++2e—===H2↑
D.Y极每生成22.4LCl2,有2molLi+从b区移至a区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废弃物的资源化回收再利用,可以更大限度地发挥原材料的价值。某教师在指导学生做研究性学习时,拟利用废铁屑在实验室制备FeSO4溶液,再与等物质的量的(NH4)2SO4反应,制备补血剂硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O,相对分子质量为392]。硫酸亚铁铵晶体比一般亚铁盐稳定,在空气中不易被氧化,易溶于水,不溶于乙醇。
(1)废铁屑的净化:将废铁屑投入10%的碳酸钠溶液中并加热5~10min,通过倾析法弃去纯碱溶液,并用蒸馏水洗净废铁屑,待用。
(2)酸浸净化后的废铁屑:将2gFe粉、10mL3mol·L-1的H2SO4溶液加入烧瓶中反应,用如图所示装置制备FeSO4溶液。保持温度70~80℃,适当添加水以补充被蒸发掉的水分,并控制溶液的pH,至反应无明显气泡产生,停止加热,过滤,称量残留固体质量。
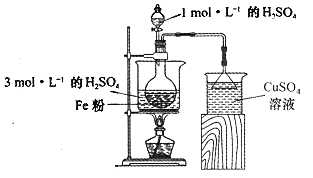
①反应过程中会产生少量H2S、PH3等气体,需使用封闭装置。写出用CuSO4溶液吸收H2S气体的化学反应方程式:____________________________
②反应过程中使用过量铁粉的目的是____________________________
(3)制备(NH4)2Fe(SO4)2·6H2O:向FeSO4溶液中加入一定质量的(NH4)2SO4固体,70~80℃条件下溶解后,趁热倒入50mL乙醇中,析出晶体。
实验中,需对过滤出产品的母液(pH<1)进行处理。室温下,分别取母液并向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是_____ (填序号)。
A.通入过量Cl2:Fe2+、H+、NH4+、Clˉ、SO42ˉ
B.加入过量KSCN溶液:K+、NH4+、Fe3+、SO42ˉ、SCNˉ
C.加入过量NaOH溶液:Na+、Fe2+、NH4+、SO42ˉ、OHˉ
D.加入过量NaClO和NaOH的混合溶液:Na+、SO42ˉ、Clˉ、ClOˉ、OHˉ
(4)产品纯度测定:称取ag产品溶于水,配制成500mL溶液,取25.00mL待测液,用浓度为cmol·L-1的酸性KMnO4溶液滴定。重复上述操作2次实验结果如下:

该产品的纯度为____________________________(用含a、c的代数式表示)。
有同学提出,测定产品中SO42ˉ的含量也可测定产品的纯度,请补充完整实验方案:称取约0.4g样品,溶于70mL水,__________________________________________________,将沉淀移入坩埚,灼烧至恒重,记录数据(实验中必须使用的试剂有:2mol·L-1的HCl溶液、BaCl2溶液、AgNO3溶液)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定某有机物A的结构,做如下实验:
①将2.3 g该有机物完全燃烧,生成0.1 mol CO2和2.7 g水;
②用质谱仪测定其相对分子质量,得如图一所示的质谱图;
③用核磁共振仪处理该化合物,得到如图二所示图谱,图中三个峰的面积之比是1∶2∶3。试回答下列问题:
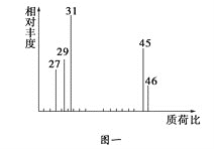

(1)有机物A的相对分子质量是________。
(2)有机物A的实验式是________。
(3)A的分子式是_______________________________________。
(4)A的结构简式为___________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com