
将如图所示实验装置的K闭合,下列判断正确的是( )
A.电子沿Zn a a b b Cu路径流动 Cu路径流动 |
| B.片刻后可观察到滤纸b点变红色 |
| C.片刻后甲池中c(SO42-)增大 |
D. 电极上发生还原反应 电极上发生还原反应 |
科目:高中化学 来源: 题型:单选题
为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。其反应原理如下:电池 Pb(s) + PbO2(s) + 2H2SO4(aq) =2PbSO4(s) + 2H2O(l)
电解池 2Al + 3H2O = Al2O3 + 3H2,对该电解过程,以下判断正确的是
| | 电池 | 电解池 |
| A | H+移向Pb电极 | H+移向Pb电极 |
| B | 每消耗3molPb | 生成1molAl2O3 |
| C | 正极:PbO2+4H++2e—=Pb2++2H2O | 阳极:2Al+3H2O—6e—=Al2O3+6H+ |
| D | Pb电极反应质量不变 | Pb电极反应质量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法中正确的是
| A.在船体上镶嵌锌块,可以减缓船体被海水腐蚀的速率 |
| B.粗铜精炼时,电镀液中的c(Cu2+)保持不变 |
| C.纯银在空气中久置变黑发生的是电化学腐蚀 |
| D.阴极电保护法是将被保护的金属与外加电源的正极相连 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。下图为RFC工作原理示意图,有关说法正确的是
A.转移0.1mol电子时,a电极产生1.12LH2
B.b电极上发生还原反应
C.酸性电解质溶液中H+移向c电极
D.d电极上发生的电极反应是:O2+4H++4e-=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列事实解释准确的是
| A.糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。脱氧过程中铁作原电池正极,电极反应为: Fe-2e- = Fe2+ |
| B.酸性氢氧燃料电池的正极电极反应为: 2H2O十O2+4e-=4OH- |
| C.用石墨电极电解CuC12溶液:阳极上发生的反应:2C1-—2e一=C12↑ |
| D.铅蓄电池的正极反应为:PbO2 +4H+ +2e一=Pb2+ +2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
如图所示,将铁棒和石墨棒插入饱和食盐水中。下列说法正确的是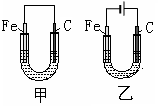
| A.甲中铁被保护不会腐蚀 |
| B.甲中正极反应式为4OH--4e- = 2H2O+O2 |
| C.乙中铁电极上发生氧化反应 |
| D.乙中石墨电极附近滴几滴碘化钾淀粉溶液变蓝色 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
“天宫一号”飞行器白天靠太阳能帆板产生电流向镍氢电池充电,夜间镍氢电池向飞行器供电。镍氢电池结构示意图如图。若电池总反应为:Ni(OH)2  NiOOH+1/2H2,充电时阴极反应为:H2O+e-=1/2H2+OH-。则下列说法正确的是( )
NiOOH+1/2H2,充电时阴极反应为:H2O+e-=1/2H2+OH-。则下列说法正确的是( )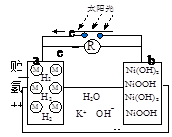
| A.充电时a极为正极 |
| B.放电时NiOOH发生氧化反应 |
| C.充电时,OH-向移a极, K+移向b极 |
| D.放电时正极反应为:NiOOH + H2O +e- = Ni(OH)2 + OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述正确的是 ( )
①原电池是把化学能转化成电能的一种装置 ②原电池的正极发生氧化反应,负极发生还原反应 ③不能自发进行的氧化还原反应,通过原电池的装置均可实现 ④碳棒不能用来作原电池的正极 ⑤反应Cu+2Ag+=2Ag+Cu2+,能以原电池的形式来实现
| A.①⑤ | B.①④⑤ | C.②③④ | D.②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
Cu2O是一种半导体材料,基于绿色化学理念设计的制取。Cu2O的电解池示意图如下,电解总反应:2Cu+H2O Cu2O+H2↑下列说法正确的是
Cu2O+H2↑下列说法正确的是
| A.石墨电极上产生氢气 |
| B.铜电极发生还原反应 |
| C.铜电极接直流电源的负极 |
| D.当有0.1mol电子转移时,有0.1molCu2O生成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com