
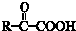 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$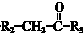
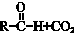 $→_{△}^{NaOH(ap)}$R1-
$→_{△}^{NaOH(ap)}$R1-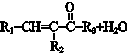
 .
.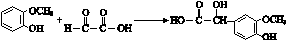 ;其反应类型是加成反应.
;其反应类型是加成反应.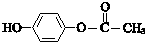 .
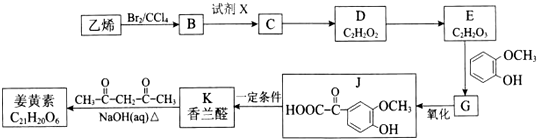
.分析 乙烯和溴发生加成反应生成B为BrCH2CH2Br,由B→E转化及D、E分子式可知,E中含有羧基,D氧化得到E,则D中含有-CHO,则B在氢氧化钠水溶液、加热条件下发生水解反应生成C为HOCH2CH2OH,D为OHC-CHO,D中部分醛基被氧化生成E为OHC-COOH,结合J的结构可知,E中醛基发生加成生成G为 ,G中的醛基被氧化生成J,J在一定条件下发生信息i中脱羧反应生成K为
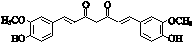
,G中的醛基被氧化生成J,J在一定条件下发生信息i中脱羧反应生成K为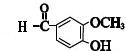 ,结合信息ii及姜黄素的分子式,可知姜黄素的结构简式为:
,结合信息ii及姜黄素的分子式,可知姜黄素的结构简式为: ,据此分析解答.
,据此分析解答.
解答 解:乙烯和溴发生加成反应生成B为BrCH2CH2Br,由B→E转化及D、E分子式可知,E中含有羧基,D氧化得到E,则D中含有-CHO,则B在氢氧化钠水溶液、加热条件下发生水解反应生成C为HOCH2CH2OH,D为OHC-CHO,D中部分醛基被氧化生成E为OHC-COOH,结合J的结构可知,E中醛基发生加成生成G为 ,G中的醛基被氧化生成J,J在一定条件下发生信息i中脱羧反应生成K为
,G中的醛基被氧化生成J,J在一定条件下发生信息i中脱羧反应生成K为 ,结合信息ii及姜黄素的分子式,可知姜黄素的结构简式为:
,结合信息ii及姜黄素的分子式,可知姜黄素的结构简式为: ,
,
(1)E为OHC-COOH,E中含有的官能团名称是醛基、羧基,故答案为:醛基、羧基;
(2)B为BrCH2CH2Br,其名称是1,2-二溴乙烷,通过以上分析知,X是氢氧化钠水溶液,故答案为:1,2-二溴乙烷;NaOH溶液;
(3)通过以上分析知,姜黄素的结构简式为
故答案为:
(4)E中醛基发生加成生成G为 ,反应方程式为
,反应方程式为

(5)香兰醛( )中含有醛基、酚羟基、苯环、醚键,不能与NaHCO3溶液反应,可以与浓溴水发生取代反应,与FeCl3溶液发生显色反应,1 mol香兰醛最多能与4molH2发生加成反应,故ad错误,bc正确,故答案为:bc;
)中含有醛基、酚羟基、苯环、醚键,不能与NaHCO3溶液反应,可以与浓溴水发生取代反应,与FeCl3溶液发生显色反应,1 mol香兰醛最多能与4molH2发生加成反应,故ad错误,bc正确,故答案为:bc;
(6)香兰醛( )的同分异构体符合条件:①属于芳香族化合物 ②与氯化铁溶液发生显色反应,说明含有酚羟基,③苯环上只有两个取代基 ④存在羰基的结构,所以苯环上除酚羟基之外的另一取代基是问题的关键,另一取代基可能的结构有-CH2COOH、-O-COCH3、-COOCH3、-CH2-O-CHO、-O-CH2CHO、-COCH2OH、-CH(OH)CHO共7种,每种取代基都有邻、间、对3种不同的结构,所以符合条件的香兰醛的同分异构体共有21种;
)的同分异构体符合条件:①属于芳香族化合物 ②与氯化铁溶液发生显色反应,说明含有酚羟基,③苯环上只有两个取代基 ④存在羰基的结构,所以苯环上除酚羟基之外的另一取代基是问题的关键,另一取代基可能的结构有-CH2COOH、-O-COCH3、-COOCH3、-CH2-O-CHO、-O-CH2CHO、-COCH2OH、-CH(OH)CHO共7种,每种取代基都有邻、间、对3种不同的结构,所以符合条件的香兰醛的同分异构体共有21种;
香兰醛(K)的同分异构体符合:①苯环上的一氯取代物只有2种,则苯环上有2种H原子;②1mol该物质与烧碱溶液反应,最多消耗3mol NaOH,说明分子中存在酚羟基、羧酸与酚形成酯基,③核磁共振氢谱中有4种吸收峰,酚羟基有1种H原子,苯环上有2种H原子,结合香兰醛的结构可知,含有2个不同的取代基且处于对位,苯环上除酚羟基之外的另一取代基含有原子H原子,所以符合该条件的K的同分异构体的结构简式为 ,
,
故答案为:21; .
.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力,需要学生对给予的信息进行利用,综合分析确定E的结构是关键,较好地考查学生自学能力与分析推理能力,注意掌握官能团想性质与转化,(6)中同分异构体的书写为易错点、难度,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 将水加热,Kw增大,pH不变 | |
| B. | 燃烧热是指可燃物热化学反应方程式中的△H | |
| C. | 用25 mL碱式滴定管量取20.00mL高锰酸钾溶液 | |
| D. | 醋酸溶液的导电能力可能比稀硫酸强 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
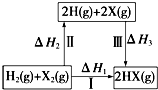
| A. | H2(g)+X2(g)═2H(g)+2X(g)△H2<0 | |
| B. | △H1=△H2+△H3 | |
| C. | 途径Ⅲ的按Cl、Br、I顺序依次增大 | |
| D. | 途径Ⅰ生成HCl比生成HBr的△H1小,说明HCl比HBr稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③④ | C. | ②④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3种 | B. | 5种 | C. | 4种 | D. | 6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
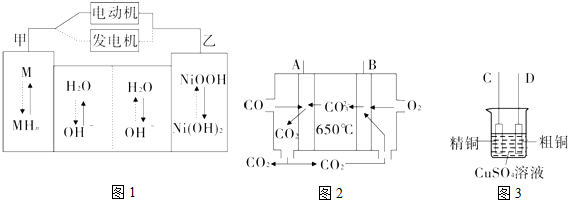
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸能使湿润的蓝色石蕊试纸先变红后变黑 | |
| B. | 浓硫酸在常温下可迅速与铜片反应,放出二氧化硫气体 | |
| C. | 浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体 | |
| D. | 浓硫酸在常温下能使铁铝等金属钝化,加热条件下也不反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 37gNH4F和16gCH4中含有的共价键数均为4NA | |
| B. | 0.51.4mol•L-1的NaHSO3溶液中含有的SO32-数为2NA | |
| C. | 标准状况下,16.8LNO2完全溶于水,转移电子数为0.5NA | |
| D. | 高温高压和催化剂条件下,密闭容器中2gH2与足量N2反应,转移电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
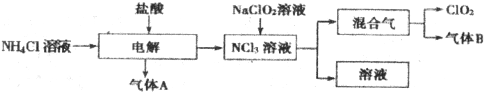
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com