
| A、乙烯的结构简式:CH2CH2 |
B、甲烷分子的比例模型: |
| C、乙酸的结构简式:C2H4O2 |
D、羟基的电子式: |
 ,故B正确;
,故B正确;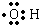 ,故D错误;
,故D错误;

科目:高中化学 来源: 题型:
 将Na2CO3和NaHCO3的混合物共19克,加热到质量不再发生变化时,称得剩余固体质量为15.9克.则
将Na2CO3和NaHCO3的混合物共19克,加热到质量不再发生变化时,称得剩余固体质量为15.9克.则查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、其单质与水反应的通式为:X2+H2O→HX+HXO |
| B、HX易溶于水,其水溶液是强酸 |
| C、HX都可用相应的NaX与浓硫酸共热制取 |
| D、按F、Cl、Br、I的顺序,其单质的氧化性逐渐减弱,阴离子的还原性逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、两种元素形成的共价分子中的化学键都是极性键 |
| B、两种非金属元素原子之间形成的化学键一定是极性键 |
| C、全部由极性键构成的分子一定是极性分子 |
| D、离子化合物熔点一定比共价化合物的熔点高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应A(g)?2B(g),若正反应的活化能为Ea KJ?mol-1,逆反应的活化能为Eb KJ?mol-1,则△H=(Ea-Eb)KJ?mol-1 |
| B、H2的热值为142.9kJ?g-1,则氢气燃烧的热化学方程式可表示为2H2(g)+O2(g)=2H2O(l)△H=-285.8kJ?mol-1 |
| C、能自发进行的化学反应,一定是△H<0、△S>0 |
| D、增大反应物浓度,可增大单位体积内活化分子百分数,从而增加有效碰撞的次数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、固态氯化钾不导电,所以氯化钾不是电解质 |
| B、石墨能导电,所以石墨是电解质 |
| C、硫酸溶液能导电,所以硫酸是电解质 |
| D、CO2溶于水能导电,所以CO2是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、强碱性溶液中:K+、Al3+、Cl-、SO42- |
| B、滴加石蕊试液显红色的溶液::K+、Mg2+、Cl-、NO3- |
| C、Fe2+物质的量浓度为0.1mol?L-1的溶液中:Na+、K+、SO42-、Cl- |
| D、加入铝粉放出大量H2的溶液中:Na+、Ba2+、HCO3-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com