
【题目】下列有关化学用语的表示方法中正确的是( )
A. 次氯酸的结构式: H -Cl - O
B. M2+离子核外有 a 个电子,b 个中子,M 原子符号为:![]()
C. 用电子式表示K2O 的形成过程为:![]()
D. Na+的结构示意图: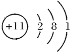
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑧中元素,回答以下问题:
主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
一 | ||||||||
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)在③~⑦元素中,原子半径最大的是__________用元素符号或化学式填空,下同),其离子的原子结构示意图为________。
(2)元素的最高价氧化物对应的水化物中酸性最强的是_____;碱性最强的是______,写出该物质和呈两性的氢氧化物的化学反应方程式____________________;
(span>3)在以上元素的单质中,化学性质最不活泼的是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳和乙二醇在氧化锌或锌盐催化下可合成碳酸乙烯酯。
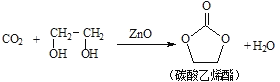
回答下列问题:
(1)锌基态离子的价电子排布图为_______________;在基态18O原子中,核外电子存在_________种空间运动状态。
(2)乙二醇中C、H、O的电负性大小关系是__________ ;碳酸乙烯酯中碳原子的杂化轨道类型有___________;1mol 碳酸乙烯酯中含有的σ键的数目为__________NA。
(3)锌盐水溶液中Zn2+可与H2O之间形成[Zn(H2O)6]2+,配体中的配位原子是_________(填微粒符号),[Zn(H2O)6]2+中所含化学键的类型为__________________________。
(4)阴离子X-与CO2互为等电子体且X-内含共价键和氢键,则X-的化学式为______________。
(5)一种锌金合金晶体的立方体晶胞中,金原子位于顶点,锌原子位于面心,则该合金中金原子与锌原子的个数之比为_________;若该晶体的晶胞棱长为apm(1pm=10-12m),则该合金的密度为_______g·cm-3(用NA表示阿伏加德罗常数的值,列出算式不要求结果)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化中,属于吸热反应的是
①液态水的汽化②将胆矾加热变为白色粉末③浓硫酸稀释④KClO3分解制氧气⑤生石灰跟水反应生成熟石灰⑥CaCO3高温分解⑦CO2+C![]() 2CO⑧Ba(OH)2·8H2O与固体NH4Cl混合⑨C(s)+H2O(g)
2CO⑧Ba(OH)2·8H2O与固体NH4Cl混合⑨C(s)+H2O(g)![]() CO(g)+H2(g) ⑩Al与HCl反应
CO(g)+H2(g) ⑩Al与HCl反应
A. ②③④⑤⑥⑦⑧⑨ B. ②③④⑧⑨
C. ②④⑥⑧ D. ②④⑥⑦⑧⑨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如下图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法不正确的是( )

A. 原子半径:W>Z>Y>X
B. 最高价氧化物对应水化物的酸性:X>W>Z
C. 最简单气态氢化物的热稳定性:Y>X>W>Z
D. 元素X、Z、W的最高化合价分别与其主族序数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种金属片在稀盐酸中,用导线连接,可以组成原电池,实验结果如图所示:则四种金属的活泼性由强到弱的顺序为( )
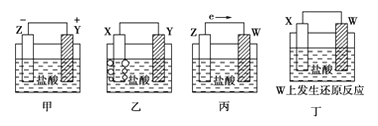
A. Z>Y>X>WB. Z>X>Y>WC. Z>Y>W>XD. Y>Z>X>W
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学对Cu的常见化合物的性质进行实验探究,研究的问题和过程如下:
(1)为探究Cu(OH)2是否和Al(OH)3一样具有两性,除选择Cu(OH)2外,必须选用的试剂为____________ (填序号) a.氨水 b.氢氧化钠溶液 c.稀硫酸 d.冰醋酸
(2)为探究不同价态铜的稳定性,进行如下实验:
①将CuO粉末加热至1000℃以上完全分解成红色的Cu2O粉末。
②向Cu2O中加适量稀硫酸,得到蓝色溶液和一种红色固体,该反应的离子化学方程式为 ____________ 。
(3)为了探究氨气能否和氢气一样还原CuO,他根据所提供的下列装置进行实验(夹持装置未画),装置A产生氨气,按气流方向连接各仪器接口,顺序为a→___→___→___→___→___→___→h
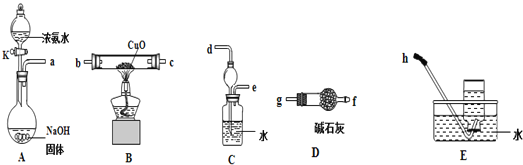
①实验开始时,打开分液漏斗的活塞K,发现浓氨水没有滴下,如果各仪器导管均没有堵塞,则可能的原因是_______________________________________。
②实验结束后,装置B中固体由黑色变为红色,装置E中收集到无色无味的气体,在空气中无颜色变化,点燃的镁条可以在其中燃烧,则B装置中发生的化学方程式为_____________________。
③装置C中的球形装置的作用是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据表中数据,下列判断正确的是( )

A. 在等浓度的NaF、NaH2PO4混合溶液中:c(Na+) + c(H+)=c(F-) + c(H2PO4-) + c(OH-)
B. 少量H3PO4和NaF反应的离子方程式为:H3PO4 +2F-===HPO42-+2HF
C. 同温同浓度时,溶液的pH:NaF>NaH2PO4>Na2HPO4
D. 结合质子能力:PO43->HPO42->F-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含有HCO3-、Na+、Ba2+、NO3-等4种离子,若向其中加入少量的Na2O2固体后溶液中离子浓度基本保持不变的是
A.HCO3-B.NO3-C.Ba2+D.Na+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com