
【题目】根据所学知识,完成题目:
(1)Ⅰ含氮的化合物在化学反应中变化复杂.现用如图3所示仪器(夹持装置己省略及药品,探究亚硝酸钠与硫酸反应及气体产物的成分.
已知:①NO+NO2+2OH﹣═2NO2﹣+H2O
②气体液化的温度:NO2 21℃、NO﹣152℃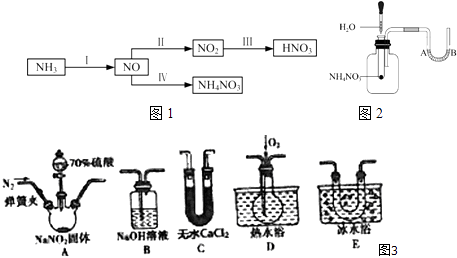
a.为了检验装置A中生成的气体产物,上述仪器的连接顺序(按左→右连接)为
b.反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是:
c.在关闭弹簧夹,滴入70%硫酸后,A中产生红棕色气体.
①盛装70%浓硫酸的仪器名称是
②实验确认有NO的现象是
d.通过上述实验探究过程,可得出装置A中反应的化学方程式是 .
(2)Ⅱ.NH3经一系列反应可以得到HNO3和NH4NO3 , 如图1所示.【资料卡片】
①NH4NO3是一种白色晶体,易溶于水,微溶于乙醇.
②在230℃以上时,同时有弱光:2NH4NO3=2N2↑+O2↑+4H2O
③在400℃以上时,剧烈分解发生爆炸:4NH4NO3=3N2↑+2NO2↑+8H2O
a.如图2将水滴入盛有硝酸铵的试管中,观察到的A处液面上升,B处液面下降,产生该现象的原因 .
b.实验室可以用氯化铵和熟石灰反应来制备氨气,该反应的化学方程式是(填“能”或“不能”)用硝酸铵代替氯化铵.
c.在汽车发生碰撞时,NaN3会产生(填化学式)气体充满安全气囊来减轻碰撞事故中乘员伤害程度.
d.完成离子反应IV:NO+H2O=++H+ .
【答案】
(1)A→C→E→D→B;防止装置中的空气将NO氧化成NO2 , 影响产物的检验;分液漏斗;D中刚开始为无色,通入O2后变为红棕色;2NaNO2+H2SO4(浓)=Na2SO4+NO↑+NO2↑+H2O
(2)NH4NO3溶于水时吸收热量;2NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O;不能;N2;8;7;3NH4+;5NO3﹣;2
CaCl2+2NH3↑+2H2O;不能;N2;8;7;3NH4+;5NO3﹣;2
【解析】(1)a.解:A中产生的气体中含有NO、NO2、水蒸气,所以先通过C吸收水蒸气,然后在E中冷却二氧化氮得到NO2 , 在D装置中检验NO的存在,NO、NO2都是大气污染物,所以最后在装置B中进行尾气处理,防止污染空气,故装置的连接为A→C→E→D→B,所以答案是:A→C→E→D→B;b.NO很容易被氧气氧化,装置中有空气,无法检验有NO生成,所以通氮气的目的是排尽整个装置中的空气,防止产生的NO被氧化生成NO2 , 所以答案是:防止装置中的空气将NO氧化成NO2 , 影响产物的检验;c.①盛装70%浓硫酸的仪器名称是分液漏斗,所以答案是:分液漏斗;②实验确认有NO的现象是D中刚开始为无色,通入O2后变为红棕色,所以答案是:D中刚开始为无色,通入O2后变为红棕色;d.通过上述实验探究过程,可得出装置A中反应产生 NO、NO2、水和硫酸钠,该装置中的化学方程式是2NaNO2+H2SO4(浓)=Na2SO4+NO↑+NO2↑+H2O,所以答案是:2NaNO2+H2SO4(浓)=Na2SO4+NO↑+NO2↑+H2O;(2)a.将水滴入盛有硝酸铵的试管中,观察到的A处液面上升,B处液面下降,产生该现象的原因是NH4NO3溶于水时吸收热量,使广口瓶中的气体压强减小,在大气压强的作用下U形管中的液体左侧A液面上升,右侧B液面下降,所以答案是:NH4NO3溶于水时吸收热量;b.实验室可以用氯化铵和熟石灰反应来制备氨气,该反应的化学方程式是2NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O;由于硝酸铵具有强的氧化性,而且分解分解产生大量气体而发生爆炸,所以不能代替NH4Cl来实验,所以答案是:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O;由于硝酸铵具有强的氧化性,而且分解分解产生大量气体而发生爆炸,所以不能代替NH4Cl来实验,所以答案是:2NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O;不能;c.在汽车发生碰撞时,NaN3会产生N2气体充满安全气囊来减轻碰撞事故中乘员伤害程度,所以答案是:N2;d.根据电子守恒、电荷守恒和原子守恒,可知离子反应IV NO发生歧化反应产生NH4+和NO3﹣ , 同时产生水,反应的方程式是:8NO+7H2O=3NH4++5NO3﹣+2H+ , 所以答案是:8;7;3NH4+;5NO3﹣;2.
CaCl2+2NH3↑+2H2O;不能;c.在汽车发生碰撞时,NaN3会产生N2气体充满安全气囊来减轻碰撞事故中乘员伤害程度,所以答案是:N2;d.根据电子守恒、电荷守恒和原子守恒,可知离子反应IV NO发生歧化反应产生NH4+和NO3﹣ , 同时产生水,反应的方程式是:8NO+7H2O=3NH4++5NO3﹣+2H+ , 所以答案是:8;7;3NH4+;5NO3﹣;2.


科目:高中化学 来源: 题型:
【题目】氯气是一种重要的化工原料.
(1)氯气是一种黄绿色气体,化学性质上和氧气有许多相似之处,比如:氯气也能支持燃烧,写出铁丝在氯气中燃烧的方程式: ______ ;氢气在氯气的燃烧观察的现象为: ______
(2)氯气和石灰乳反应可以制得漂白粉,漂白粉暴露在空气中因吸收了空气中的![]() 和
和![]() 而失效,漂白粉失效过程的化学反应方程式为: ______
而失效,漂白粉失效过程的化学反应方程式为: ______
(3)氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空![]() 、b、c、d中重合部分代表物质间反应,且氯水足量
、b、c、d中重合部分代表物质间反应,且氯水足量![]() .
.

![]() 过程的反应方程式 ______ , e过程中的化学方程式为 ______ .
过程的反应方程式 ______ , e过程中的化学方程式为 ______ .
![]() 过程所观察到的现象为: ______
过程所观察到的现象为: ______
b过程证明了氯水的存在 ______ 微粒
![]()
![]()
![]()
![]() .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验用品的使用或操作正确的是( )
A. 称量NaOH固体时,将NaOH直接放在托盘上的滤纸上
B. 容量瓶用于配制准确浓度的溶液,但不能作为反应容器使用
C. 保存汽油和苯等有机溶剂应选用细口瓶和橡胶塞
D. 用托盘天平称取11.72g食盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向2L的密闭容器中充入7.6mol NO和3.8mol O2 , 发生如下反应: ①2NO(g)+O2(g)2NO2(g)
②2NO2(g)N2O4(g)
测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T1℃,10min后升高并维持容器的温度为T2℃.下列说法正确的是( )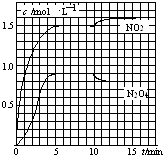
A.前5min反应的平均速率v(N2O4)=0.36mol(Lmin)﹣1
B.T1℃时反应②的化学平衡常数K=0.6
C.反应①、②均为吸热反应
D.若起始时向该容器中充入3.6mol NO2和2.0mol N2O4 , T1℃达到平衡时,N2O4的转化率为10%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Hagemann酶(H)是一种合成多环化合物的中间体,可由下列路线合成(部分反映条件略去):
(1)(A→B)为加成反应,则B的结构简式是;B→C的反应类型是 .
(2)H中含有的官能团名称是 , F的名称(系统命名)是 .
(3)E→F的化学方程式是 .
(4)TMOB是H的同分异构体,具有下列结构特征:①核磁共振氢谱除苯环吸收峰外仅有一个吸收峰;②存在甲氧基(CH3O﹣).TMOB的结构简式是 .
(5)下列说法正确的是 . a.A能和HCl反应得到聚氯乙烯的单体 b.D和F中均含有2个π健
c.1molG完全燃烧生成7mol H2O d.H能发生加成,取代反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制100mL1.0mol·L-1的NaOH溶液,下列情况会导致溶液浓度偏高的是( )
A.容量瓶使用前有少量蒸馏水
B.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒
C.在转移过程中有溶液撒在外面
D.俯视确定凹液面与刻度线相切
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当光束通过下列物质时,不会出现丁达尔效应的是( )
①Fe(OH)3胶体 ②水 ③蔗糖溶液 ④FeCl3溶液 ⑤云、雾
A. ②④⑤B. ③④⑤
C. ②③④D. ①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行下列实验,能达到实验目的的是 ( )
选项 | ① | ② | ③ | 实验结论 |
|
A | 浓硫酸 | 铜 | 溴水 | 验证浓硫酸具有强氧化性 | |
B | 浓盐酸 | 浓硫酸 | 空气 | 制取并收集HCl | |
C | 浓氨水 | 氧化钙 | 空气 | 制取并收集NH3 | |
D | 稀硫酸 | Na2CO3 | Na2SiO3 溶液 | 验证酸性:硫酸>碳酸>硅酸 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的K2SO4、NaCl、Ba(NO3)2、AgNO3混合均匀后,置于指定容器中,加入足量的水,搅拌、静置、过滤.取滤液,用铂电极电解一段时间.则两极区析出的氧化产物与还原产物的质量比约为( )
A.35.5:108
B.108:35.5
C.8:1
D.1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com