
【题目】已知A、B、D、E均为化学中的常见物质,它们之间的转化关系如图所示(部分产物略去),则下列有关物质的推断不正确的是( )

A. 若A是铁,则E可能为稀硝酸
B. 若A是CuO,E是碳,则B为CO
C. 若A是NaOH溶液,E是CO2,则B为NaHCO3
D. 若A是AlCl3溶液,E可能是氨水
【答案】D
【解析】试题分析:A、如果A是Fe,E为稀硝酸,B为Fe(NO3)3,D为Fe(NO3)2,Fe(NO)3和Fe反应生成Fe(NO3)2,Fe(NO3)2和硝酸反应生成Fe(NO3)3,符合转化关系,故说法正确;B、C+CuO=Cu+CO2,过量的C和CO2发生反应:C+CO2=2CO,因此B为CO,D为CO2,符合转化关系,故说法正确;C、2NaOH+CO2(少量))=Na2CO3+H2O,NaOH+CO2(过量)=NaHCO3、2NaHCO3![]() Na2CO3+CO2↑+H2O,Na2CO3+CO2+H2O=2NaHCO3,符合转化关系,故说法正确;D、氢氧化铝溶于强碱,不溶于弱碱,无论氨水是否过量,生成都是氢氧化铝沉淀,不符合转化关系,故说法错误。
Na2CO3+CO2↑+H2O,Na2CO3+CO2+H2O=2NaHCO3,符合转化关系,故说法正确;D、氢氧化铝溶于强碱,不溶于弱碱,无论氨水是否过量,生成都是氢氧化铝沉淀,不符合转化关系,故说法错误。


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
【题目】如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( ) 
A.W元素的第一电离能小于Y元素的第一电离能
B.Y、Z的阴离子电子层结构都与R原子的相同
C.p能级未成对电子最多的是Z元素
D.X元素是电负性最大的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制玻璃时,发生的主要反应的化学方程式为: ![]()
![]()
![]()
完成下列填空:
(1)钠原子核外具有______种不同能量的电子,钠元素在周期表中的位置为____________。
(2)在上述反应中,反应物和生成物的晶体类型共有_____种,写出气体产物的电子式_______________。
(3)上述物质中的非金属元素原子半径由大到小顺序为___________(用元素符号表示),下列能判断它们的非金属性强弱的依据是:________(选填编号)。
a. 气态氢化物的熔沸点 b. 最高价氧化物对应水化物的酸性
c. 气态氢化物的热稳定性 d. 三种元素两两形成的化合物中电子对偏向
(4)常温下,相同物质的量浓度的![]() 和
和![]() 溶液中,
溶液中, ![]() _____
_____ ![]() (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(5)向10mL一定浓度的![]() 溶液中逐滴加入0.1mol/L的稀盐酸,加入盐酸的体积与产生气体的体积有如图关系。由此可知原
溶液中逐滴加入0.1mol/L的稀盐酸,加入盐酸的体积与产生气体的体积有如图关系。由此可知原![]() 溶液的物质的量浓度为__________。在滴入盐酸的整个过程中,溶液中
溶液的物质的量浓度为__________。在滴入盐酸的整个过程中,溶液中![]() 的变化情况是______________。
的变化情况是______________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羚羊角或犀牛角是治疗创伤的中药方剂中用量极少的成分,但是缺少这味药,疗效将大大下降甚至无效。已知动物的角主要由死亡细胞的角化(变性)蛋白质组成,则羚羊角等的有效成分最可能是( )
A. 特殊活性的蛋白质
B. DNA
C. 微量元素
D. 大量元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
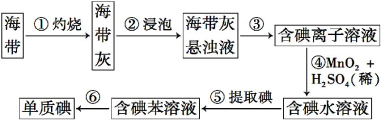
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是_________(从下列仪器中选出所需的仪器,用标号字母填写空白处)。
A.烧杯
B.坩埚
C.表面皿
D.泥三角
E.酒精灯
F.干燥器
(2)步骤③的实验操作名称是 ;步骤⑥的目的是从含碘的苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是 。
(3)步骤④反应的离子方程式是 。
(4)步骤⑤中,某学生选择用苯来提取碘的理由是 。
(5)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铬是用途广泛的金属元素.
(1)工业生产过程中易产生有害的含铬废水,含铬废水中存在下列平衡:Cr2O72﹣(橙色)+H2O2CrO42﹣(黄色)+2H+ . 处理该废水常用还原沉淀法,其流程如图所示.
已知:Ksp[Fe(OH)3]=4.0×10﹣38 , Ksp[Cr(OH)3]=6.0×10﹣31
含铬废水 ![]() 含Cr2O
含Cr2O ![]() 的沸水
的沸水 ![]() 含Cr3+的沸水
含Cr3+的沸水 ![]() Cr(OH)3沉淀
Cr(OH)3沉淀
①Cr2O72﹣中铬元素化合价为 .
②第I步转化控制溶液的pH=2,该溶液显色.
③第Ⅲ步沉淀反应后,溶液中c(Fe3+)=2.0×10﹣12 molL﹣1 , 则c(Cr3+)=molL﹣1 .
(2)室温下,初始浓度为1.0molL﹣1的Na2CrO4溶液中c(Cr2O72﹣)随c(H+)的变化如图所示.
①用离子方程式表示Na2CrO4溶液中的转化反应 .
②根据A点数据,计算该反应的平衡常数值为 . 由图可知,溶液酸性增强,CrO42﹣平衡转化率(填“增大”“减小”或“不变”).
③升高温度,溶液中CrO42﹣的平衡转化率减小,则该反应的△H0(填“大于”“小于”或“等于”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】小苏打是一种常用的食品添加剂。
(1)精制食盐是制备小苏打的原料之一。粗盐中含有少量Ca2+、Mg2+、SO42-,粗盐精制的步骤顺序是:溶解→ → → → (填字母编号)。_____________
a.加盐酸调pH b.加Ba(OH)2溶液 c.加Na2CO3溶液 d.过滤
(2)NH3、CO2先后通入饱和食盐水中,反应的离子方程式________________。
(3)侯氏制碱法中,母液的处理方法是通入氨气,再加入细小食盐颗粒,最后冷却析出的副产品是_______;简述通氨气的作用____________________________________。
(4)称取2.640 g小苏打样品(含少量NaCl),配置成250 mL溶液,准确取出20.00 mL溶液于锥形瓶中,滴加_______作指示剂,滴定时消耗0.1000 mol/L盐酸的体积为20.67 mL。则该样品中碳酸氢钠的质量分数为_________(保留两位小数)。若装标准溶液的滴定管没有润洗,则测得的结果会____(填“偏大”、“偏小”或“不变”)。
(5)测定上述样品中碳酸氢钠的质量分数还可通过如图装置进行测定。实验需使用的定量仪器是_____;写出涉及的化学方程式__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中,元素组成都相同的一组是( )
A. 糖原、胰岛素、纤维素 B. 磷脂、核糖核酸、脱氧核糖
C. 淀粉、乳糖、脂肪 D. 抗原、抗体、血红蛋白
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com