
【题目】常温下,pH=10的X、Y两种碱溶液各1mL,分别加水稀释到100mL,其pH与溶液体积(V)的关系如图所示,下列说法正确的是( ) 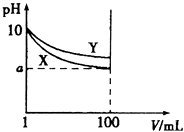
A.稀释前,两种碱溶液中溶质的物质的量浓度一定相等
B.稀释后,X溶液的碱性比Y溶液的碱性强
C.完全中和X、Y溶液时,消耗同浓度盐酸的体积VX>VY
D.若8<a<10,则X、Y都是弱碱
【答案】D
【解析】解:由图象可知,pH=10的碱稀释100倍,X变化大,则Y一定是弱碱,X碱性比Y强,若a=8,则X为强碱, A.Y的碱性弱,pH相同时,Y的浓度大,则稀释前,两种碱溶液中溶质的物质的量浓度不相等,故A错误;
B.稀释后,Y中OH﹣浓度大,X溶液的碱性比Y溶液的碱性弱,故B错误;
C.Y的碱性弱,pH相同时,Y的浓度大,等体积时Y的物质的量大,则完全中和X、Y溶液时,消耗同浓度盐酸的体积VX<VY , 故C错误;
D.a=8,则X为强碱,若8<a<10,则X、Y都是弱碱,故D正确;
故选D.
碱溶液加水稀释,氢氧根离子浓度不断减小,pH不断减小,但弱碱存在电离平衡,加水稀释促进电离,氢氧根离子浓度减小的慢,故pH也减小的慢,所以Y一定是弱碱,X碱性比Y强,若a=8,则X为强碱,以此来解答.


科目:高中化学 来源: 题型:
【题目】某学生研究小组欲探究CuSO4溶液与Na2CO3溶液混合产生的蓝绿色沉淀组成,小组进行下列实验探究。
【提出假设】
假设1:沉淀为Cu(OH)2
假设2:沉淀为_________
假设3:沉淀为碱式碳酸铜[化学式可表示为nCuCO3mCu(OH)2]
【查阅资料】无论是哪一种沉淀受热均易分解(假设均不含结晶水)。
【物质成分探究】
步骤1:将所得悬浊液过滤,用蒸馏水洗涤,再用无水乙醇洗涤
步骤2:甲同学取一定量固体,用气密性良好的下图装置(夹持仪器未画出)进行定性实验。
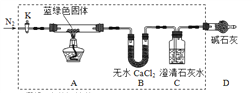
请回答下列问题:
(1)假设2中的沉淀为___________________。
(2)假设1中沉淀为Cu(OH)2的理论依据是(用离子方程式表示)____________。
(3)无水乙醇洗涤的目的_______________________________________。
(4)若反应后A中蓝绿色固体变黑,C中无明显现象,证明___________成立。(填写“假设1” “假设2”或“假设3”)。
(5)乙同学认为只要将上图中B装置的试剂改用______试剂后,便可验证上述所有假设。
(6)乙同学更换B试剂后验证假设3成立的实验现象是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据下图中氮元素及其化合物的转化关系,回答问题:
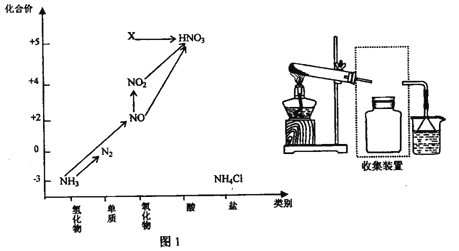
(1)实验窒常用NH4Cl 与Ca(OH)2制取氨气,该反应的化学方程式为___________。
(2)若要收集一瓶氨气,请将下列装置补充完整,在虚框内画出连接图。___________
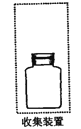
(3)下列试剂不能用手干燥NH3的是_________。
A.浓硫酸 B.碱石灰 C.NaOH 固体
(4)工业上以NH3、空气、水为原料生产硝酸分为三步:
①NH3→NO 化学方程式为____________。
②NO→NO2 实验现象是_______ 。
③ NO2![]() HNO3 氧 化剂 与 还原剂物质的量之比为_______。
HNO3 氧 化剂 与 还原剂物质的量之比为_______。
(5)图1中,实验室只用一种物质将NO 直接转化为硝酸且绿色环保,则该物质的化学式为_____________,
(6) 图1中,X的化学式为__________,从物质性质上看,X 属于_______氧化物。
(7)若要将NH3→N2,,从原理上看,下列试剂可行的是_______。
A.O2 B.Na C.NH4Cl D.NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将足量的二氧化锰与40 mL10 mol·L-1浓盐酸反应产生的氯气同0.1 mol二氧化锰与足量的浓盐酸反应产生的氯气相比
A. 两者产生的氯气一样多 B. 前者产生的氯气的量是后者的2倍
C. 后者产生的氯气的量比前者多 D. 后者产生的氯气的量是前者的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质应用的说法正确的是
A. 生石灰用作食品抗氧化剂 B. 盐类都可用作调味品
C. 铝罐可久盛食醋 D. 小苏打是面包发酵粉的主要成分之一
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一定质量的氯化钠、溴化钠、碘化钠的混合物平均分成五等份,分别加水配成溶液并编号为甲、乙、丙、丁、戊,再分别向各溶液中通入一定体积的氯气,将反应后所得溶液蒸干,灼烧固体。通入氯气的量与最终所得固体质量记录如下:
编号 | 甲 | 乙 | 丙 | 丁 | 戊 |
固体组成 | NaI、NaBr、NaCl | NaBr、NaCl | NaCl | ||
氯气的体积/ml | V | 2V | 3V | 4V | 5V |
固体质量/g | 54.62 | 43.64 | 35.48 | 30.14 | 29.25 |
求:(1)请填写表中空白______________、____________;
(2)标准状况下氯气的体积V为_______,原混合物中溴化钠的物质的量为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素性质呈周期性变化的决定因素是______
A.元素原子半径大小呈周期性变化
B.元素的相对原子质量依次递增
C.元素原子核外电子排布呈周期性变化
D.元素的最高正化合价呈周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下存在反应C(s)+H2O(g)![]() CO(g)+H2(g) △H>0,向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示。下列说法错误的是( )
CO(g)+H2(g) △H>0,向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示。下列说法错误的是( )
容器 | 甲 | 乙 | 丙 |
容积 | 0.5 L | 0.5 L | V |
温度 | T1℃ | T2℃ | T1℃ |
起始量 | 2 molC 1 molH2O | 1 molCO 1 molH2 | 4 molC 2molH2O |
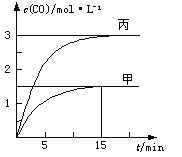
A. 甲容器中,反应在前15 min的平均速率v(H2)=0.1mol·L-1·min-1
B. 丙容器的体积V>0.5 L
C. 当温度为T1℃时,反应的平衡常数K=4.5
D. 乙容器中,若平衡时n(H2O)=0.4 mol,则T2< T1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com