
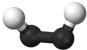
 aA、bB、cC、dD四种短周期元素,它们的原子序数有如下关系:c-b=b-a=1 且 b+c=d,B的最高价氧化物对应水化物为强酸.
aA、bB、cC、dD四种短周期元素,它们的原子序数有如下关系:c-b=b-a=1 且 b+c=d,B的最高价氧化物对应水化物为强酸.
| ||
| ||


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| t/K | 298 | 398 | 498 | … |
| K/(mol?L-1)-2 | 4.1×106 | 8.2×107 | K1 | … |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com