
【题目】向10.0mL 0.10molL﹣1氨水中滴入0.10molL﹣1的盐酸,溶液的pH与所加盐酸的体积关系如图所示(假设无气体逸出),下列有关叙述正确的是( ) 
A.M﹣N间一定存在c(Cl﹣)>c(NH4+)>c(OH﹣)>c(H+)
B.M点对应的盐酸体积为10.0mL
C.pH=7溶液中有c(NH4+)=c(Cl﹣)=c(H+)=c(OH﹣)
D.P点处的溶液中存在:2c(NH4+)+2c(NH3H2O)=c(Cl﹣)
科目:高中化学 来源: 题型:
【题目】根据题意解答
(1)将锌片和银片用导线相连浸入稀硫酸中组成原电池.若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干澡后称重,总质量为47g,试计算产生氢气的体积(标准状况) .
(2)利用下列反应:Fe+2Fe3+=3Fe2+ , 设计一个化学电池(给出若干导线和一个小灯泡,电极材料和电解液自选):负极电极反应;正极材料 , 正极电极反应 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.某有机物燃烧只生成CO2和H2O,且二者物质的量相等,则此有机物的组成为CnH2n
B.一种烃在足量的氧气中燃烧并通过碱石灰,减少的体积就是生成水蒸气的体积
C.某气态烃CxHy与足量O2恰好完全反应,如果反应前后气体体积不变(温度>100℃),则y=4,若体积减少,则y>4,否则y<4
D.相同质量的烃,完全燃烧,消耗的O2越多,则烃中氢元素的百分含量越高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外活动小组通过实验研究NO2的性质. 已知:2NO2+2NaOH═NaNO3+NaNO2+H2O
利用图1所示装置探究NO2能否被NH3还原(K1、K2为止水夹,夹持固定装置略去)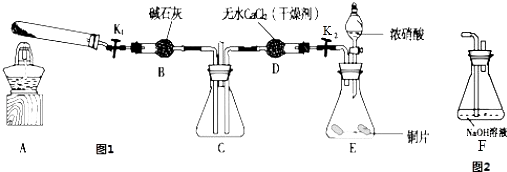
(1)该实验中制取氨气时若只用一种试剂,从下列物质中选取 a.NH4HCO3 b.NH4Cl c.浓氨水
(2)若NO2能够被NH3还原,预期观察到C装置中的现象是 .
(3)此实验装置存在一个明显的缺陷是 .
(4)探究NO2能否与Na2O2发生氧化还原反应.为了验证NO2能被Na2O2氧化,该小组同学选用B、D、E装置,将B中的药品更换为Na2O2 , 另选F装置(如图2所示),重新组装,进行实验,装置的合理连接顺序是
(5)实验过程中,B装置中淡黄色粉末逐渐变成白色.经检验该白色物质为纯净物,且无其他物质生成.推测B装置中反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用.下表列出了①~⑩九种元素在周期表中的位置.
族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | O |
1 | ① | ⑩ | ||||||
2 | ⑥ | ⑦ | ||||||
3 | ② | ③ | ④ | ⑧ | ||||
4 | ⑤ | ⑨ |
请回答:(以下用相应的元素符号回答问题)
(1)在表里填写①~⑩元素符号,写出元素符号①、③、⑧ .
(2)其中化学性质最不活泼的是(填元素符号).
(3)在②、③、④三种元素的氧化物对应的水化物中,碱性最强的是(填化学式).
(4)元素①、②、⑤按原子半径由大到小的顺序依次为(填元素符号)
(5)元素⑥的氢化物的化学式是 , 该氢化物溶于水,所得溶液的pH(填“<”、“>”或“=”)7.
(6)元素②与元素⑧形成的化合物的电子式是 , 高温下灼烧该化合物火焰呈色.
(7)(填化学式)的单质既可以和盐酸又可以和氢氧化钠溶液反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用Cl2生产某些含氯有机物时会产生副产物HCl.利用反应A,可实现氯的循环利用.
反应A:4HCl+O2 ![]() 2Cl2+2H2O
2Cl2+2H2O
已知:I.反应A中,4molHCl被氧化,放出115.6kJ热量.
II. 
判断下列说法正确的是( )
A.反应A的△H>﹣115.6kJmol﹣1
B.H2O中H﹣O键比HCl中H﹣Cl键弱
C.由II中的数据判断氯元素的非金属性比氧元素强
D.断开1molH﹣O键与断开1molH﹣Cl键所需能量相差31.9kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com