

分析 (1)Al3+水解生成的Al(OH)3胶体,具有吸附性;
(2)NH4Al(SO4)2水解,溶液呈酸性,升高温度其水解程度增大;
(3)①a、b、c、d四个点,根据反应量的关系,a点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4;
②b点溶液呈中性,即溶液含有(NH4)2SO4、Na2SO4、NH3•H2O三种成分,所以b点时c(Na+)>c(SO42-),根据N元素与S元素的关系,可以得出c(SO42-)>c(NH4+),据此分析.
解答 解:(1)Al3+水解生成的Al(OH)3胶体,具有吸附性,离子方程式:Al3++3H2O?Al(OH)3胶体+3H+,
故答案为:Al3+水解生成的Al(OH)3胶体,具有吸附性,即Al3++3H2O?Al(OH)3胶体+3H+,Al(OH)3吸附悬浮颗粒使其沉降从而净化水;
(2)NH4Al(SO4)2水解,溶液呈酸性,升高温度其水解程度增大,pH减小,符合的曲线为Ⅰ,
故答案为:Ⅰ;NH4Al(SO4)2水解,溶液呈酸性,升高温度,其水解程度增大,pH减小;
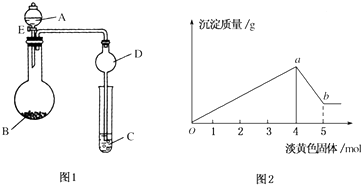
(3)①a、b、c、d四个点,根据反应量的关系,a点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4,b、c、d三点溶液均含有NH3•H2O,(NH4)2SO4可以促进水的电离,而NH3•H2O抑制水的电离,所以a水的电离程度最大,则在a点,反应的离子方程式为Al3++3OH-=Al(OH)3↓,故答案为:a;Al3++3OH-=Al(OH)3↓;
②b点溶液呈中性,即溶液含有(NH4)2SO4、Na2SO4、NH3•H2O三种成分,所以Al3+已经完全沉淀,故A正确,C错误;
b点溶液呈中性,b点时c(Na+)>c(SO42-),根据N元素与S元素的关系,可以得出c(SO42-)>c(NH4+),故c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+),故B正确;
又b点溶液呈中性,即溶液含有(NH4)2SO4、Na2SO4、NH3•H2O三种成分,则氢氧化钠不仅使铝离子沉淀还与部分铵根生成了氨水,所以消耗的NaOH溶液体积大于$\frac{0.1×0.1×3}{0.1}$L=300mL,故D正确;
故选:ABD.
点评 本题考查盐类的水解和离子浓度大小的比较,题目难度较大,(3)②为易错点,注意根据守恒思想解题.


 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | O2 | B. | Cl2 | C. | HCl | D. | H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A. | 1 mol•L-1的溶液中,pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) | |
| B. | 升高温度,HCN溶液中H+浓度增大,平衡正向移动,电离平衡常数增大 | |
| C. | 向稀醋酸中逐滴加水,或加入少量冰醋酸,CH3COOH的电离平衡都正向移动 | |
| D. | 向CH3COOH溶液中加入少量氢氧化钠固体,平衡正向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 实验方案(不要求写出具体操作过程) | 预期实验现象和结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 实验室制NH3:NH4++OH-$\frac{\underline{\;△\;}}{\;}$NH3↑+H2O | |
| B. | NaOH与NH4Cl溶液混合加热:NH4++OH-$\frac{\underline{\;△\;}}{\;}$NH3•H2O | |
| C. | 氨水中加盐酸:NH3•H2O+H+═NH4++H2O | |
| D. | 氨气通入稀H2SO4中:NH3+H+═NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入无水CuSO4,再过滤 | |
| B. | 加入生石灰,再蒸馏 | |
| C. | 加入浓H2SO4,再加热,蒸出乙醇 | |
| D. | 将96%的乙醇溶液直接加热蒸馏出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸式盐的水溶液一定显碱性 | |
| B. | 只要酸和碱的物质的量浓度和体积分别相等,它们反应后的溶液就呈中性 | |
| C. | 纯水呈中性是因为水中氢离子的物质的量浓度和氢氧根离子的物质的量浓度相等 | |
| D. | 碳酸溶液中氢离子的物质的量浓度是碳酸根离子的物质的量浓度的2倍 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com