
| A. | pH=0的溶液中:NO3-、SO42-、Na+、I-能大量共存 | |
| B. | 0.1mol•L-1Na2S溶液中:c(Na+)=2c(S2-) | |
| C. | NaHSO3溶液中:c(HSO3-)+c(OH-)+c(SO32-)=c(H+)+c(Na+) | |
| D. | 等体积的硝酸和氨水混合可能存在:c(NO3-)=c(NH4+) |
分析 A.pH=0的溶液,显酸性,离子之间发生氧化还原反应;
B.硫离子水解;
C.溶液遵循电荷守恒;
D.等体积的硝酸和氨水混合可能显中性.
解答 解:A.pH=0的溶液,显酸性,SO42-、H+、I-发生氧化还原反应,不能共存,故A不选;
B.硫离子水解,则0.1mol•L-1Na2S溶液中:c(Na+)>2c(S2-),故B不选;
C.溶液遵循电荷守恒,则存在c(HSO3-)+c(OH-)+2c(SO32-)=c(H+)+c(Na+),故C不选;
D.等体积的硝酸和氨水混合可能显中性,c(OH-)=c(H+),结合电荷守恒可知,c(NO3-)=c(NH4+),故D选;
故选D.
点评 本题考查离子共存及溶液中离子浓度关系,为高频考点,把握习题中的信息及常见离子之间的反应、盐类水解、电荷守恒为解答的关键,侧重分析与应用能力的考查,注意氧化还原反应的判断,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 化学反应速率变化时,化学平衡一定发生移动 | |
| B. | 化学平衡发生移动时,化学反应速率一定变化 | |
| C. | 正反应进行的程度大,正反应速率一定大 | |
| D. | 化学反应速率变化而化学平衡不移动的情况,只有使用催化剂条件下才会发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑤ | B. | ②⑤⑦⑧ | C. | ③④⑥⑦ | D. | ②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在实验室中可以用己烯通过萃取提取溴水中的溴单质 | |
| B. | 在一定条件下乙烯可被氧化成乙醇,乙醇可以被氧化为乙酸 | |
| C. | lmol葡萄糖能水解生成2molCH3CH2OH和2molCO2 | |
| D. | 乙烯使酸性高锰酸钾溶液褪色与乙烯使溴水褪色的原理不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  图中,Zn-MnO2干电池放电时,MnO2被氧化 | |
| B. |  图中,电解精炼铜时,阳极减少的质量与阴极增加的质量一定相等 | |
| C. |  图中,在钢材上电镀铝,熔融盐中Al和Cl元素只以AlCl4-、Al2Cl7-形式存在,则阳极反应式为:Al-3e-+7AlCl4-=4Al2Cl7- | |
| D. |  图中,K分别与M、N连接,均可保护Fe电极,连接M时为“牺牲阳极的阴极保护法” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、NO3-、CO32-、Na+ | B. | NO3-、Ba2+、K+、Cl- | ||
| C. | Al3+、Ba2+、Mg2+、HCO3- | D. | NO3-、K+、SO32-、H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
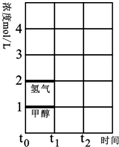 工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H.如表所列数据是该反应在不同温度下的化学平衡常数(K).
工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H.如表所列数据是该反应在不同温度下的化学平衡常数(K).| 温度 | 250℃ | 300℃ | 350℃ |
| K/L2•mol-2 | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H单位中的每摩尔指的既不是每摩尔C4H10,也不是其他反应物或生成物,而是每摩尔反应 | |
| B. | 该反应的△H与各物质的状态有关,与化学计量数也有关 | |
| C. | 该式的含义为:25℃、101 kPa下,2 mol C4H10气体完全燃烧生成CO2和液态水时放出热量5 800 kJ | |
| D. | 该反应为丁烷燃烧的热化学方程式,由此可知丁烷的燃烧热为5 800 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2通入品红溶液,品红溶液褪色,说明Cl2有漂白性 | |
| B. | 向久置的Na2SO3溶液中加入足量BaCl2溶液,出现白色沉淀;再加入足量稀盐酸,部分沉淀溶解,说明部分Na2SO3被氧化 | |
| C. | Fe与稀HNO3溶液、稀H2SO4溶液反应均有气泡产生,说明Fe与两种酸均发生置换反应 | |
| D. | 向溶液中加NaOH溶液后加热,产生使湿润的蓝色石蕊试纸变红的气体,说明原溶液中含有NH4+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com