
【题目】下列酸溶液的pH相同时,其物质的量浓度最小的是
A. H2SO4 B. H2SO3 C. CH3COOH D. HNO3
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】不用其他试剂,用最简单的方法鉴别下列物质 ①NaOH溶液 ②Mg(NO3)2溶液 ③CuSO4溶液 ④KCl溶液;
正确的鉴别顺序是( )
A.①②③④
B.③④②①
C.④①②③
D.③①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】20℃时,在H2C2O4、NaOH混合溶液中,c(H2C2O4)-c(HC2O4-)+c(C2O42-)=0.100mol/L。含碳元素微粒的分布分数δ随溶液pH变化的关系如图所示。下列说法正确确是
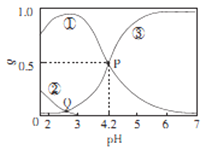
A. ①表示H2C2O4的分布曲线,③表示C2O42-的分布曲线
B. 20℃时,H2C2O4的二级电离平衡常数Ka=1×10-4.2
C. Q点对应溶液中lgc(H+)<lgc(OH-)
D. 0.100mol/L的NaHC204溶液中:c(OH-)=c(H+)-2c(C2042-)+c(H2C2O4)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃ 时,用0.10mol·L-1的盐酸分别滴定体积相同且浓度均为0.10mol·L-1的三种一元碱XOH、YOH及ZOH,滴定曲线如图所示。

下列说法正确的是( )
A. YOH是强碱 B.  =0.5时,c(Z+)>c(Y+)>c(X+)
=0.5时,c(Z+)>c(Y+)>c(X+)
C. X++H2O![]() XOH+H+的平衡常数K=10-4 D. 滴定XOH时可用酚酞作指示剂
XOH+H+的平衡常数K=10-4 D. 滴定XOH时可用酚酞作指示剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】难挥发性二硫化钽(TaS2)可采用如下装置提纯。将不纯的TaS2粉末装入石英管一端,抽真空后引入适量碘并封管,置于加热炉中。反应如下:TaS2(s)+2I2(g) ![]() TaI4(g)+S2(g)下列说法正确的是
TaI4(g)+S2(g)下列说法正确的是

A. 在不同温度区域,TaI4的量保持不变
B. 在提纯过程中,I2的量不断减少
C. 在提纯过程中,I2的作用是将TaS2从高温区转移到低温区
D. 该反应的平衡常数与TaI4和S2的浓度乘积成反比
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与 Y同族,Z 与X 形成的离子化合物的水溶液呈中性。下列说法正确的是
A. 简单离子半径:W<X<Z
B. W与X形成的化合物溶于水后溶液呈碱性
C. 气态氢化物的热稳定性:W<Y
D. 最高价氧化物的水化物的酸性:Y>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. ![]() 和
和![]() 是中子数不同质子数相同的同种核素
是中子数不同质子数相同的同种核素
B. 质子数为 53,中子数为 78 的碘原子:![]()
C. 同种元素的原子均有相同的质子数和中子数
D. 通过化学变化可以实现 16O 与 18O 间的相互转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铁,黑棕色结晶,熔点306℃、沸点315℃,易升华;FeCl3易溶于水且具有强烈的吸水性。某化学兴趣小组利用如下装置(夹持仪器略去)制备氯化铁晶体 ( FeCl3.6H2O)。
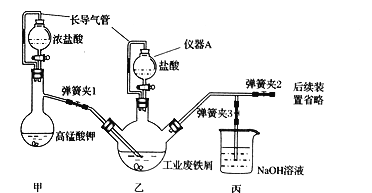
(1)仪器A的名称是 ____,在该实验中长导气管的作用是____,同时防止盐酸挥发污染环境。
(2)装置甲中发生反应的离子方程式为 ____,装置丙的作用为__________________ 。
(3)为顺利达成实验目的,实验过程中先关闭弹簧夹l和3,打开弹簧夹2,再打开乙装置中的活塞,待铁粉完全溶解后,关闭乙中的活塞,___ 再打开甲中的活塞。
(4)在实验过程中判断乙瓶中铁元素完全转化成氯化铁的方法是:取试样于试管中,然后向试管中力口入 __(填试剂)后观察现象。
(5)反应结束后,将乙中溶液边加入____,边进行加热浓缩、____、过滤、洗涤、干燥即得到产品。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的数值,下列说祛正确的是
A. 24gMg与足量N2反应生成Mg3N2,转移的电子数为6NA
B. lmolNa218O2中所含的中子数为42NA
C. 9.8g由H2SO4和H3PO4组成的混合物中含有的氧原子数为0.4NA
D. 1mol环已烷中含有的共价键数为12NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com