
【题目】我国明代《本草纲目》记载了烧酒的制造工艺:“凡酸坏之酒,皆可蒸烧”,“以烧酒复烧二次……价值数倍也”。这里用到的可用于分离的实验方法是
A. 萃取 B. 蒸馏 C. 过滤 D. 分液
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,回答下列问题: 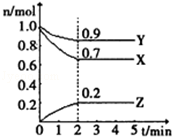
(1)该反应在min时达到化学平衡状态.
(2)该反应的化学方程式是 .
(3)从开始到2min,Z的平均反应速率是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素原子价电子排布式为3d54s2,下列说法正确的是
A.该元素位于周期表ds区
B.该元素的最高化合价为 +5价
C.该元素位于第四周期第VB族
D.该元素的某些氧化物可用作催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭的2L的容器里装有4mol SO2和2mol O2 , 在一定条件下开始反应.2min末测得容器中共有5.2mol 气体,试计算:
(1)2min末SO3气体的物质的量浓度;
(2)2min内O2的平均反应速率v(O2);
(3)2min末SO2的转化率.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应CH3OH(l)+NH3(g)===CH3NH2(g)+H2O(g)在某温度自发向右进行,若反应的|ΔH|=17 kJ·mol-1,|ΔH-TΔS|=17 kJ·mol-1,则下列正确的
A.ΔH>0,ΔH-TΔS<0 B.ΔH<0,ΔH-TΔS>0
C.ΔH>0,ΔH-TΔS>0 D.ΔH<0,ΔH-TΔS<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D均为短周期元素,A和B是同周期相邻的两种元素,A和C是同主族相邻的两种元素,A、B、C三种元素的原子序数之和为31,D元素与A、B、C三种元素既不同周期,也不同主族,请回答:
(1)C元素在元素周期表中的位置是;
(2)A、B、D可组成一种离子化合物,是常见的化肥,其化学式为;
(3)A2和D2两种物质可以构成一种新型的原电池,若原电池中电解质溶液为KOH溶液,则正极的电极反应式为;
(4)若将一充满20mLBA2和A2混合气体的大试管倒立于D2A中,充分反应后,在相同条件下,测得试管中余下5mL无色气体,则原混合气体中BA2和A2物质的量之比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定物质的主要成分与化学式对应正确的是
A. 沼气——CH4 B. 碱石灰——Na2CO3
C. 漂白粉——CaCl2 D. 明矾——CuSO4·5H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com