
����ѭ���ֽ�ˮ������Ҫ�漰���з�Ӧ��
��.SO2��2H2O��I2=H2SO4��2HI
��.2HI H2����I2
H2����I2
��.2H2SO4=2SO2��O2����2H2O
(1)����������Ӧ�������ж���ȷ���� ��
a����Ӧ�����ڳ����½���
b����Ӧ����SO2�����Ա�HIǿ
c��ѭ���������貹��H2O
d��ѭ�������в���1 mol O2��ͬʱ����1 mol H2
(2)һ���¶��£���1 L�ܱ������м���1 mol HI(g)��������Ӧ��H2�����ʵ�����ʱIP��ı仯��ͼ��ʾ��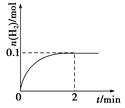
��0��2 min�ڵ�ƽ����Ӧ����v(HI)�� ��
����ͬ�¶��£�����ʼ����HI(g)�����ʵ�����ԭ����2������ ��ԭ����2����
a��HI��ƽ��Ũ��
b���ﵽƽ���ʱ��
c��ƽ��ʱH2���������
(3)ʵ������Zn��ϡ������ȡH2���������������й����Լ��е� ������H2�����ʽ�����
a��NaNO3 b��CuSO4 c��Na2SO4 d��NaHSO3

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
(9��)��֪A(g)+B(g)  C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
| |�¶�/ �� | 700 | 900 | 830 | 1000 | 1200 |
| ƽ�ⳣ�� | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
 A(g)+B(g)��ƽ�ⳣ����ֵΪ ��
A(g)+B(g)��ƽ�ⳣ����ֵΪ ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
һ���¶��£���һ��10 L�ܱ������з���ij���淴Ӧ����ƽ�ⳣ������ʽΪK�� ����ش��������⡣
����ش��������⡣
(1)�÷�Ӧ�Ļ�ѧ����ʽΪ__________________________________________��
���¶����ߣ�K������÷�Ӧ��________��Ӧ(����ȡ����ȡ�)��
(2)���жϸ÷�Ӧһ���ﵽƽ��״̬����________(����ĸ���)��
| A��v��(H2O)��v��(H2) |
| B�������������ƽ����Է�����������ʱ��ı� |
| C������n mol H2��ͬʱ����n mol CO |
| D�����������ʵ������ʵ�������ʱ��ı� |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�״���ͨ����ú�������������ɵ�CO��H2��һ�������£��������·�Ӧ�Ƶã�CO(g)��2H2(g)  CH3OH(g)�������ͼʾ�ش��������⣺
CH3OH(g)�������ͼʾ�ش��������⣺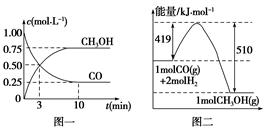
(1)�ӷ�Ӧ��ʼ��ƽ�⣬��H2Ũ�ȱ仯��ʾƽ����Ӧ����v(H2)�� ��CO��ת����Ϊ ��
(2)�÷�Ӧ��ƽ�ⳣ������ʽΪ ���¶����ߣ�ƽ�ⳣ�� (���������С�����䡱)��
(3)����һ����ɱ���ܱ������г���1 mol CO��2 mol H2��1 mol CH3OH���ﵽƽ��ʱ��û��������ܶ���ͬ��ͬѹ����ʼ��1.6�������������ʺ�÷�Ӧ�� (����������桱)��Ӧ�����ƶ��������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��һ��������ܱ�������,�������»�ѧ��Ӧ:CO2(g)+H2(g) CO(g)+H2O(g),�仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���ʾ:
CO(g)+H2O(g),�仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���ʾ:
| t/�� | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ij�¶�ʱ��2L������X��Y��Z������̬���ʵ����ʵ�����n����ʱ�䣨t���仯��������ͼ��ʾ����ͼ�����ݷ�����
��1���÷�Ӧ�Ļ�ѧ����ʽΪ��
��2����Ӧ��ʼ��2min����X��ʾ��ƽ����Ӧ����Ϊ��
��3������������˵��������Ӧ�ﵽ��ѧƽ��״̬���� ������ĸ��
A���������������ʵ�������ʱ��ı仯���仯
B����λʱ����ÿ����3mol X��ͬʱ����2mol Z
C��������������������ʱ��ı仯���仯
��4�����ܱ������ͨ��a mol X(g)��b mol Y(g)��������ӦX(g��+ Y(g��=2Z(g)�����ı���������ʱ����Ӧ���ʻᷢ��ʲô�仯��ѡ������� ��С�� ���䡱��
�� �����¶ȣ�
�ڱ���������������䣬����X(g)�����ʵ�����
�� ���������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��0.1 mol MnO2��ĩ��50 mL��������(H2O2���ѣ�1.1 g�� mL��1)�У��ڱ�״���·ų�����������ʱ��Ĺ�ϵ��ͼ��ʾ��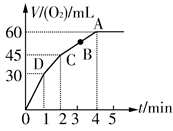
(1)ʵ��ʱ�ų�������������_____________________________��
(2)�ų�һ����������ʱ��Ϊ_______________________________��
(3)��Ӧ�ų������������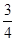 �����ʱ��ԼΪ__________________
�����ʱ��ԼΪ__________________
(4)A��B��C��D���㷴Ӧ���ʿ�����˳��Ϊ____________________
(5)���ͷ�Ӧ���ʱ仯��ԭ��___________________________________________________
(6)����H2O2�ij�ʼ���ʵ���Ũ��____________________
(7)��Ӧ��2 minʱ��H2O2����������_________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��2 L�ܱ������У�800��ʱ��Ӧ2NO��g����O2��g�� 2NO2��g����ϵ�У�n��NO����ʱ��ı仯�����
2NO2��g����ϵ�У�n��NO����ʱ��ı仯�����
| ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n��NO��/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
���п���֤��H2(g)+I2(g) 2HI(g)�Ѵ�ƽ��״̬��������������
2HI(g)�Ѵ�ƽ��״̬��������������
�ٵ�λʱ��������n mol H2��ͬʱ,����n mol HI
��һ��H��H�����ѵ�ͬʱ������H��I������
�۰ٷֺ���w(HI)=w(I2)
�ܷ�Ӧ����v(H2)=v(I2)=v(HI)
��c(HI)��c(H2)��c(I2)=2��1��1
���¶Ⱥ����һ��ʱ,������Ũ�Ȳ��ٱ仯
���¶Ⱥ����һ��ʱ,������ѹǿ���ٱ仯
������һ��,��������ƽ����Է����������ٱ仯
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com