
铁及其化合物与生产、生活关系密切,请回答下列问题:
(1)印刷电路板是有高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”。请你写出该反应的离子方程式:___________________。
(2)工业上可用废铁屑制铁红(Fe2O3),生产中首先用废铁屑与HNO3反应制得Fe(NO3)2。写出稀HNO3与过量Fe反应的离子方程式:___ _;从“绿色化学”思想看制备Fe(NO3)2应用浓HNO3还是稀HNO3?并说明理由:______________________
(3)高铁酸盐(FeO42-)是一种新型净水剂,既能净水又能杀菌。请运用所学知识推测高铁酸盐(FeO42-)能用于自来水杀菌消毒的原因:__________。制备它的一种方法是用Fe2(SO4)3和NaClO在强碱性溶液中反应,写出反应的离子方程式:_________________________。
(4)在一定体积的含有Al3+、Fe3+、Ba2+的混合溶液中逐滴加入NaOH和NaSO4的混合溶液(除上述离子外,其他离子不与所加试剂反应),产生沉淀的物质的量与所加溶液的体积的关系如图所示:
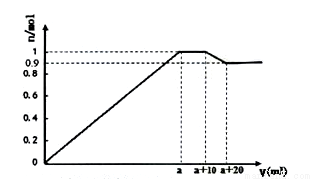
①写出(a+10)到(a+20)过程中反应的离子方程式:_____________
②NaOH和Na2SO4的混合溶液中c(NaOH) c(Na2SO4)(填>、<或=)
③上述含Al3+、Fe3+、Ba2+的混合溶液中n(Al3+)=mol
科目:高中化学 来源:2016届贵州遵义航天高中高三上学期第三次模拟理综化学试卷(解析版) 题型:简答题
1913年,德国化学家哈伯实现了合成氨的工业化生产,被称作解救世界粮食危机的化学天才。现将lmolN2和3molH2投入1L的密闭容器,在一定条件下,利用如下反应模拟哈伯合成氨的工业化生产:N2(g)+3H2(g) 2NH3(g) △H<0
2NH3(g) △H<0
当改变某一外界条件(温度或压强)时,NH3的体积分数ψ(NH3)变化趋势如下图所示。

回答下列问题:
(1)已知:①NH3(g)  NH3(g) △H1
NH3(g) △H1
②N2(g)+3H2(g) 2NH3(l) △H2
2NH3(l) △H2
则反应N2(g)+3H2(g) 2NH3(g)的△H= (用含△H1、△H2的代数式表示)。
2NH3(g)的△H= (用含△H1、△H2的代数式表示)。
(2)合成氨的平衡常数表达式为____ ,平衡时,M点NH3的体积分数为10%,则N2的转化率为 (保留两位有效数字)。
(3)X轴上a点的数值比b点 (填“大”或“小”)。上图中, Y轴表示 (填“温度”或“压强”),判断的理由是 。
(4)若将1mol N2和3mol H2分别投入起始容积为1L的密闭容器中,实验条件和平衡时的相关数据如下表所示:

下列判断正确的是____。
A.放出热量:Ql< Q2< △Hl B. N2的转化率:I> III
C.平衡常数:II >I D.达平衡时氨气的体积分数:I>II
(5)常温下,向VmL amoI.L-l的稀硫酸溶液中滴加等体积bmol.L-l 的氨水,恰好使混合溶液呈中性,此时溶液中c(NH4+)__c(SO42-)(填“>”、“<”或“=”)。
(6)利用氨气设计一种环保燃料电池,一极通入氨气,另一极通入空气,电解质是掺杂氧化钇(Y203)的氧化锆(ZrO2)晶体,它在熔融状态下能传导O2-。写出负极的电极反应式 。
查看答案和解析>>
科目:高中化学 来源:2015-2016浙江宁波效实中学高一上期中考试化学试卷(解析版) 题型:选择题
设NA 表示阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,0.1 mol Cl2 溶于水,转移的电子数目为0.1NA
B.常温常压下,18 g H2O 中含有的原子总数为3NA
C.标准状况下,11.2 L 乙醇中含有的分子数目为0.5NA
D.常温常压下,2.24 L CO 和CO2 混合气体中含有的碳原子数目为0.1NA
查看答案和解析>>
科目:高中化学 来源:2015-2016宁夏回族自治银川一中高一上期中考试化学试卷(解析版) 题型:选择题
科学家刚刚发现了某种元素的原子,其质量是ag,12C的原子质量是bg,NA是阿伏加德罗常数的值,下列说法不正确的是
A.该原子的摩尔质量是aNAg/mol
B.Wg该原子的物质的量一定是 mol
mol
C.Wg该原子中含有 个该原子
个该原子
D.由已知信息可得:NA=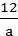
查看答案和解析>>
科目:高中化学 来源:2016届福建省、霞浦七中、周宁十中高三上期中联考化学试卷(解析版) 题型:填空题
要准确掌握化学基本概念和研究方法。按要求回答下列问题:
(1)下列是某同学对有关物质进行分类的列表:
碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
第一组 | Na2CO3 | H2SO4 | NaHCO3 | CaO | CO2 |
第二组 | NaOH | HCl | NaCl | Na2O | CO |
第三组 | NaOH | CH3COOH | CaF2 | Al2O3 | SO2 |
每组分类均有错误,其错误的物质分别是__________(填化学式,下同)、__________、_________。
(2)鉴别胶体和溶液所采用的方法是观察是否能发生__________现象。
(3)一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,按要求回答下列问题:
物质 | M | N | Q | P |
反应前质量(g) | 50 | 1 | 3 | 12 |
反应后质量(g) | X | 26 | 3 | 30 |
①该变化的基本反应类型是___________反应; ②物质Q在反应中起的作用是__________。
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古鄂尔多斯市西部四校高三上学期期中联考化学试卷(解析版) 题型:选择题
金属Ti(钛)是一种具有许多优良性能的较为昂贵的金属,钛和钛合金被认为是21世纪的重要金属材料。某化学兴趣小组用实验探究Ti、Mg、Cu的活泼性顺序。他们在相同温度下,取大小相同的三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,观察现象如下:
金属 | Ti | Mg | Cu |
金属表面现象 | 放出气泡速度缓慢 | 放出气泡速度快 | 无变化 |
下列有关三种金属的说法正确的是
A.三种金属的活泼性由强到弱的顺序是Ti、Mg、Cu
B.若钛粉中混有Mg,提纯Ti时可用稀盐酸除去Mg
C.用Ti从CuSO4溶液中置换出Cu是工业制取Cu的很好途径
D.Cu和稀盐酸不发生化学反应
查看答案和解析>>
科目:高中化学 来源:2016届山东省德州市高三上学期期中测试化学试卷(解析版) 题型:选择题
若NA表示阿伏加德罗常数,下列说法正确的是
A.标准状况下,6.72LNO2与水充分反应转移电子数为0.1NA
B.18gD2O中含有的质子数目为10NA
C.常温常压下,1mol氦气中含有的核外电子数为2NA
D.ag某气体含分子数为b,cg该气体在标况下的体积为22.4ab/(c NA)L
查看答案和解析>>
科目:高中化学 来源:2016届四川省雅安市高三上学期11月月考理综化学试卷(解析版) 题型:选择题
利尿酸是奥运会禁止使用的兴奋剂之一,其结构简式如下图。下列有关利尿酸的说法中正确的是
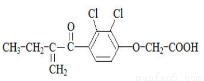
A. 分子式是C13H14O4Cl2
B. 1mol利尿酸最多能与5mol H2发生加成反应
C. 一定条件下能发生加聚、缩聚反应
D. 分子中所有碳原子不可能共平面
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期期中模块测试化学试卷(解析版) 题型:选择题
某溶液中可能含有下列离子: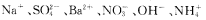 中的某几种离子,为确定该溶液的组成,某同学做了如下实验:
中的某几种离子,为确定该溶液的组成,某同学做了如下实验:
(1)取少量上述溶液,向其中加入硫酸钠溶液,产生白色沉淀,加入稀硝酸沉淀不溶解;
(2)另取少量该溶液,向其中加入足量的NaOH溶液并加热,产生有刺激性气味的气体。则下列有关说法中不正确的是
A.该溶液中一定含有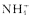
B.该溶液中一定含有硝酸根离子
C.该溶液中一定含有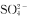
D.根据上述实验不能确定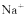 是否存在
是否存在
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com